引用本文: 馬智, 智明, 王文濤. 肝泡型包蟲病根治性切除術后教科書式結局的影響因素:回顧性隊列研究. 中國普外基礎與臨床雜志, 2024, 31(8): 916-923. doi: 10.7507/1007-9424.202402025 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
肝泡型包蟲病(hepatic alveolar echinococcosis,HAE)是一種由多房棘球蚴引起的嚴重疾病,主要感染肝臟[1]。該疾病的特點是肝內病灶生長緩慢且隱匿,常導致確診時病灶往往已侵犯到肝內重要的管道結構[2]。盡管首選的治療方法是根治性切除手術,且術后死亡率已明顯下降,但術后并發癥的發生率并未見顯著降低[3]。并發癥的發生嚴重影響了手術的質量。既往手術質量的評估多采用單一并發癥評估模式,但這種評估方式難以全面覆蓋整個手術過程,導致評估標準化和規范化存在困難[4]。在這種背景下,“教科書式結局”(textbook outcomes,TO)這一以患者為中心的綜合評價指標越來越受到重視[5]。TO綜合考慮了多個參數,并以“全”或“無”的方式反映最佳手術結果,有助于提升復雜手術的整體治療效果,對未來所有外科治療均具有重要意義[6]。目前,TO作為一個綜合性指標,能夠更好地以患者為中心,評估接受外科手術患者的短期預后,已在胃癌、肝癌、胰腺癌等消化道腫瘤的術后研究中得到應用[7]。然而,國內外關于HAE根治性切除術后TO實現的研究相對較少。基于此,本研究采用回顧性研究方法,收集全球HAE發病率最高的四川省甘孜藏族自治州地區的國家級包蟲病研究中心的病例資料,分析HAE術后TO實現的影響因素,并構建預測模型,以協助臨床肝膽醫生進行更有效地臨床決策。
1 資料與方法
1.1 研究對象
通過病例系統回顧性收集2015年至2022年期間在四川大學華西醫院甘孜分院確診的HAE患者,篩選成功接受根治性肝切除手術并通過病理學檢查確診的患者。排除標準:① 年齡>65歲和<18歲的患者;② 接受姑息性切除術、介入手術治療的患者;③ 術前缺乏影像學資料無法進行WHO-PNM分期的患者;④ WHO-PNM分期中有遠處轉移(M1)的患者;⑤ 術后病理學檢查提示囊型和混合型包蟲病的患者;⑥ 術后病理學檢查提示合并有肝臟其他良惡性腫瘤的患者;⑦ 術后并發癥資料缺乏者;⑧ 術后長期隨訪資料缺乏者。
1.2 相關定義
1.2.1 TO
關于HAE術后TO的定義目前尚無統一的共識。本研究根據已有的TO相關研究[8]定義。TO是基于一系列相關的結果來定義的,這些結果代表了患者最佳的手術結果:無術后并發癥、無圍手術期輸血、切緣陰性、無延長的住院時間、出院后90 d內無再次入院以及術后90 d內無死亡。其中再次入院被定義為出院后90 d內的任何醫院入院。切緣陰性定義為病理學檢查肉眼和顯微鏡下無殘余包蟲病灶。當所有期望結果都達到時,即實現了TO。
1.2.2 白蛋白-膽紅素指數(albumin-bilirubin index,ALBI)
ALBI是一種用于評估肝功能的評分系統,于2015年提出,旨在通過簡單的數學公式結合患者的血清膽紅素和白蛋白水平,提供一個更準確的肝功能評估。ALBI評分通過以下公式計算:ALBI評分=(log10總膽紅素×0.66)+[白蛋白×(–0.085)],其中總膽紅素單位為μmol/L,白蛋白單位為g/L。根據得出的評分,患者被分為3個等級:1級(≤–2.60)、2級(>–2.60 且≤–1.39)和3級(>–1.39),分別反映了從較好到較差的肝功能狀態。ALBI評分提供了一個依賴客觀生化指標的肝功能評估工具,有助于臨床醫生更好地預測慢性肝病患者的預后。
1.2.3 肝切除方式
肝切除術后并發癥的研究中,肝切除方式分為大肝切除和小肝切除。大肝切除是指切除3個或以上的肝段,如右半肝切除和左半肝切除,通常風險較高;小肝切除則是切除少于3個肝段,如單個或2個相鄰肝段切除,其創傷和風險較低。這個分類幫助醫生更好地評估手術復雜性和術后預后。
1.2.4 WHO-PNM分期
PNM分期方法是WHO為泡型包蟲病制定的一種分期系統,用于描述疾病的范圍和嚴重程度,幫助醫療專業人員更好地評估患者病情并制定治療方案。PNM分型基于AE的特定病變特征,考慮了病變的解剖部位、鄰近器官的侵犯程度以及遠處轉移情況。具體而言,P(parasite)指寄生蟲相關的肝內病變大小和范圍,包括P1(單個病灶,直徑小于5 cm)、P2(單個病灶,直徑大于等于5 cm,或多個病灶但少于10個)、P3(多個病灶,總數大于等于10個但集中于1個肝葉內)和P4(多個病灶,累及整個肝臟的2個或更多部位);N(neighboring organs)指鄰近器官的侵犯情況,包括N0(無鄰近器官侵犯)、N1(侵犯鄰近器官但不包括主要血管)和N2(侵犯主要血管);M(metastasis)指遠處轉移情況,包括M0(無遠處轉移)和M1(存在遠處轉移)。
1.3 倫理
本研究方案符合1975年《赫爾辛基宣言》(2008年第6次修訂版)的倫理準則,并通過了四川大學華西醫院甘孜分院倫理委員會審批。
1.4 統計學方法
采用R軟件進行統計分析。計數資料以例(%)表示;計量資料按是否服從正態分布分別處理,服從正態分布者以均數±標準差( ±s)表示,不服從正態分布者以中位數(M)及四分位間距(IQR)表示。進行差異性分析時,對于服從正態分布的計量資料,若方差齊性,則進行獨立樣本t檢驗;方差不齊時,則采用Kruskal-Wallis H秩和檢驗。對于計數資料則使用四格表或R×C列聯表χ2檢驗或Fisher確切概率法。最小絕對收縮和選擇算子回歸(least absolute shrinkage and selection operator regression,LASSO)模型(選擇α=1時為L1正則化)通過10折交叉驗證來選擇懲罰系數,旨在選擇使誤差最小化的λ值來建立回歸模型,篩選HAE根治性切除術后發生TO的潛在影響因素。接下來,對所有的因素進行單因素和多因素logistic回歸分析,確定TO的影響因素。在研究初始階段,筆者擬將數據集按7∶3隨機拆分為訓練集和驗證集,但由于樣本量影響模型的泛化能力,筆者決定使用全部數據進行模型訓練,以提高模型的穩定性和預測效能。預測模型結果通過Nomogram圖展示,以便直觀評估各預測變量對術后TO風險的影響。隨后,采用受試者工作特征(receiver operating characteristic,ROC)曲線分析模型的預測性能,并計算曲線下面積(area under curve,AUC)、C-index以評估模型在不同閾值下的敏感性和特異性,最后通過Bootstrap法進行1 000次內部抽樣進行內部驗證,獲得預測模型的95%置信區間(confidence interval,CI)。檢驗水準α=0.05。
±s)表示,不服從正態分布者以中位數(M)及四分位間距(IQR)表示。進行差異性分析時,對于服從正態分布的計量資料,若方差齊性,則進行獨立樣本t檢驗;方差不齊時,則采用Kruskal-Wallis H秩和檢驗。對于計數資料則使用四格表或R×C列聯表χ2檢驗或Fisher確切概率法。最小絕對收縮和選擇算子回歸(least absolute shrinkage and selection operator regression,LASSO)模型(選擇α=1時為L1正則化)通過10折交叉驗證來選擇懲罰系數,旨在選擇使誤差最小化的λ值來建立回歸模型,篩選HAE根治性切除術后發生TO的潛在影響因素。接下來,對所有的因素進行單因素和多因素logistic回歸分析,確定TO的影響因素。在研究初始階段,筆者擬將數據集按7∶3隨機拆分為訓練集和驗證集,但由于樣本量影響模型的泛化能力,筆者決定使用全部數據進行模型訓練,以提高模型的穩定性和預測效能。預測模型結果通過Nomogram圖展示,以便直觀評估各預測變量對術后TO風險的影響。隨后,采用受試者工作特征(receiver operating characteristic,ROC)曲線分析模型的預測性能,并計算曲線下面積(area under curve,AUC)、C-index以評估模型在不同閾值下的敏感性和特異性,最后通過Bootstrap法進行1 000次內部抽樣進行內部驗證,獲得預測模型的95%置信區間(confidence interval,CI)。檢驗水準α=0.05。
2 結果
2.1 TO組和非TO組患者的臨床資料比較
共計427例HAE患者納入本研究,均接受了根治性肝切除術,患者的人口學資料、術前影像學特征、實驗室資料、肝功能評分、手術情況、術后住院時間以及住院費用見表1。
427例患者中,174例(40.7%)實現了TO。TO組患者與非TO組患者的年齡、性別、體質量指數、病灶數目、病灶部位、丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、凝血酶原時間、國際標準化比值、合并乙肝情況比較差異均無統計學意義(P>0.05);但2組的P分期、N分期、病灶直徑、前白蛋白、白蛋白、ALBI、切肝方式、術后住院時間、住院費用比較差異有統計學意義(P<0.05),相較于非TO組,TO組患者的P分期1+2期、N0期、ALBI≤–2.6、病灶直徑≤10 cm、小肝切除比例高,前白蛋白和白蛋白水平高,術后住院時間短,住院費用低。見表1。
2.2 TO影響因素分析
2.2.1 LASSO回歸分析
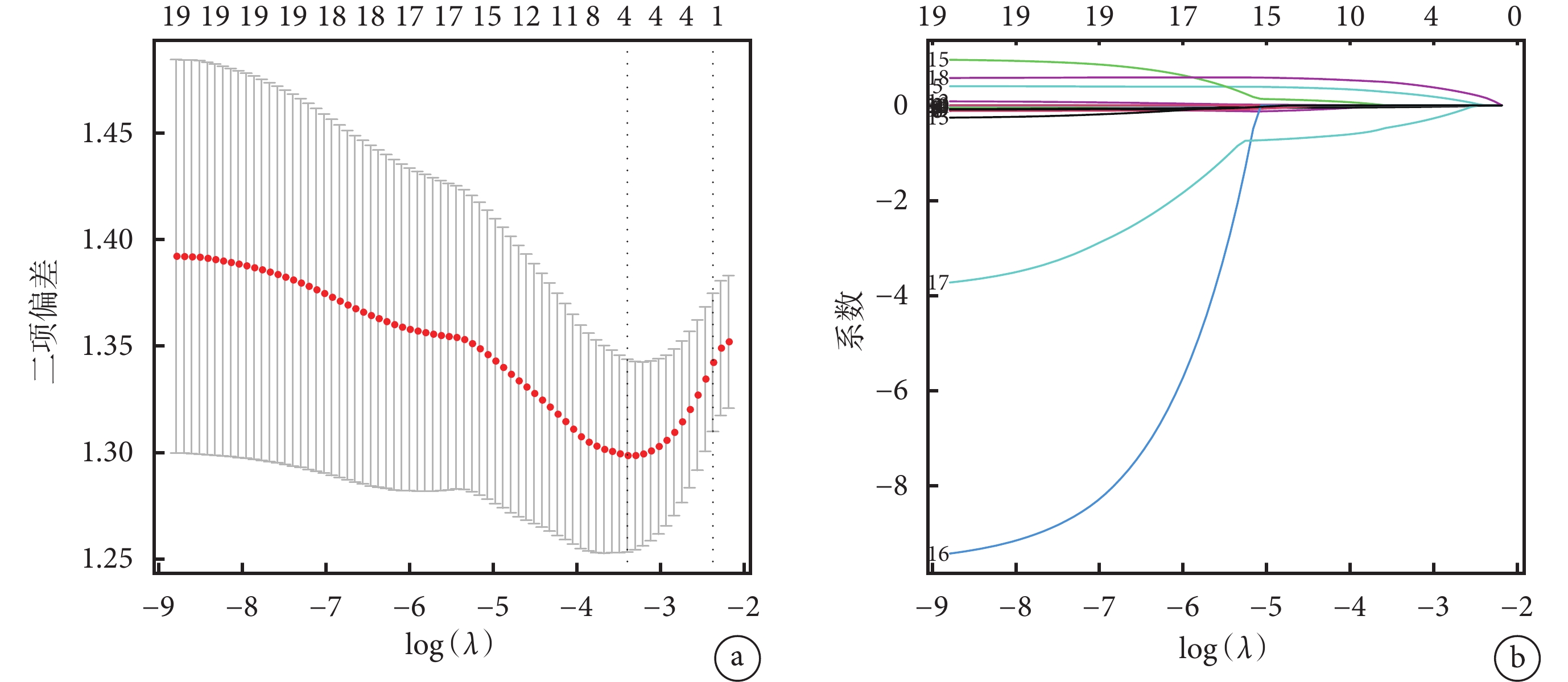
在本研究中,筆者將表1中的人口學特征數據(年齡、性別、體質量指數)、術前檢查指標(P分期、N分期、病灶直徑、病灶數目、侵犯部位)、實驗室檢查指標(丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、前白蛋白、白蛋白、凝血酶原時間、國際標準化比值)、肝功能評價指標(ALBI)、是否感染乙肝及術中肝切除方式共18個指標納入LASSO回歸模型,初步篩選出與患者術后TO達成相關的潛在影響因素。圖1展示了最優模型(λ=0.033 613 27,預測模型A),圖1a顯示隨著正則化參數的增加,4個變量系數保持非零,具體回歸系數見表2。篩選出的變量包括:P分期、病灶直徑、ALBI及切肝方式。其中P 1+2期者的TO率高于P 3+4期者,病灶直徑≤10 cm者的TO率高于病灶直徑>10 cm者,ALBI≤–2.6者的TO率高于ALBI>–2.6者,小肝切除者的TO率高于大肝切除者。
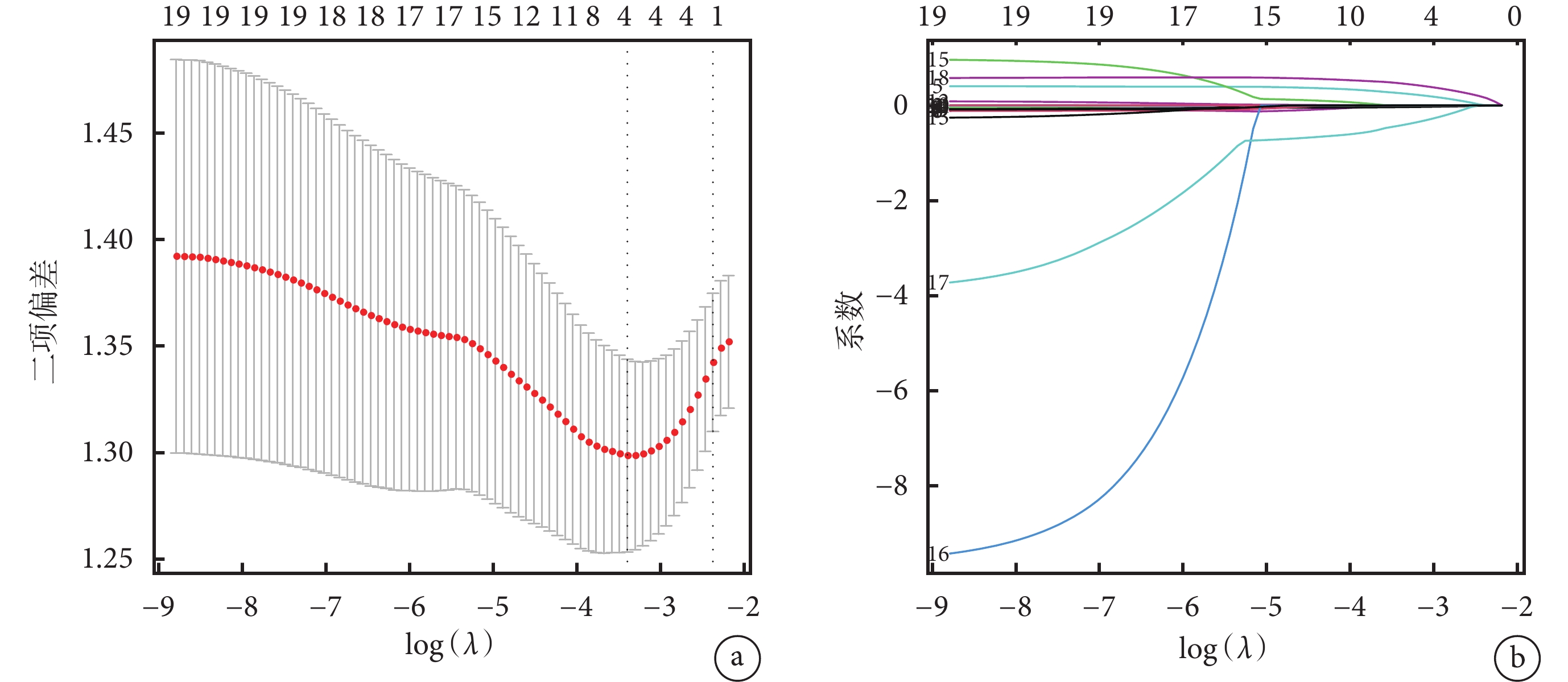 圖1
示LASSO回歸的系數路徑圖(a)和交叉驗證曲線(b)
圖1
示LASSO回歸的系數路徑圖(a)和交叉驗證曲線(b)
2.2.2 單因素和多因素logistic回歸分析
在本研究中,筆者將表1中人口學特征數據(年齡、性別、體質量指數)、術前檢查指標(P分期、N分期、病灶直徑、病灶數目、侵犯部位)、實驗室檢查指標(丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、前白蛋白、白蛋白、凝血酶原時間、國際標準化比值)、肝功能評價指標(ALBI)、是否感染乙肝以及術中切肝方式共計18項指標首先進行單因素分析,然后再進行多因素logistic回歸分析,探索HAE患者術后TO的影響因素,見表3。單因素分析結果表明,病灶直徑、P分期、N分期、白蛋白、ALBI、切肝方式是HAE術后實現TO的影響因素(P<0.05)。多因素分析結果(預測模型B)表明,P分期和切肝方式是HAE術后TO的影響因素(P<0.05),其中P 1+2期者的TO率高于P 3+4期者(OR=1.800,P=0.025),小肝切除者的TO率高于大肝切除者(OR=1.974,P<0.001)。
2.3 HAE術后TO預測模型列線圖的建立及驗證
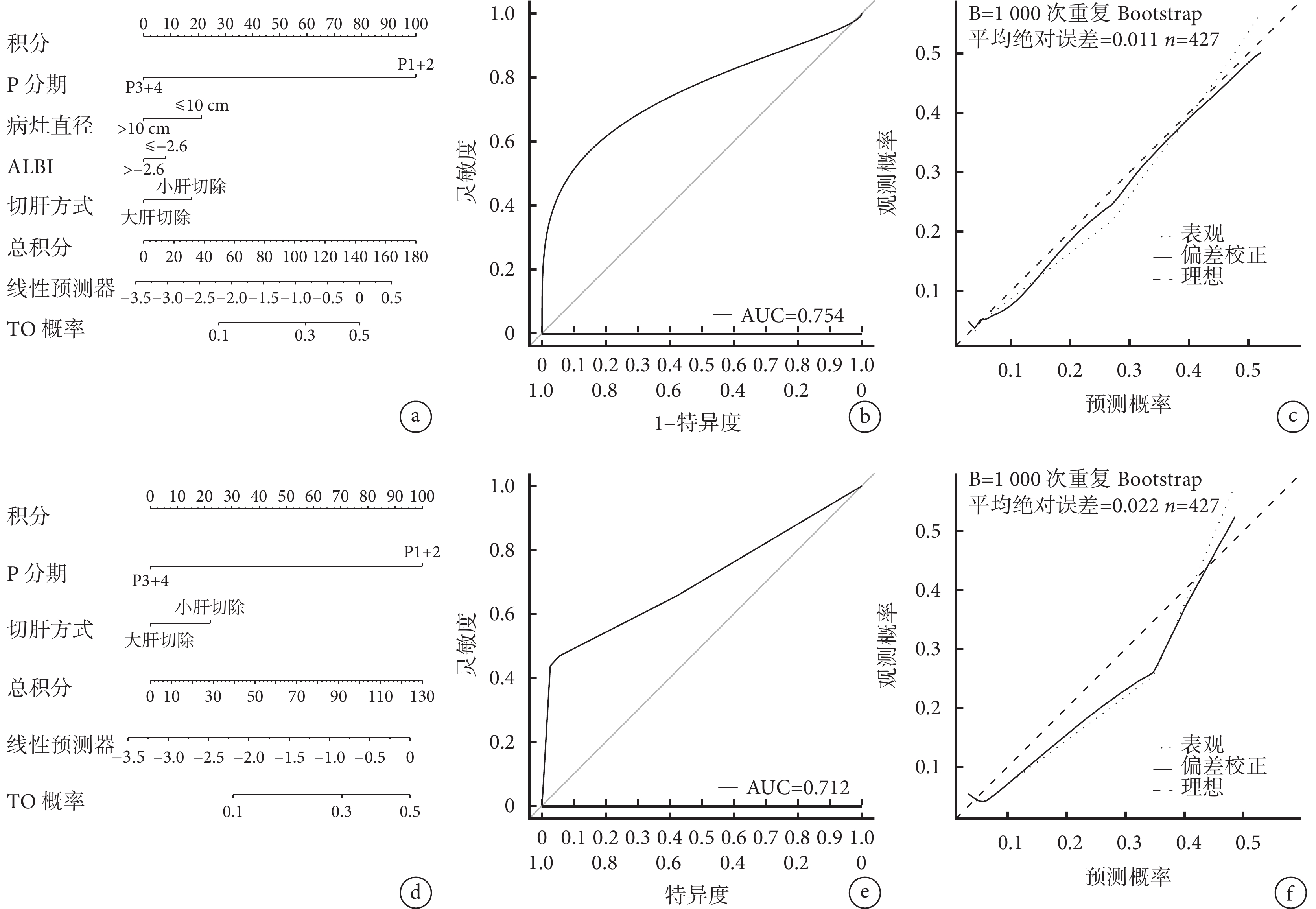
本項研究中,筆者分別基于LASSO回歸分析結果建立了TO預測模型A,以及基于多因素logistic回歸分析結果建立了TO預測模型B,旨在預測HAE患者在接受根治性切除術后實現TO的概率,并且對該2個模型分別進行了準確性(ROC曲線分析、C-index計算)、穩定性(Bootstrap 1 000次內部驗證校準曲線分析)評價,見圖2。具體來說,在預測模型A,當患者總得分為188分時,實現TO的預測概率為50%,該預測模型的AUC值為0.754(0.662,0.862),C-index=0.756,校準曲線顯示該預測模型在各個預測概率區間內的校準情況良好;大多數點接近對角線,表明模型預測的術后TO概率與實際發生概率高度一致。在某些區間內,模型略微高估/低估了實際發生概率,但總體趨勢仍然較好。
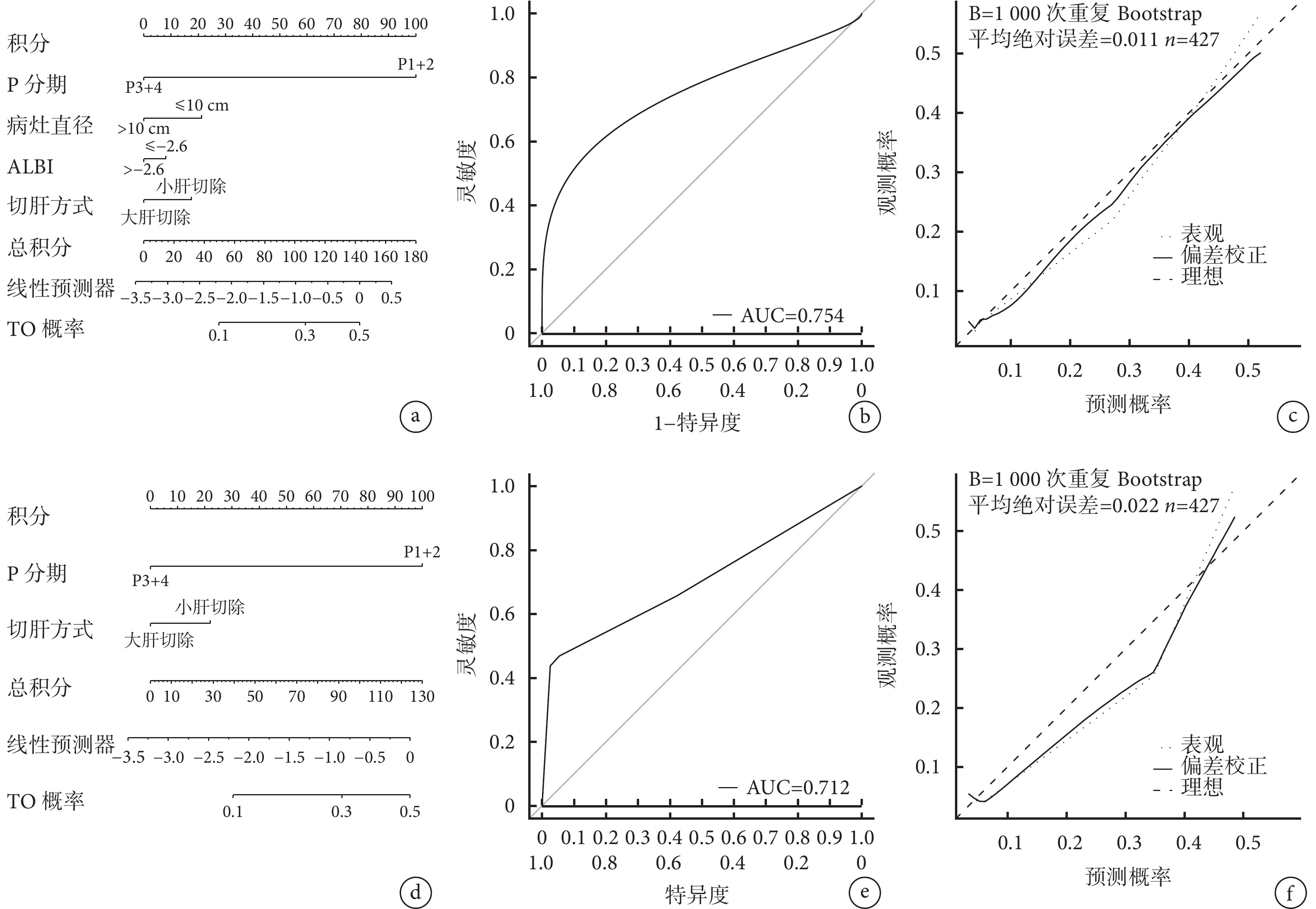 圖2
示TO預測模型列線圖、內部驗證ROC曲線以及Bootstrap 1 000次內部驗證的校準曲線
圖2
示TO預測模型列線圖、內部驗證ROC曲線以及Bootstrap 1 000次內部驗證的校準曲線
a~c:預測模型A的列線圖(a)、內部驗證ROC曲線(b)以及校準曲線(c);d~f:預測模型B的列線圖(d)、內部驗證ROC曲線(e)以及校準曲線(f)
對預測模型B,當患者總得分為160分時,實現TO的預測概率為50%,該預測模型的AUC值為0.712(0.618,0.816),C-index=0.707。校準曲線顯示預測模型B相較于預測模型A,大多數偏離對角線,模型略微高估/低估了實際發生概率。結果表明,基于P分期、病灶直徑、ALBI、切肝方式建立的預測模型A在區分HAE術后TO發生概率方面相較于僅基于P分期和切肝方式建立的預測模型具備較為理想的準確性和穩定性。
3 討論
肝包蟲病(hepatic echinococcosis,HE)分為HAE和肝囊型包蟲病(hepatic cystic echinococcosis,HCE)2種類型,其中根治性切除寄生蟲病灶是治療的首選[9-10]。相比于HCE,HAE的發病率較低,因此大部分關于HE手術后治療效果的研究主要集中在HCE上。然而,HAE通常表現為浸潤性生長的病灶,其病情更加復雜,根治性切除手術中面臨更大的挑戰,術后患者的恢復情況也存在顯著的差異,因此,對HAE術后的研究顯得尤為重要。筆者所在研究中心位于全球HAE發病率最高的地區—中國四川省甘孜藏族自治州。本研究結果顯示,僅有約40%的接受根治性切除的HAE實現了TO,這一發現對未來的治療策略和研究方向具有重要意義。筆者比較了TO組和非TO組患者的醫療費用和術后住院時間,結果實現TO的患者的醫療費用比非TO患者節約人民幣10 988元,住院時間減少4 d。因此,TO可能是一個評價HAE患者根治性手術質量更好的綜合價值指標—結合了高質量與較低成本。因此,專注于提高TO的比例不僅可以優化患者護理,還可以降低醫療保健成本,并帶來性價比高的高價值護理。
多個病灶本身的解剖學特點、圍手術期指標和手術因素影響了HAE術后TO的實現(見圖1、表3)。其中LASSO回歸分析、多因素logistic回歸分析均表明,包蟲病灶解剖學因素是患者術后TO達成重要的影響因素,究其原因,原發包蟲侵犯肝臟一、二和三肝門的比例在P 3+4期者中高。P 3+4期患者由于侵犯第一肝門結構,導致手術常常涉及一級膽管切除、膽管匯合部切除、整形和包括膽腸吻合在內的膽道重建,使其術后出現各種并發癥的風險增高,延長了住院時間,顯著影響了TO的實現,此與既往研究[11-12]結論吻合。另一個特別引人注目的發現是,LASSO回歸、單因素logistic回歸分析均表明,與TO顯著相關的因素有ALBI。這一發現很重要,因為與攜帶肝背景異常(如慢性乙肝病毒性肝炎、脂肪性肝炎、非酒精性脂肪性肝炎)的肝惡性腫瘤患者不同,HAE患者通常不表現出明顯肝指標異常,往往被視為肝功能正常[13-14]。這表明HAE患者也可能存在肝功能下降,只是這種下降可能更加隱匿。盡管在多因素logistic回歸分析中,ALBI指標未能繼續作為影響TO實現的因素,但這一結果再次表明,HAE術后的并發癥仍主要與HE的解剖學特征密切相關。但這一發現并非否認了維護良好的肝功能以及提供適當的營養支持在提高HAE肝切除手術效果中的重要性。其次,在手術方式的選擇上,小肝切除與大肝切除相比,更有利于實現TO。這一發現并不意外,因為后者導致的術后殘余肝臟體積不足與重大并發癥相關,特別是肝功能衰竭[15-17]。但這對于實現TO具有現實意義,尤其是在處理位于肝門部等特殊位置的小病灶時。為了避免HAE術后復發風險,許多醫生傾向于模仿肝癌治療,嘗試保證至少2 cm的切緣,但這可能增加手術難度,對實現TO產生負面影響[18-19]。考慮到HAE病灶生長緩慢,且R0切除加上適量、足夠療程的阿苯達唑治療可帶來良好的長期預后,因此筆者建議盡量選擇小肝切除。
本研究進一步利用上述影響TO的關鍵因素,開發了2個列線圖,用于預測HAE患者在根治性切除后實現TO的可能性。列線圖是預后分析工具,旨在通過特定臨床變量以更準確估計個體的風險和治療效果[20-22]。本研究中預測模型A經過了內部驗證,展示出了較好的預測性能和穩定性。它的優點在于綜合考慮了HAE病灶的解剖學特征(病期、直徑)、患者肝功能狀態及手術方法。其局限在于圍手術期變量數據較少。若對病灶特征進行量化分析,有望進一步提高預測模型的精確度。該研究為識別有望實現TO的患者提供了數據支持,指明了未來更詳細列線圖研究和干預措施的方向。
總之,在接受根治性切除的HAE患者中,實現TO的比例未達到一半。致力于實現TO不僅能顯著縮短患者的住院時間,還能有效降低醫療費用。具體來說,提高TO的比例應該是HAE根治性切除術的最高價值目標。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:馬智負責所有患者的臨床數據收集、隨訪等;智明負責臨床數據整理、分析;2位作者共同完成了文章的撰寫、修改。王文濤指導文章。
倫理聲明:本研究通過了甘孜州人民醫院醫學倫理委員會審批(批文編號:GYYLY20240613)。
肝泡型包蟲病(hepatic alveolar echinococcosis,HAE)是一種由多房棘球蚴引起的嚴重疾病,主要感染肝臟[1]。該疾病的特點是肝內病灶生長緩慢且隱匿,常導致確診時病灶往往已侵犯到肝內重要的管道結構[2]。盡管首選的治療方法是根治性切除手術,且術后死亡率已明顯下降,但術后并發癥的發生率并未見顯著降低[3]。并發癥的發生嚴重影響了手術的質量。既往手術質量的評估多采用單一并發癥評估模式,但這種評估方式難以全面覆蓋整個手術過程,導致評估標準化和規范化存在困難[4]。在這種背景下,“教科書式結局”(textbook outcomes,TO)這一以患者為中心的綜合評價指標越來越受到重視[5]。TO綜合考慮了多個參數,并以“全”或“無”的方式反映最佳手術結果,有助于提升復雜手術的整體治療效果,對未來所有外科治療均具有重要意義[6]。目前,TO作為一個綜合性指標,能夠更好地以患者為中心,評估接受外科手術患者的短期預后,已在胃癌、肝癌、胰腺癌等消化道腫瘤的術后研究中得到應用[7]。然而,國內外關于HAE根治性切除術后TO實現的研究相對較少。基于此,本研究采用回顧性研究方法,收集全球HAE發病率最高的四川省甘孜藏族自治州地區的國家級包蟲病研究中心的病例資料,分析HAE術后TO實現的影響因素,并構建預測模型,以協助臨床肝膽醫生進行更有效地臨床決策。
1 資料與方法
1.1 研究對象
通過病例系統回顧性收集2015年至2022年期間在四川大學華西醫院甘孜分院確診的HAE患者,篩選成功接受根治性肝切除手術并通過病理學檢查確診的患者。排除標準:① 年齡>65歲和<18歲的患者;② 接受姑息性切除術、介入手術治療的患者;③ 術前缺乏影像學資料無法進行WHO-PNM分期的患者;④ WHO-PNM分期中有遠處轉移(M1)的患者;⑤ 術后病理學檢查提示囊型和混合型包蟲病的患者;⑥ 術后病理學檢查提示合并有肝臟其他良惡性腫瘤的患者;⑦ 術后并發癥資料缺乏者;⑧ 術后長期隨訪資料缺乏者。
1.2 相關定義
1.2.1 TO
關于HAE術后TO的定義目前尚無統一的共識。本研究根據已有的TO相關研究[8]定義。TO是基于一系列相關的結果來定義的,這些結果代表了患者最佳的手術結果:無術后并發癥、無圍手術期輸血、切緣陰性、無延長的住院時間、出院后90 d內無再次入院以及術后90 d內無死亡。其中再次入院被定義為出院后90 d內的任何醫院入院。切緣陰性定義為病理學檢查肉眼和顯微鏡下無殘余包蟲病灶。當所有期望結果都達到時,即實現了TO。
1.2.2 白蛋白-膽紅素指數(albumin-bilirubin index,ALBI)
ALBI是一種用于評估肝功能的評分系統,于2015年提出,旨在通過簡單的數學公式結合患者的血清膽紅素和白蛋白水平,提供一個更準確的肝功能評估。ALBI評分通過以下公式計算:ALBI評分=(log10總膽紅素×0.66)+[白蛋白×(–0.085)],其中總膽紅素單位為μmol/L,白蛋白單位為g/L。根據得出的評分,患者被分為3個等級:1級(≤–2.60)、2級(>–2.60 且≤–1.39)和3級(>–1.39),分別反映了從較好到較差的肝功能狀態。ALBI評分提供了一個依賴客觀生化指標的肝功能評估工具,有助于臨床醫生更好地預測慢性肝病患者的預后。
1.2.3 肝切除方式
肝切除術后并發癥的研究中,肝切除方式分為大肝切除和小肝切除。大肝切除是指切除3個或以上的肝段,如右半肝切除和左半肝切除,通常風險較高;小肝切除則是切除少于3個肝段,如單個或2個相鄰肝段切除,其創傷和風險較低。這個分類幫助醫生更好地評估手術復雜性和術后預后。
1.2.4 WHO-PNM分期
PNM分期方法是WHO為泡型包蟲病制定的一種分期系統,用于描述疾病的范圍和嚴重程度,幫助醫療專業人員更好地評估患者病情并制定治療方案。PNM分型基于AE的特定病變特征,考慮了病變的解剖部位、鄰近器官的侵犯程度以及遠處轉移情況。具體而言,P(parasite)指寄生蟲相關的肝內病變大小和范圍,包括P1(單個病灶,直徑小于5 cm)、P2(單個病灶,直徑大于等于5 cm,或多個病灶但少于10個)、P3(多個病灶,總數大于等于10個但集中于1個肝葉內)和P4(多個病灶,累及整個肝臟的2個或更多部位);N(neighboring organs)指鄰近器官的侵犯情況,包括N0(無鄰近器官侵犯)、N1(侵犯鄰近器官但不包括主要血管)和N2(侵犯主要血管);M(metastasis)指遠處轉移情況,包括M0(無遠處轉移)和M1(存在遠處轉移)。
1.3 倫理
本研究方案符合1975年《赫爾辛基宣言》(2008年第6次修訂版)的倫理準則,并通過了四川大學華西醫院甘孜分院倫理委員會審批。
1.4 統計學方法
采用R軟件進行統計分析。計數資料以例(%)表示;計量資料按是否服從正態分布分別處理,服從正態分布者以均數±標準差( ±s)表示,不服從正態分布者以中位數(M)及四分位間距(IQR)表示。進行差異性分析時,對于服從正態分布的計量資料,若方差齊性,則進行獨立樣本t檢驗;方差不齊時,則采用Kruskal-Wallis H秩和檢驗。對于計數資料則使用四格表或R×C列聯表χ2檢驗或Fisher確切概率法。最小絕對收縮和選擇算子回歸(least absolute shrinkage and selection operator regression,LASSO)模型(選擇α=1時為L1正則化)通過10折交叉驗證來選擇懲罰系數,旨在選擇使誤差最小化的λ值來建立回歸模型,篩選HAE根治性切除術后發生TO的潛在影響因素。接下來,對所有的因素進行單因素和多因素logistic回歸分析,確定TO的影響因素。在研究初始階段,筆者擬將數據集按7∶3隨機拆分為訓練集和驗證集,但由于樣本量影響模型的泛化能力,筆者決定使用全部數據進行模型訓練,以提高模型的穩定性和預測效能。預測模型結果通過Nomogram圖展示,以便直觀評估各預測變量對術后TO風險的影響。隨后,采用受試者工作特征(receiver operating characteristic,ROC)曲線分析模型的預測性能,并計算曲線下面積(area under curve,AUC)、C-index以評估模型在不同閾值下的敏感性和特異性,最后通過Bootstrap法進行1 000次內部抽樣進行內部驗證,獲得預測模型的95%置信區間(confidence interval,CI)。檢驗水準α=0.05。
±s)表示,不服從正態分布者以中位數(M)及四分位間距(IQR)表示。進行差異性分析時,對于服從正態分布的計量資料,若方差齊性,則進行獨立樣本t檢驗;方差不齊時,則采用Kruskal-Wallis H秩和檢驗。對于計數資料則使用四格表或R×C列聯表χ2檢驗或Fisher確切概率法。最小絕對收縮和選擇算子回歸(least absolute shrinkage and selection operator regression,LASSO)模型(選擇α=1時為L1正則化)通過10折交叉驗證來選擇懲罰系數,旨在選擇使誤差最小化的λ值來建立回歸模型,篩選HAE根治性切除術后發生TO的潛在影響因素。接下來,對所有的因素進行單因素和多因素logistic回歸分析,確定TO的影響因素。在研究初始階段,筆者擬將數據集按7∶3隨機拆分為訓練集和驗證集,但由于樣本量影響模型的泛化能力,筆者決定使用全部數據進行模型訓練,以提高模型的穩定性和預測效能。預測模型結果通過Nomogram圖展示,以便直觀評估各預測變量對術后TO風險的影響。隨后,采用受試者工作特征(receiver operating characteristic,ROC)曲線分析模型的預測性能,并計算曲線下面積(area under curve,AUC)、C-index以評估模型在不同閾值下的敏感性和特異性,最后通過Bootstrap法進行1 000次內部抽樣進行內部驗證,獲得預測模型的95%置信區間(confidence interval,CI)。檢驗水準α=0.05。
2 結果
2.1 TO組和非TO組患者的臨床資料比較
共計427例HAE患者納入本研究,均接受了根治性肝切除術,患者的人口學資料、術前影像學特征、實驗室資料、肝功能評分、手術情況、術后住院時間以及住院費用見表1。
427例患者中,174例(40.7%)實現了TO。TO組患者與非TO組患者的年齡、性別、體質量指數、病灶數目、病灶部位、丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、凝血酶原時間、國際標準化比值、合并乙肝情況比較差異均無統計學意義(P>0.05);但2組的P分期、N分期、病灶直徑、前白蛋白、白蛋白、ALBI、切肝方式、術后住院時間、住院費用比較差異有統計學意義(P<0.05),相較于非TO組,TO組患者的P分期1+2期、N0期、ALBI≤–2.6、病灶直徑≤10 cm、小肝切除比例高,前白蛋白和白蛋白水平高,術后住院時間短,住院費用低。見表1。
2.2 TO影響因素分析
2.2.1 LASSO回歸分析
在本研究中,筆者將表1中的人口學特征數據(年齡、性別、體質量指數)、術前檢查指標(P分期、N分期、病灶直徑、病灶數目、侵犯部位)、實驗室檢查指標(丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、前白蛋白、白蛋白、凝血酶原時間、國際標準化比值)、肝功能評價指標(ALBI)、是否感染乙肝及術中肝切除方式共18個指標納入LASSO回歸模型,初步篩選出與患者術后TO達成相關的潛在影響因素。圖1展示了最優模型(λ=0.033 613 27,預測模型A),圖1a顯示隨著正則化參數的增加,4個變量系數保持非零,具體回歸系數見表2。篩選出的變量包括:P分期、病灶直徑、ALBI及切肝方式。其中P 1+2期者的TO率高于P 3+4期者,病灶直徑≤10 cm者的TO率高于病灶直徑>10 cm者,ALBI≤–2.6者的TO率高于ALBI>–2.6者,小肝切除者的TO率高于大肝切除者。
 圖1
示LASSO回歸的系數路徑圖(a)和交叉驗證曲線(b)
圖1
示LASSO回歸的系數路徑圖(a)和交叉驗證曲線(b)
2.2.2 單因素和多因素logistic回歸分析
在本研究中,筆者將表1中人口學特征數據(年齡、性別、體質量指數)、術前檢查指標(P分期、N分期、病灶直徑、病灶數目、侵犯部位)、實驗室檢查指標(丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、總膽紅素、前白蛋白、白蛋白、凝血酶原時間、國際標準化比值)、肝功能評價指標(ALBI)、是否感染乙肝以及術中切肝方式共計18項指標首先進行單因素分析,然后再進行多因素logistic回歸分析,探索HAE患者術后TO的影響因素,見表3。單因素分析結果表明,病灶直徑、P分期、N分期、白蛋白、ALBI、切肝方式是HAE術后實現TO的影響因素(P<0.05)。多因素分析結果(預測模型B)表明,P分期和切肝方式是HAE術后TO的影響因素(P<0.05),其中P 1+2期者的TO率高于P 3+4期者(OR=1.800,P=0.025),小肝切除者的TO率高于大肝切除者(OR=1.974,P<0.001)。
2.3 HAE術后TO預測模型列線圖的建立及驗證
本項研究中,筆者分別基于LASSO回歸分析結果建立了TO預測模型A,以及基于多因素logistic回歸分析結果建立了TO預測模型B,旨在預測HAE患者在接受根治性切除術后實現TO的概率,并且對該2個模型分別進行了準確性(ROC曲線分析、C-index計算)、穩定性(Bootstrap 1 000次內部驗證校準曲線分析)評價,見圖2。具體來說,在預測模型A,當患者總得分為188分時,實現TO的預測概率為50%,該預測模型的AUC值為0.754(0.662,0.862),C-index=0.756,校準曲線顯示該預測模型在各個預測概率區間內的校準情況良好;大多數點接近對角線,表明模型預測的術后TO概率與實際發生概率高度一致。在某些區間內,模型略微高估/低估了實際發生概率,但總體趨勢仍然較好。
 圖2
示TO預測模型列線圖、內部驗證ROC曲線以及Bootstrap 1 000次內部驗證的校準曲線
圖2
示TO預測模型列線圖、內部驗證ROC曲線以及Bootstrap 1 000次內部驗證的校準曲線
a~c:預測模型A的列線圖(a)、內部驗證ROC曲線(b)以及校準曲線(c);d~f:預測模型B的列線圖(d)、內部驗證ROC曲線(e)以及校準曲線(f)
對預測模型B,當患者總得分為160分時,實現TO的預測概率為50%,該預測模型的AUC值為0.712(0.618,0.816),C-index=0.707。校準曲線顯示預測模型B相較于預測模型A,大多數偏離對角線,模型略微高估/低估了實際發生概率。結果表明,基于P分期、病灶直徑、ALBI、切肝方式建立的預測模型A在區分HAE術后TO發生概率方面相較于僅基于P分期和切肝方式建立的預測模型具備較為理想的準確性和穩定性。
3 討論
肝包蟲病(hepatic echinococcosis,HE)分為HAE和肝囊型包蟲病(hepatic cystic echinococcosis,HCE)2種類型,其中根治性切除寄生蟲病灶是治療的首選[9-10]。相比于HCE,HAE的發病率較低,因此大部分關于HE手術后治療效果的研究主要集中在HCE上。然而,HAE通常表現為浸潤性生長的病灶,其病情更加復雜,根治性切除手術中面臨更大的挑戰,術后患者的恢復情況也存在顯著的差異,因此,對HAE術后的研究顯得尤為重要。筆者所在研究中心位于全球HAE發病率最高的地區—中國四川省甘孜藏族自治州。本研究結果顯示,僅有約40%的接受根治性切除的HAE實現了TO,這一發現對未來的治療策略和研究方向具有重要意義。筆者比較了TO組和非TO組患者的醫療費用和術后住院時間,結果實現TO的患者的醫療費用比非TO患者節約人民幣10 988元,住院時間減少4 d。因此,TO可能是一個評價HAE患者根治性手術質量更好的綜合價值指標—結合了高質量與較低成本。因此,專注于提高TO的比例不僅可以優化患者護理,還可以降低醫療保健成本,并帶來性價比高的高價值護理。
多個病灶本身的解剖學特點、圍手術期指標和手術因素影響了HAE術后TO的實現(見圖1、表3)。其中LASSO回歸分析、多因素logistic回歸分析均表明,包蟲病灶解剖學因素是患者術后TO達成重要的影響因素,究其原因,原發包蟲侵犯肝臟一、二和三肝門的比例在P 3+4期者中高。P 3+4期患者由于侵犯第一肝門結構,導致手術常常涉及一級膽管切除、膽管匯合部切除、整形和包括膽腸吻合在內的膽道重建,使其術后出現各種并發癥的風險增高,延長了住院時間,顯著影響了TO的實現,此與既往研究[11-12]結論吻合。另一個特別引人注目的發現是,LASSO回歸、單因素logistic回歸分析均表明,與TO顯著相關的因素有ALBI。這一發現很重要,因為與攜帶肝背景異常(如慢性乙肝病毒性肝炎、脂肪性肝炎、非酒精性脂肪性肝炎)的肝惡性腫瘤患者不同,HAE患者通常不表現出明顯肝指標異常,往往被視為肝功能正常[13-14]。這表明HAE患者也可能存在肝功能下降,只是這種下降可能更加隱匿。盡管在多因素logistic回歸分析中,ALBI指標未能繼續作為影響TO實現的因素,但這一結果再次表明,HAE術后的并發癥仍主要與HE的解剖學特征密切相關。但這一發現并非否認了維護良好的肝功能以及提供適當的營養支持在提高HAE肝切除手術效果中的重要性。其次,在手術方式的選擇上,小肝切除與大肝切除相比,更有利于實現TO。這一發現并不意外,因為后者導致的術后殘余肝臟體積不足與重大并發癥相關,特別是肝功能衰竭[15-17]。但這對于實現TO具有現實意義,尤其是在處理位于肝門部等特殊位置的小病灶時。為了避免HAE術后復發風險,許多醫生傾向于模仿肝癌治療,嘗試保證至少2 cm的切緣,但這可能增加手術難度,對實現TO產生負面影響[18-19]。考慮到HAE病灶生長緩慢,且R0切除加上適量、足夠療程的阿苯達唑治療可帶來良好的長期預后,因此筆者建議盡量選擇小肝切除。
本研究進一步利用上述影響TO的關鍵因素,開發了2個列線圖,用于預測HAE患者在根治性切除后實現TO的可能性。列線圖是預后分析工具,旨在通過特定臨床變量以更準確估計個體的風險和治療效果[20-22]。本研究中預測模型A經過了內部驗證,展示出了較好的預測性能和穩定性。它的優點在于綜合考慮了HAE病灶的解剖學特征(病期、直徑)、患者肝功能狀態及手術方法。其局限在于圍手術期變量數據較少。若對病灶特征進行量化分析,有望進一步提高預測模型的精確度。該研究為識別有望實現TO的患者提供了數據支持,指明了未來更詳細列線圖研究和干預措施的方向。
總之,在接受根治性切除的HAE患者中,實現TO的比例未達到一半。致力于實現TO不僅能顯著縮短患者的住院時間,還能有效降低醫療費用。具體來說,提高TO的比例應該是HAE根治性切除術的最高價值目標。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:馬智負責所有患者的臨床數據收集、隨訪等;智明負責臨床數據整理、分析;2位作者共同完成了文章的撰寫、修改。王文濤指導文章。
倫理聲明:本研究通過了甘孜州人民醫院醫學倫理委員會審批(批文編號:GYYLY20240613)。