引用本文: 沈寅知, 黃斌, 袁丁, 趙紀春. 探究Stanford B型主動脈夾層合并單發左側椎動脈對胸主動脈覆膜支架修復術后結局的影響. 中國普外基礎與臨床雜志, 2024, 31(8): 961-967. doi: 10.7507/1007-9424.202403028 復制
版權信息: ?四川大學華西醫院華西期刊社《中國普外基礎與臨床雜志》版權所有,未經授權不得轉載、改編
Stanford B型主動脈夾層(type B aortic dissection,TBAD)由于其高并發癥率和高死亡率的特征[1-2],始終是血管外科領域的研究熱點。單發左側椎動脈(isolated left vertebral artery,ILVA)指生理情況下起自左鎖骨下動脈的左椎動脈直接自主動脈弓發出,據報道在TBAD患者中占比約3.6%[3]。TBAD患者合并ILVA將增加胸主動脈腔內覆膜支架修復術(thoracic endovascular aortic repair,TEVAR)的手術難度,并可能引起卒中等嚴重并發癥[4]。然而,由于ILVA的發生率低,其中罹患TBAD的患者更為少見,目前學界對其與TEVAR術后結局事件的關系不甚明確。因此,本研究基于回顧性隊列研究,分析了行TEVAR手術的TBAD患者的臨床及影像資料,旨在探究合并IVLA對TBAD患者TEVAR術后結局的影響,以利于臨床醫生對該解剖變異的深入理解,個性化制定手術方案。
1 資料與方法
1.1 研究對象
本研究患者納入標準:① 術前經胸腹部計算機體層血管成像(computed tomography angiography,CTA)確診為 Stanford B型主動脈夾層即Debakey Ⅲa/Ⅲb型主動脈夾層,包括近年來新提出的非A非B型夾層;② 接受TEVAR手術,即于胸主動脈接受覆膜支架系統植入;③ 術后至少行1次胸腹部CTA影像隨訪檢查,且該次檢查距手術間隔時間 ≥90 d;④ 入院后臨床數據及術前CTA圖像可查。排除標準:① 孤立性胸主動脈瘤;② 胸主動脈穿通性潰瘍及壁間血腫;③ 累及長度小于2 cm的局限性主動脈夾層;④ 病例信息不完整或術前CTA圖像缺失;⑤ 既往曾于胸主動脈植入覆膜支架;⑥ 術后90 d后無夾層CTA影像隨訪記錄且無再干預或主動脈相關死亡記錄;⑦ 既往曾因Stanford A型夾層行升主動脈或主動脈弓置換術。回顧性收集2016年1月至2023年12月期間在四川大學華西醫院接受TEVAR治療且符合納入排除標準的307例TBAD患者的臨床及影像學資料。患者年齡22~85歲、中位年齡為50歲;男263例(85.7%),女44例(14.3%);外傷性主動脈夾層5例(1.6%),6例患者(2.0%)合并馬凡綜合征。307例患者的具體臨床特征見表1。
1.2 治療
納入研究患者接受的TEVAR治療均在四川大學華西醫院血管外科由同一專家團隊實施。 一般通過穿刺右側股總動脈,置入5F穿刺鞘的方式建立血管入路,后交換為16F或18F穿刺鞘。根據主動脈夾層累及范圍,則可能需穿刺或切開左頸動脈或左肱動脈,置入血管鞘后留置PA35183M導絲于主動脈弓備用。左頸總動脈-左鎖骨下動脈旁路手術可能同期或二期進行,不在此詳述。自一側經GA35183M導絲置入5F黃金標記豬尾導管,確定進入真腔后分別于腎動脈水平腹主動脈、升主動脈造影,進一步評估病情。造影進行近端錨定區定位后交換Lunderquist超硬導絲前進至主動脈瓣成袢,經導絲置入Valiant(Medtronic, Inc. USA)覆膜支架主體輸送系統于預計近端錨定點,釋放主體支架,解鎖近端后釋放金屬裸支架。視患者具體情況,可能行煙囪支架植入、遠端破口栓塞、遠端動脈球囊擴張及支架植入等輔助操作。最后經黃金標記豬尾導管于升主動脈造影,明確是否存在內漏、支架移位等并發癥。術畢,撤出導絲導管,嚴密止血并密切監視病情變化。
1.3 患者資料收集
1.3.1 患者臨床基線資料收集
① 一般資料:包括性別、年齡、身高、體質量、吸煙史、Barthel自理能力評分、入院時收縮壓及舒張壓、外傷史。② 術前合并癥:如高血壓、糖尿病、心律失常、慢性阻塞性肺疾病、慢性腎臟病、卒中病史、馬凡綜合征、冠狀動脈粥樣硬化性心臟病。③ 收集檢驗結果,包括血肌酐及腦鈉肽。
1.3.2 患者影像學資料收集
包括假腔最大直徑、假腔供血小動脈數量、DeBekay分型、初始破口位置及直徑、主動脈弓型及假腔通暢程度。主動脈形態學參數由血管外科具有5年臨床經驗的醫師人工測量CT血管造影平片獲得,為保證數據準確性,由具備10年以上臨床經驗的血管外科副主任醫師及主任醫師隨機抽查20%數據,若測量偏差 >10%,則由該名醫師重新測量并更正。如出現臨界值數據(如術前和術后主動脈最大直徑相差1 mm,處于不良重塑判斷標準邊緣)或2次測得結果偏差較大,則在共同閱片后商議決定。
1.3.3 患者手術資料收集
包括左頸總動脈干預方式、左鎖骨下動脈干預方式、覆膜支架覆蓋長度和近端放大率比例(oversize ratio,OSR)。OSR計算公式為(Ds–Da)/Da×100%,Ds為近端支架的近端口徑,Da為近端錨定區主動脈直徑。
1.4 結局指標定義
結局指標包括臨床及影像學結局事件,通過血管外科門診隨訪、影像學復查與電話隨訪獲得。
1.4.1 臨床結局事件
① 主動脈相關死亡,即術后夾層動脈瘤破裂致死、再干預術后30 d內死亡、其他夾層相關原因(包括支架感染和瘺形成)引起的死亡;② 主動脈事件,包含再干預、夾層動脈瘤破裂和主動脈相關死亡[5]。③ 再干預,即手術指征與首次TEVAR植入支架或主動脈夾層本身有關的二次干預;④ 卒中事件。
1.4.2 影像學結局事件
① 主動脈不良重塑,根據2020年國際指南[6]定義為胸主動脈或腹主動脈參數變化均未能滿足以下3項條件:一為假腔最大直徑縮小,全主動脈直徑無增長;二為真腔最大直徑增加,全主動脈直徑無增長;三為全主動脈直徑縮小、真腔或假腔最大直徑可增加或減小。② Ⅰ A型內漏,即正向血流持續經破口進入假腔的支架近端周圍滲漏;③ Ⅱ型內漏,經由主動脈弓分支、肋間動脈、支氣管動脈等流入假腔的逆向血流;④ 逆撕,即夾層近端累及范圍擴大。
1.5 統計學方法
為減少因2組患者影像信息及手術方式可能的差異而造成的偏倚影響,本研究使用傾向性評分匹配(propensity score matching,PSM)以均衡組間混雜因素,減少其對研究結果的影響,由于2組人數差距較大,設置使用1∶4匹配2組人數。研究采用IBM SPSS 25.0和R 4.3.1軟件對數據進行統計學分析。使用Kolmogorov-Smirnov檢驗對計量資料進行正態性檢驗,服從正態分布者以均數±標準差( ±s)表示,不服從正態分布者以中位數(M)和四分位間距(IQR)表示;分別使用獨立樣本均數比較的t檢驗和秩和檢驗。計數資料使用頻數和百分比表述,統計學檢驗使用成組χ2檢驗或Fisher確切概率法(后簡稱“Fisher法” )。使用單因素非條件logistic回歸檢驗ILVA對Ⅰ A型內漏、Ⅱ型內漏和逆撕的影響,計算比值比(odds ratio,OR)及95%置信區間(95% confidence interval,95%CI)。繪制Kaplan-Meier圖并使用log-rank檢驗分析2組患者在其他結局事件上的統計學差異,計算其風險比(hazard ratio,HR)及95%CI。除非特殊說明,所有檢驗水準為雙側α=0.05。
±s)表示,不服從正態分布者以中位數(M)和四分位間距(IQR)表示;分別使用獨立樣本均數比較的t檢驗和秩和檢驗。計數資料使用頻數和百分比表述,統計學檢驗使用成組χ2檢驗或Fisher確切概率法(后簡稱“Fisher法” )。使用單因素非條件logistic回歸檢驗ILVA對Ⅰ A型內漏、Ⅱ型內漏和逆撕的影響,計算比值比(odds ratio,OR)及95%置信區間(95% confidence interval,95%CI)。繪制Kaplan-Meier圖并使用log-rank檢驗分析2組患者在其他結局事件上的統計學差異,計算其風險比(hazard ratio,HR)及95%CI。除非特殊說明,所有檢驗水準為雙側α=0.05。
2 結果
2.1 納入患者的影像學及手術相關資料
根據本研究的納入及排除標準,本研究共納入TBAD患者307例,其中系ILVA者17例(ILVA組),未合并ILVA者290例(對照組)。由于2組患者的例數差距較大,按1∶4比例采用PSM法匹配2組樣本量后共納入TBAD患者82例,其中ILVA組17例,對照組65例。匹配前后2組患者的影像學及手術情況見表2,由表可知,2組患者在匹配后全部指標比較差異均無統計學意義(P>0.05)。
2.2 2組患者臨床結局事件比較結果
納入本研究患者的隨訪時間1~79個月,中位隨訪時間為37個月。按計劃完成術后3、6及12個月CTA檢查的患者分別為216例(70.4%)、157例(51.1%)和180例(58.6%)。
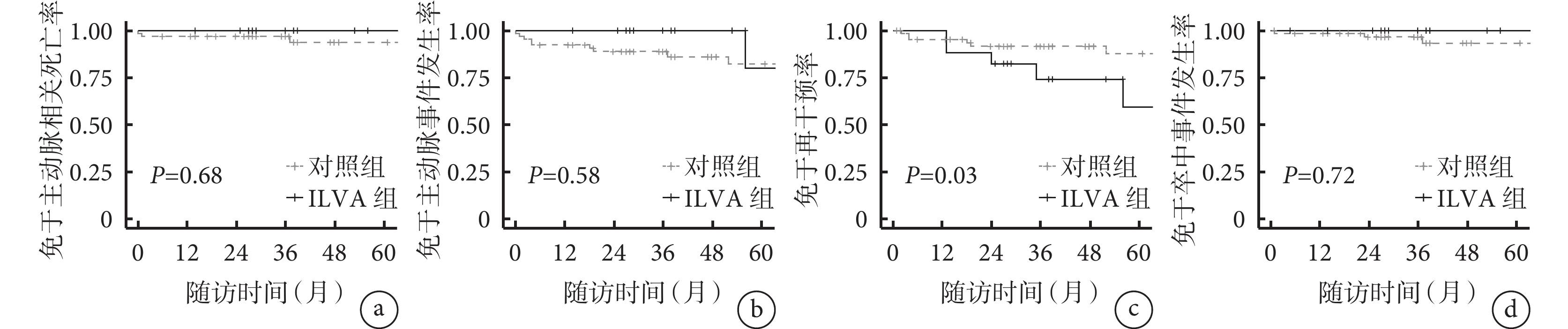
PSM匹配后, 82例患者于隨訪期間共發生6例主動脈相關死亡,5年免于主動脈相關死亡率為95.1% [95%CI為(91.1%,99.1%)];ILVA組與對照組患者的5年免于主動脈相關死亡率比較差異無統計學意義 [HR=0.63,95%CI為(0.07,5.43),β值=–0.460,P=0.68],見圖1a。隨訪期間共發生14例主動脈事件,5年免于主動脈事件發生率為82.9% [95%CI為(72.3%,93.5%)];ILVA組與對照組患者的5年免于主動脈事件發生率相比差異無統計學意義 [HR=0.65,95%CI為(0.14,2.94),β值=–0.429,P=0.58],見圖1b。在再干預方面,13例患者于隨訪期間接受了二次或更多相關手術治療,5年免于再干預率為81.5% [95%CI為(70.7%,92.3%)];與對照組相比,ILVA組患者更多接受了再干預 [HR=2.56,95%CI為(1.55,8.11),β值=0.940,P=0.03],見圖1c。在卒中事件方面,共6例患者發生卒中,5年免于卒中發生率為94.8% [95%CI為(90.7%,98.9%)];ILVA組與對照組的5年免于卒中發生率相比差異無統計學意義 [HR=0.67,95%CI為(0.08,5.76),β值=–0.400,P=0.72],見圖1d。
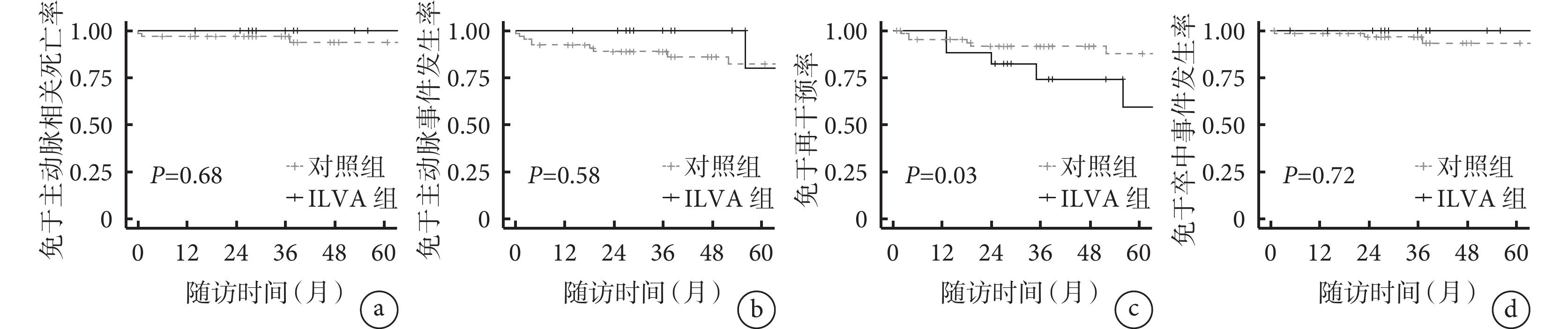 圖1
示ILVA組與對照組患者免于主動脈相關死亡(a)、主動脈事件(b)、免于再干預(c)和卒中事件(d)發生率曲線
圖1
示ILVA組與對照組患者免于主動脈相關死亡(a)、主動脈事件(b)、免于再干預(c)和卒中事件(d)發生率曲線
2.3 2組患者影像學結局事件比較結果
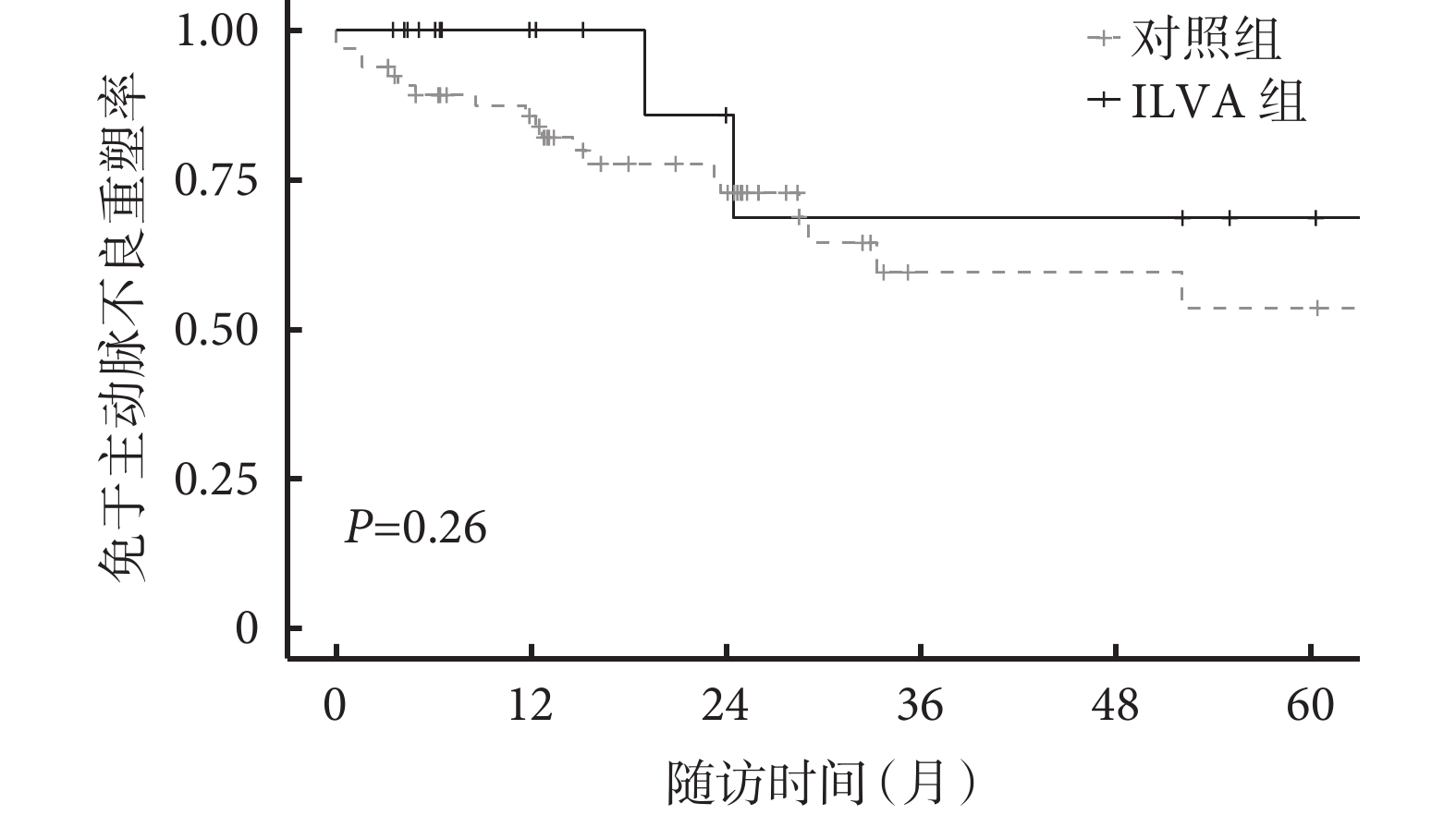
PSM匹配后, 82例患者于隨訪期間共發生23例主動脈不良重塑,5年免于不良重塑率為54.8% [95%CI為(41.5%,74.1%)];ILVA組與對照組患者的5年免于不良重塑率相比差異無統計學意義 [HR=0.43,95%CI為(0.10,1.86),β值=–0.837,P=0.26], 見圖2。 其余結局指標2組間比較結果見表3。由表3可見, ILVA組與對照組患者的Ⅱ 型內漏發生率比較差異有統計學意義(P=0.04),但Ⅰ A型內漏 (P=0.09)和逆撕 (P=0.51)發生率2組間比較差異無統計學意義。
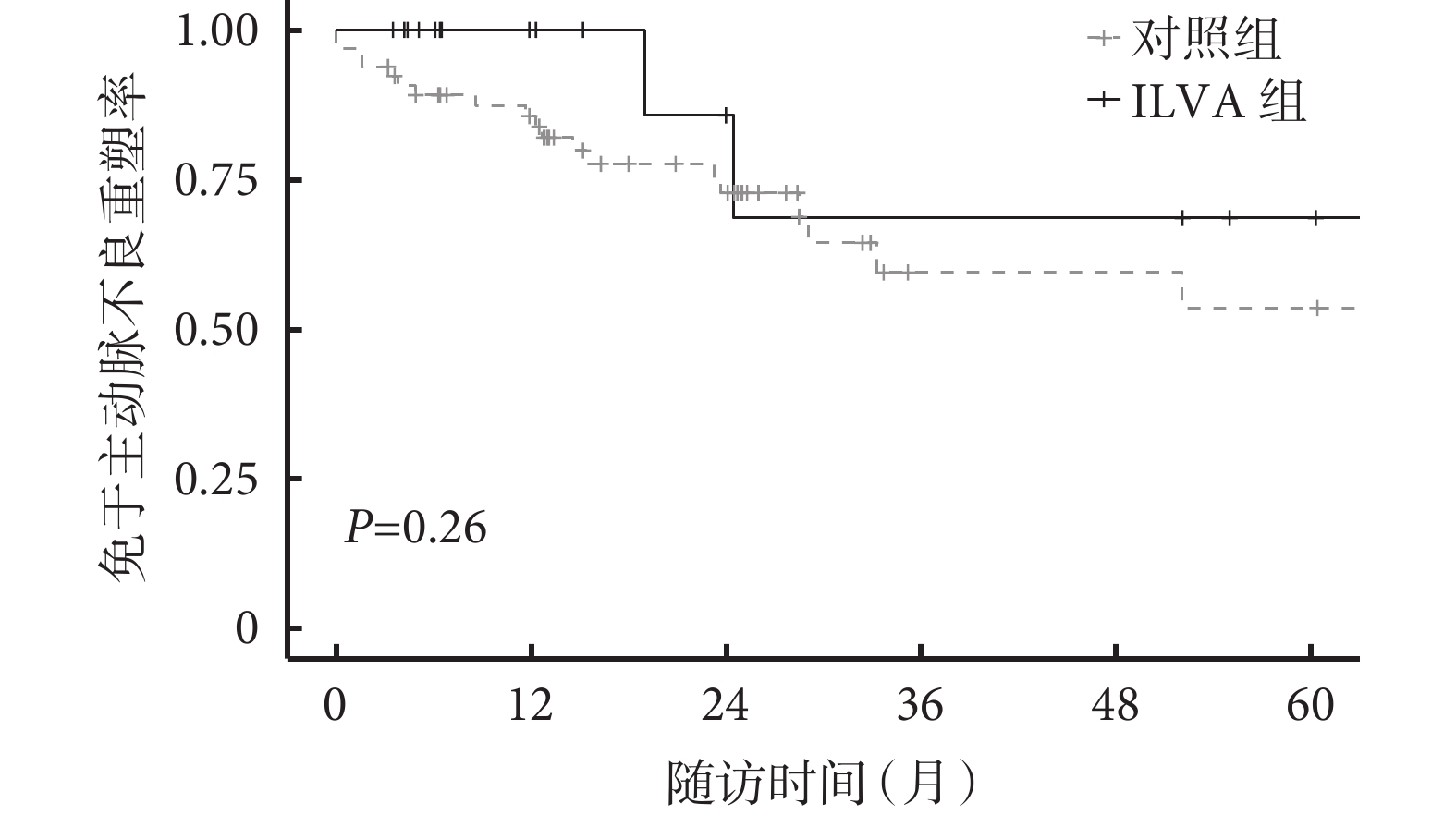 圖2
示ILVA組與對照組患者免于主動脈不良重塑曲線
圖2
示ILVA組與對照組患者免于主動脈不良重塑曲線
3 討論
主動脈弓及其分支存在多種解剖變異,ILVA是其中常見的一種類型,據報道在TBAD患者中的比率可高達5.8%[7-8]。在本研究中,發現合并ILVA的TBAD患者在再干預事件和Ⅱ型內漏發生上較正常主動脈弓患者為多,但在其他臨床或影像學結局事件上沒有統計學差異,這一發現有助于實現臨床對此類患者的個性化治療。本研究中合并ILVA的患者占比為5.5%(17/307),與前述文獻報道結果基本相同,但高于Ding等[3]研究中的3.6%(31/864),推測可能與患者的納入和排除標準等有關。需要注意的是,由于該變異動脈較為纖細,在CT閱片中可能被忽略,導致誤診漏診,因此該比率可能較實際情況為低。
盡管ILVA這一解剖學變異在正常人及TBAD患者中的發生比率接近[9],但已有研究[10]表明ILVA變異可能與主動脈夾層的發生發展有關,和TBAD的發病存在顯著聯系。 從生理角度考慮,ILVA對血流的影響不僅在于其本身,相應的主動脈弓及其他弓部分支的走行、直徑也可能產生變化,導致對血流動力學的影響進一步擴大。Shalhub等[11]的研究也支持這一結論,他們的研究結果表明,在4D Flow MRI掃描結果中,具有牛型主動脈弓、迷走右鎖骨下動脈等主動脈弓部變異的TBAD患者具有與正常主動脈弓的患者不同的血流形式,接受手術干預的比例也更高。
TBAD的治療方面,傳統外科手術治療一般選擇開放手術,該手術創傷大、耗時久,盡管近年來手術方式和圍手術期管理持續進步,但開放手術仍具有相當高的并發癥率及死亡率[12-13]。自1999年首例TEVAR手術開展以來,由于其在短期和中遠期臨床結局方面相對于藥物治療及傳統開放手術的優勢,TEVAR現已成為TBAD的一線治療手段[14-15],體外開窗等技術在治療復雜類型TBAD時也表現出良好療效[16-18]。 相對Stanford A型主動脈夾層而言,TBAD的手術過程中對ILVA的關注相對較少,因為A型夾層患者往往需接受弓部重建,完整重建左椎動脈對于保護大腦血供、預防卒中等嚴重并發癥的發生具有重要意義。相對而言,在目前的TBAD治療的臨床實踐中,ILVA的存在主要影響手術前的決策,如忽略該解剖變異行常規手術,可能在導絲選入主動脈弓部或分支時遭遇困難,若不慎將覆膜支架覆蓋ILVA開口,圍手術期可能造成卒中等嚴重并發癥,遠期來看內漏等支架并發癥的概率也將上升。由于病變本身特點,常規TEVAR操作中,在植入覆膜支架時其多數錨定于左鎖骨下動脈開口處遠端,而ILVA多位于左鎖骨下動脈近端,二者位置并無交集,因此,既往對ILVA進行重建的案例也相對較少,對此的國內外研究也相對缺乏。但需要指出的是,臨床實踐中由于病變位置偏向主動脈近端,導致可能需要干預左鎖骨下動脈并不罕見,如Evangelista等[19]學者就指出,實際上有超過一半(51.3%)的患者,其初始破口位置偏向近端,即靠近左鎖骨下動脈,因此,TBAD患者術前仍然需要準確識別是否合并ILVA并進行合理的手術方案設計。
既往報道合并ILVA的TBAD患者預后的研究,其術式多為開放或雜交手術[20-22],如Zhu等[23]隨訪7例該類型患者發現,其短期結局良好,均未出現院內死亡或神經系統并發癥,在中位隨訪44個月后也僅有1例患者出現遠端主動脈瘤樣擴張。賴前成等[24]研究合并ILVA的Stanford A型主動脈夾層患者的預后情況,20例患者中有1例出現一過性腦功能障礙,遠期有2例患者因主動脈破裂死亡,3例患者接受相關再干預。綜合來看,此類患者預后良好,但需注意的是,由于手術創傷大,術中可能需要體外循環等,并非所有患者均可接受開放或雜交手術,TEVAR仍然是TBAD患者的一線治療選擇,新型分支或開窗支架也為保留ILVA血供提供了新思路[25-27]。Ding等[3]收集31例合并ILVA的TBAD患者信息,在隨訪中(中位隨訪時間33個月),1例患者由于Ⅱ型內漏接受左鎖骨下動脈彈簧圈栓塞,1例患者發生非主動脈相關死亡,無患者出現卒中等其他不良事件。Zhang等[28]對合并ILVA且因弓部病變行TEVAR的67例患者的資料進行分析,發現其早期Ⅰ A型內漏發生率較高(13.4%,9/67);遠期結果來看,5例患者出現再干預,未觀察到死亡事件。
目前,多數相關研究均關注合并ILVA患者的臨床預后情況,然而,目前尚無學者研究此類患者遠期內漏、主動脈不良重塑等影像學結局事件,盡管其理論上出現相關事件的概率更高。同時,相關研究也未使用傾向性分析等統計方法,這將可能導致手術方式和主動脈夾層形態學參數作為混雜因素,影響后續的統計學檢驗結果。本研究也的確發現,2組患者在左頸總動脈的干預方式上存在差異,但采用PSM法對2組患者進行一對多匹配,校正了可能的混雜因素;同時研究多項臨床和影像學結局事件,對患者的綜合預后情況進行隨訪調查。在關注的4項臨床結局指標中,ILVA組患者僅出現再干預情況較對照組為多,其他包括主動脈相關死亡、主動脈事件和卒中在內的結局事件均無明顯差異,與前文引用文獻結果類似。在影像學結局上,ILVA組患者在主動脈不良重塑、Ⅰ A型內漏和逆撕3項不良事件上與正常主動脈弓患者無明顯差異,但出現Ⅱ型內漏的概率高于對照組,這一結果也與既往文獻類似。Zhang等[28]的研究中,開窗支架組和手術轉位組分別有21%和27%的患者在ILVA中發現雙向血流,也從側面揭示了患者需接受再干預的原因。
綜上所述,筆者通過回顧性隊列研究,探究合并ILVA的TBAD患者在接受TEVAR術后的預后情況,就研究結果和既往文獻報道結果來看,TEVAR手術對合并ILVA的患者仍有良好的安全性和有效性,遠期來看該解剖變異并不增加卒中、逆撕、主動脈相關死亡等嚴重不良事件風險,手術效果與正常主動脈弓患者相當。但需注意的是,合并該解剖變異的患者容易發生Ⅱ型內漏,也更容易接受再干預,臨床對該特殊群體有必要進行密切關注,囑其定期進行隨訪復查。本研究也存在一定局限性,由于全部數據來源于單中心,導致樣本量仍偏少,可能無法充分檢驗ILVA與各結局事件的相關性,且由于本身研究性質所限,回顧性隊列研究可能存在失訪偏倚等情況,因此,得出的結論也需要客觀批判看待。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:沈寅知負責文獻檢索、數據計算和撰寫論文;黃斌修訂論文格式及文中圖表,擬定文章重要論點;袁丁參與論文大綱的制定并對最終文稿進行修訂;趙紀春給予指導性意見并對最終文稿的內容進行審閱。
倫理聲明:本研究通過了四川大學華西醫院生物醫學倫理審查委員會的審批,批文編號:2023年審(1664)號。
Stanford B型主動脈夾層(type B aortic dissection,TBAD)由于其高并發癥率和高死亡率的特征[1-2],始終是血管外科領域的研究熱點。單發左側椎動脈(isolated left vertebral artery,ILVA)指生理情況下起自左鎖骨下動脈的左椎動脈直接自主動脈弓發出,據報道在TBAD患者中占比約3.6%[3]。TBAD患者合并ILVA將增加胸主動脈腔內覆膜支架修復術(thoracic endovascular aortic repair,TEVAR)的手術難度,并可能引起卒中等嚴重并發癥[4]。然而,由于ILVA的發生率低,其中罹患TBAD的患者更為少見,目前學界對其與TEVAR術后結局事件的關系不甚明確。因此,本研究基于回顧性隊列研究,分析了行TEVAR手術的TBAD患者的臨床及影像資料,旨在探究合并IVLA對TBAD患者TEVAR術后結局的影響,以利于臨床醫生對該解剖變異的深入理解,個性化制定手術方案。
1 資料與方法
1.1 研究對象
本研究患者納入標準:① 術前經胸腹部計算機體層血管成像(computed tomography angiography,CTA)確診為 Stanford B型主動脈夾層即Debakey Ⅲa/Ⅲb型主動脈夾層,包括近年來新提出的非A非B型夾層;② 接受TEVAR手術,即于胸主動脈接受覆膜支架系統植入;③ 術后至少行1次胸腹部CTA影像隨訪檢查,且該次檢查距手術間隔時間 ≥90 d;④ 入院后臨床數據及術前CTA圖像可查。排除標準:① 孤立性胸主動脈瘤;② 胸主動脈穿通性潰瘍及壁間血腫;③ 累及長度小于2 cm的局限性主動脈夾層;④ 病例信息不完整或術前CTA圖像缺失;⑤ 既往曾于胸主動脈植入覆膜支架;⑥ 術后90 d后無夾層CTA影像隨訪記錄且無再干預或主動脈相關死亡記錄;⑦ 既往曾因Stanford A型夾層行升主動脈或主動脈弓置換術。回顧性收集2016年1月至2023年12月期間在四川大學華西醫院接受TEVAR治療且符合納入排除標準的307例TBAD患者的臨床及影像學資料。患者年齡22~85歲、中位年齡為50歲;男263例(85.7%),女44例(14.3%);外傷性主動脈夾層5例(1.6%),6例患者(2.0%)合并馬凡綜合征。307例患者的具體臨床特征見表1。
1.2 治療
納入研究患者接受的TEVAR治療均在四川大學華西醫院血管外科由同一專家團隊實施。 一般通過穿刺右側股總動脈,置入5F穿刺鞘的方式建立血管入路,后交換為16F或18F穿刺鞘。根據主動脈夾層累及范圍,則可能需穿刺或切開左頸動脈或左肱動脈,置入血管鞘后留置PA35183M導絲于主動脈弓備用。左頸總動脈-左鎖骨下動脈旁路手術可能同期或二期進行,不在此詳述。自一側經GA35183M導絲置入5F黃金標記豬尾導管,確定進入真腔后分別于腎動脈水平腹主動脈、升主動脈造影,進一步評估病情。造影進行近端錨定區定位后交換Lunderquist超硬導絲前進至主動脈瓣成袢,經導絲置入Valiant(Medtronic, Inc. USA)覆膜支架主體輸送系統于預計近端錨定點,釋放主體支架,解鎖近端后釋放金屬裸支架。視患者具體情況,可能行煙囪支架植入、遠端破口栓塞、遠端動脈球囊擴張及支架植入等輔助操作。最后經黃金標記豬尾導管于升主動脈造影,明確是否存在內漏、支架移位等并發癥。術畢,撤出導絲導管,嚴密止血并密切監視病情變化。
1.3 患者資料收集
1.3.1 患者臨床基線資料收集
① 一般資料:包括性別、年齡、身高、體質量、吸煙史、Barthel自理能力評分、入院時收縮壓及舒張壓、外傷史。② 術前合并癥:如高血壓、糖尿病、心律失常、慢性阻塞性肺疾病、慢性腎臟病、卒中病史、馬凡綜合征、冠狀動脈粥樣硬化性心臟病。③ 收集檢驗結果,包括血肌酐及腦鈉肽。
1.3.2 患者影像學資料收集
包括假腔最大直徑、假腔供血小動脈數量、DeBekay分型、初始破口位置及直徑、主動脈弓型及假腔通暢程度。主動脈形態學參數由血管外科具有5年臨床經驗的醫師人工測量CT血管造影平片獲得,為保證數據準確性,由具備10年以上臨床經驗的血管外科副主任醫師及主任醫師隨機抽查20%數據,若測量偏差 >10%,則由該名醫師重新測量并更正。如出現臨界值數據(如術前和術后主動脈最大直徑相差1 mm,處于不良重塑判斷標準邊緣)或2次測得結果偏差較大,則在共同閱片后商議決定。
1.3.3 患者手術資料收集
包括左頸總動脈干預方式、左鎖骨下動脈干預方式、覆膜支架覆蓋長度和近端放大率比例(oversize ratio,OSR)。OSR計算公式為(Ds–Da)/Da×100%,Ds為近端支架的近端口徑,Da為近端錨定區主動脈直徑。
1.4 結局指標定義
結局指標包括臨床及影像學結局事件,通過血管外科門診隨訪、影像學復查與電話隨訪獲得。
1.4.1 臨床結局事件
① 主動脈相關死亡,即術后夾層動脈瘤破裂致死、再干預術后30 d內死亡、其他夾層相關原因(包括支架感染和瘺形成)引起的死亡;② 主動脈事件,包含再干預、夾層動脈瘤破裂和主動脈相關死亡[5]。③ 再干預,即手術指征與首次TEVAR植入支架或主動脈夾層本身有關的二次干預;④ 卒中事件。
1.4.2 影像學結局事件
① 主動脈不良重塑,根據2020年國際指南[6]定義為胸主動脈或腹主動脈參數變化均未能滿足以下3項條件:一為假腔最大直徑縮小,全主動脈直徑無增長;二為真腔最大直徑增加,全主動脈直徑無增長;三為全主動脈直徑縮小、真腔或假腔最大直徑可增加或減小。② Ⅰ A型內漏,即正向血流持續經破口進入假腔的支架近端周圍滲漏;③ Ⅱ型內漏,經由主動脈弓分支、肋間動脈、支氣管動脈等流入假腔的逆向血流;④ 逆撕,即夾層近端累及范圍擴大。
1.5 統計學方法
為減少因2組患者影像信息及手術方式可能的差異而造成的偏倚影響,本研究使用傾向性評分匹配(propensity score matching,PSM)以均衡組間混雜因素,減少其對研究結果的影響,由于2組人數差距較大,設置使用1∶4匹配2組人數。研究采用IBM SPSS 25.0和R 4.3.1軟件對數據進行統計學分析。使用Kolmogorov-Smirnov檢驗對計量資料進行正態性檢驗,服從正態分布者以均數±標準差( ±s)表示,不服從正態分布者以中位數(M)和四分位間距(IQR)表示;分別使用獨立樣本均數比較的t檢驗和秩和檢驗。計數資料使用頻數和百分比表述,統計學檢驗使用成組χ2檢驗或Fisher確切概率法(后簡稱“Fisher法” )。使用單因素非條件logistic回歸檢驗ILVA對Ⅰ A型內漏、Ⅱ型內漏和逆撕的影響,計算比值比(odds ratio,OR)及95%置信區間(95% confidence interval,95%CI)。繪制Kaplan-Meier圖并使用log-rank檢驗分析2組患者在其他結局事件上的統計學差異,計算其風險比(hazard ratio,HR)及95%CI。除非特殊說明,所有檢驗水準為雙側α=0.05。
±s)表示,不服從正態分布者以中位數(M)和四分位間距(IQR)表示;分別使用獨立樣本均數比較的t檢驗和秩和檢驗。計數資料使用頻數和百分比表述,統計學檢驗使用成組χ2檢驗或Fisher確切概率法(后簡稱“Fisher法” )。使用單因素非條件logistic回歸檢驗ILVA對Ⅰ A型內漏、Ⅱ型內漏和逆撕的影響,計算比值比(odds ratio,OR)及95%置信區間(95% confidence interval,95%CI)。繪制Kaplan-Meier圖并使用log-rank檢驗分析2組患者在其他結局事件上的統計學差異,計算其風險比(hazard ratio,HR)及95%CI。除非特殊說明,所有檢驗水準為雙側α=0.05。
2 結果
2.1 納入患者的影像學及手術相關資料
根據本研究的納入及排除標準,本研究共納入TBAD患者307例,其中系ILVA者17例(ILVA組),未合并ILVA者290例(對照組)。由于2組患者的例數差距較大,按1∶4比例采用PSM法匹配2組樣本量后共納入TBAD患者82例,其中ILVA組17例,對照組65例。匹配前后2組患者的影像學及手術情況見表2,由表可知,2組患者在匹配后全部指標比較差異均無統計學意義(P>0.05)。
2.2 2組患者臨床結局事件比較結果
納入本研究患者的隨訪時間1~79個月,中位隨訪時間為37個月。按計劃完成術后3、6及12個月CTA檢查的患者分別為216例(70.4%)、157例(51.1%)和180例(58.6%)。
PSM匹配后, 82例患者于隨訪期間共發生6例主動脈相關死亡,5年免于主動脈相關死亡率為95.1% [95%CI為(91.1%,99.1%)];ILVA組與對照組患者的5年免于主動脈相關死亡率比較差異無統計學意義 [HR=0.63,95%CI為(0.07,5.43),β值=–0.460,P=0.68],見圖1a。隨訪期間共發生14例主動脈事件,5年免于主動脈事件發生率為82.9% [95%CI為(72.3%,93.5%)];ILVA組與對照組患者的5年免于主動脈事件發生率相比差異無統計學意義 [HR=0.65,95%CI為(0.14,2.94),β值=–0.429,P=0.58],見圖1b。在再干預方面,13例患者于隨訪期間接受了二次或更多相關手術治療,5年免于再干預率為81.5% [95%CI為(70.7%,92.3%)];與對照組相比,ILVA組患者更多接受了再干預 [HR=2.56,95%CI為(1.55,8.11),β值=0.940,P=0.03],見圖1c。在卒中事件方面,共6例患者發生卒中,5年免于卒中發生率為94.8% [95%CI為(90.7%,98.9%)];ILVA組與對照組的5年免于卒中發生率相比差異無統計學意義 [HR=0.67,95%CI為(0.08,5.76),β值=–0.400,P=0.72],見圖1d。
 圖1
示ILVA組與對照組患者免于主動脈相關死亡(a)、主動脈事件(b)、免于再干預(c)和卒中事件(d)發生率曲線
圖1
示ILVA組與對照組患者免于主動脈相關死亡(a)、主動脈事件(b)、免于再干預(c)和卒中事件(d)發生率曲線
2.3 2組患者影像學結局事件比較結果
PSM匹配后, 82例患者于隨訪期間共發生23例主動脈不良重塑,5年免于不良重塑率為54.8% [95%CI為(41.5%,74.1%)];ILVA組與對照組患者的5年免于不良重塑率相比差異無統計學意義 [HR=0.43,95%CI為(0.10,1.86),β值=–0.837,P=0.26], 見圖2。 其余結局指標2組間比較結果見表3。由表3可見, ILVA組與對照組患者的Ⅱ 型內漏發生率比較差異有統計學意義(P=0.04),但Ⅰ A型內漏 (P=0.09)和逆撕 (P=0.51)發生率2組間比較差異無統計學意義。
 圖2
示ILVA組與對照組患者免于主動脈不良重塑曲線
圖2
示ILVA組與對照組患者免于主動脈不良重塑曲線
3 討論
主動脈弓及其分支存在多種解剖變異,ILVA是其中常見的一種類型,據報道在TBAD患者中的比率可高達5.8%[7-8]。在本研究中,發現合并ILVA的TBAD患者在再干預事件和Ⅱ型內漏發生上較正常主動脈弓患者為多,但在其他臨床或影像學結局事件上沒有統計學差異,這一發現有助于實現臨床對此類患者的個性化治療。本研究中合并ILVA的患者占比為5.5%(17/307),與前述文獻報道結果基本相同,但高于Ding等[3]研究中的3.6%(31/864),推測可能與患者的納入和排除標準等有關。需要注意的是,由于該變異動脈較為纖細,在CT閱片中可能被忽略,導致誤診漏診,因此該比率可能較實際情況為低。
盡管ILVA這一解剖學變異在正常人及TBAD患者中的發生比率接近[9],但已有研究[10]表明ILVA變異可能與主動脈夾層的發生發展有關,和TBAD的發病存在顯著聯系。 從生理角度考慮,ILVA對血流的影響不僅在于其本身,相應的主動脈弓及其他弓部分支的走行、直徑也可能產生變化,導致對血流動力學的影響進一步擴大。Shalhub等[11]的研究也支持這一結論,他們的研究結果表明,在4D Flow MRI掃描結果中,具有牛型主動脈弓、迷走右鎖骨下動脈等主動脈弓部變異的TBAD患者具有與正常主動脈弓的患者不同的血流形式,接受手術干預的比例也更高。
TBAD的治療方面,傳統外科手術治療一般選擇開放手術,該手術創傷大、耗時久,盡管近年來手術方式和圍手術期管理持續進步,但開放手術仍具有相當高的并發癥率及死亡率[12-13]。自1999年首例TEVAR手術開展以來,由于其在短期和中遠期臨床結局方面相對于藥物治療及傳統開放手術的優勢,TEVAR現已成為TBAD的一線治療手段[14-15],體外開窗等技術在治療復雜類型TBAD時也表現出良好療效[16-18]。 相對Stanford A型主動脈夾層而言,TBAD的手術過程中對ILVA的關注相對較少,因為A型夾層患者往往需接受弓部重建,完整重建左椎動脈對于保護大腦血供、預防卒中等嚴重并發癥的發生具有重要意義。相對而言,在目前的TBAD治療的臨床實踐中,ILVA的存在主要影響手術前的決策,如忽略該解剖變異行常規手術,可能在導絲選入主動脈弓部或分支時遭遇困難,若不慎將覆膜支架覆蓋ILVA開口,圍手術期可能造成卒中等嚴重并發癥,遠期來看內漏等支架并發癥的概率也將上升。由于病變本身特點,常規TEVAR操作中,在植入覆膜支架時其多數錨定于左鎖骨下動脈開口處遠端,而ILVA多位于左鎖骨下動脈近端,二者位置并無交集,因此,既往對ILVA進行重建的案例也相對較少,對此的國內外研究也相對缺乏。但需要指出的是,臨床實踐中由于病變位置偏向主動脈近端,導致可能需要干預左鎖骨下動脈并不罕見,如Evangelista等[19]學者就指出,實際上有超過一半(51.3%)的患者,其初始破口位置偏向近端,即靠近左鎖骨下動脈,因此,TBAD患者術前仍然需要準確識別是否合并ILVA并進行合理的手術方案設計。
既往報道合并ILVA的TBAD患者預后的研究,其術式多為開放或雜交手術[20-22],如Zhu等[23]隨訪7例該類型患者發現,其短期結局良好,均未出現院內死亡或神經系統并發癥,在中位隨訪44個月后也僅有1例患者出現遠端主動脈瘤樣擴張。賴前成等[24]研究合并ILVA的Stanford A型主動脈夾層患者的預后情況,20例患者中有1例出現一過性腦功能障礙,遠期有2例患者因主動脈破裂死亡,3例患者接受相關再干預。綜合來看,此類患者預后良好,但需注意的是,由于手術創傷大,術中可能需要體外循環等,并非所有患者均可接受開放或雜交手術,TEVAR仍然是TBAD患者的一線治療選擇,新型分支或開窗支架也為保留ILVA血供提供了新思路[25-27]。Ding等[3]收集31例合并ILVA的TBAD患者信息,在隨訪中(中位隨訪時間33個月),1例患者由于Ⅱ型內漏接受左鎖骨下動脈彈簧圈栓塞,1例患者發生非主動脈相關死亡,無患者出現卒中等其他不良事件。Zhang等[28]對合并ILVA且因弓部病變行TEVAR的67例患者的資料進行分析,發現其早期Ⅰ A型內漏發生率較高(13.4%,9/67);遠期結果來看,5例患者出現再干預,未觀察到死亡事件。
目前,多數相關研究均關注合并ILVA患者的臨床預后情況,然而,目前尚無學者研究此類患者遠期內漏、主動脈不良重塑等影像學結局事件,盡管其理論上出現相關事件的概率更高。同時,相關研究也未使用傾向性分析等統計方法,這將可能導致手術方式和主動脈夾層形態學參數作為混雜因素,影響后續的統計學檢驗結果。本研究也的確發現,2組患者在左頸總動脈的干預方式上存在差異,但采用PSM法對2組患者進行一對多匹配,校正了可能的混雜因素;同時研究多項臨床和影像學結局事件,對患者的綜合預后情況進行隨訪調查。在關注的4項臨床結局指標中,ILVA組患者僅出現再干預情況較對照組為多,其他包括主動脈相關死亡、主動脈事件和卒中在內的結局事件均無明顯差異,與前文引用文獻結果類似。在影像學結局上,ILVA組患者在主動脈不良重塑、Ⅰ A型內漏和逆撕3項不良事件上與正常主動脈弓患者無明顯差異,但出現Ⅱ型內漏的概率高于對照組,這一結果也與既往文獻類似。Zhang等[28]的研究中,開窗支架組和手術轉位組分別有21%和27%的患者在ILVA中發現雙向血流,也從側面揭示了患者需接受再干預的原因。
綜上所述,筆者通過回顧性隊列研究,探究合并ILVA的TBAD患者在接受TEVAR術后的預后情況,就研究結果和既往文獻報道結果來看,TEVAR手術對合并ILVA的患者仍有良好的安全性和有效性,遠期來看該解剖變異并不增加卒中、逆撕、主動脈相關死亡等嚴重不良事件風險,手術效果與正常主動脈弓患者相當。但需注意的是,合并該解剖變異的患者容易發生Ⅱ型內漏,也更容易接受再干預,臨床對該特殊群體有必要進行密切關注,囑其定期進行隨訪復查。本研究也存在一定局限性,由于全部數據來源于單中心,導致樣本量仍偏少,可能無法充分檢驗ILVA與各結局事件的相關性,且由于本身研究性質所限,回顧性隊列研究可能存在失訪偏倚等情況,因此,得出的結論也需要客觀批判看待。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:沈寅知負責文獻檢索、數據計算和撰寫論文;黃斌修訂論文格式及文中圖表,擬定文章重要論點;袁丁參與論文大綱的制定并對最終文稿進行修訂;趙紀春給予指導性意見并對最終文稿的內容進行審閱。
倫理聲明:本研究通過了四川大學華西醫院生物醫學倫理審查委員會的審批,批文編號:2023年審(1664)號。