引用本文: 宋心月, 徐文靜, 段昊玙, 梁斌苗. 成人超重和肥胖患者體重指數與肺功能的關系. 中國呼吸與危重監護雜志, 2024, 23(11): 802-806. doi: 10.7507/1671-6205.202404019 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
肥胖的發生率在全球呈上升趨勢[1]。據《中國居民營養與慢性病狀況報告(2020年)》指出,我國成年居民超重或肥胖人數占比已經超過一半,肥胖已成為我國最嚴重的公共衛生問題之一[2]。研究表明肥胖可導致機體各個系統出現慢性生理損傷,是哮喘等呼吸系統疾病發病的危險因素[3]。肥胖可以通過多種機制損傷呼吸系統,導致肺功能降低,出現限制性通氣功能障礙和呼吸調節功能失調等問題[4-6]。目前關于肥胖影響肺功能的主流假說有力學機制和炎癥途徑兩類,其確切機制尚未明確[7]。體重指數(body mass index,BMI)通常用于對肥胖的診斷,并可用于粗略判斷機體的營養狀況。根據BMI數值可以定義超重和肥胖:BMI≥25 kg/m2時診斷為超重,BMI≥30 kg/m2時可診斷為肥胖[8-9];在肥胖范圍內可按照世界衛生組織(World Health Organization,WHO)肥胖分級對BMI再次分級:30 kg/m2≤BMI<35 kg/m2為Ⅰ級肥胖,35 kg/m2≤BMI<40 kg/m2為Ⅱ級肥胖,BMI≥40 kg/m2為Ⅲ級肥胖,又稱極度肥胖。超重和肥胖患者BMI與肺功能是否存在相關關系,以及BMI增加時患者彌散功能如何變化,國外此類研究結果尚未統一。有學者認為隨著BMI增加患者肺一氧化碳彌散量占預計值百分比(DLCO%pred)也隨之增加[10-13],另一些學者則認為隨著BMI增加患者DLCO%pred不變或降低[13-15]。此外,關注極度肥胖患者彌散功能的研究較少。本研究通過對390例超重和肥胖患者的一般資料和基礎肺功能結果進行分析,以了解它們之間的相互關系,并試圖分析極度肥胖患者彌散功能的改變。
1 資料與方法
1.1 一般資料
回顧性收集2021年1月—2023年12月間到我院進行了全套肺功能測定的390例成年超重和肥胖患者的一般資料和肺功能數據。其中男147例,女243例,平均年齡(32.28±9.13)歲。
1.2 方法
1.2.1 收集資料和分組
記錄患者的年齡、性別、身高、體重、吸煙史、職業,并計算BMI。根據BMI數值可以定義超重和肥胖:BMI≥25 kg/m2時診斷為超重,BMI≥30 kg/m2時可診斷為肥胖[9-10];在肥胖范圍內可按照WHO肥胖分級對BMI再次分級:30 kg/m2≤BMI<35kg/m2為Ⅰ級肥胖,35 kg/m2≤BMI<40 kg/m2為Ⅱ級肥胖,BMI≥ 40 kg/m2為Ⅲ級肥胖,又稱極度肥胖。并據此將患者分為4組:超重組、Ⅰ級肥胖組、Ⅱ級肥胖組和Ⅲ級肥胖組。職業劃分為三類,第一類是非體力勞動為主職業,包括職員、企業管理人員、專業技術人員、教師、公務員;第二類是體力勞動為主職業,包括個體經營者、工人、自由職業者、農民;第三類是其他,包括在校學生、待業、離退休人員。
1.2.2 肺功能測定
在本院肺功能室進行肺功能測定。每日在測試開始前對肺功能測試儀器(Jaeger Corp,Germany)進行校準檢查。由專人進行肺功能檢測,并根據美國胸科協會/歐洲呼吸協會的質量標準[16]和中國肺活量測定指南推薦的參考方程[17]指導測試和確定預計值。測定每位患者的最大呼氣流量—容積曲線,連續測定3次,取最佳值為基礎值;使用單次呼吸法測定彌散能力;使用體積描記法測定肺容量。記錄肺功能指標,包括用力肺活量(forced vital capacity,FVC)、第1秒用力呼氣容積(forced expiratory volume in the first second,FEV1)、FEV1/FVC、最大呼氣流量(peak expiratory flow,PEF)、最大呼氣中段流量(maximal mid-expiratory flow,MMEF)、深吸氣量(inspiratory capacity,IC)、肺活量(vital capacity,VC)和肺總量(total lung capacity,TLC)、肺一氧化碳彌散量(diffusion capacity of carbon monoxide of lung,DLCO)等。除FEV1/FVC用實測值表示外,其余數值均以實測值/預計值的百分比(as a percentage of predicted value,%pred)表示。
1.3 統計學方法
使用SPSS20.0軟件進行統計學分析。呈正態分布的定量資料以均數±標準差(x±s)表示。采用方差分析或Wilcoxon配對符號秩檢驗比較根據BMI不同分組間患者的肺功能指標。BMI與肺功能參數之間的關系分析用Spearman或Pearson相關性判定法,并使用簡單線性回歸或分段線性回歸進行相關性分析。P<0.05為差異有統計學意義。
2 結果
2.1 患者一般情況
390例患者中,超重組37例,Ⅰ級肥胖組106例,Ⅱ級肥胖組110例,Ⅲ級肥胖組137例。不同BMI分組在超重和肥胖患者中年齡、性別和吸煙史的差異有統計學意義(P<0.05)。結果見表1。
2.2 根據BMI值分組后超重和肥胖患者的基礎肺功能測定
四組患者的基礎肺功能測定結果見表2。Ⅲ級肥胖組FVC%pred、TLC%pred、VC%pred、FEV1%pred、PEF%pred低于超重組、Ⅰ級肥胖組(P<0.05),超重組IC%pred值高于Ⅰ級肥胖組、Ⅱ級肥胖組和Ⅲ級肥胖組(P<0.05),Ⅱ級肥胖組DLCO%pred高于超重組和Ⅰ級肥胖組(P<0.05),FEV1/FVC、MMEF%pred在四組之間沒有明顯差異。
2.3 BMI與TLC%pred、VC%pred、DLCO SB%pred之間的關系
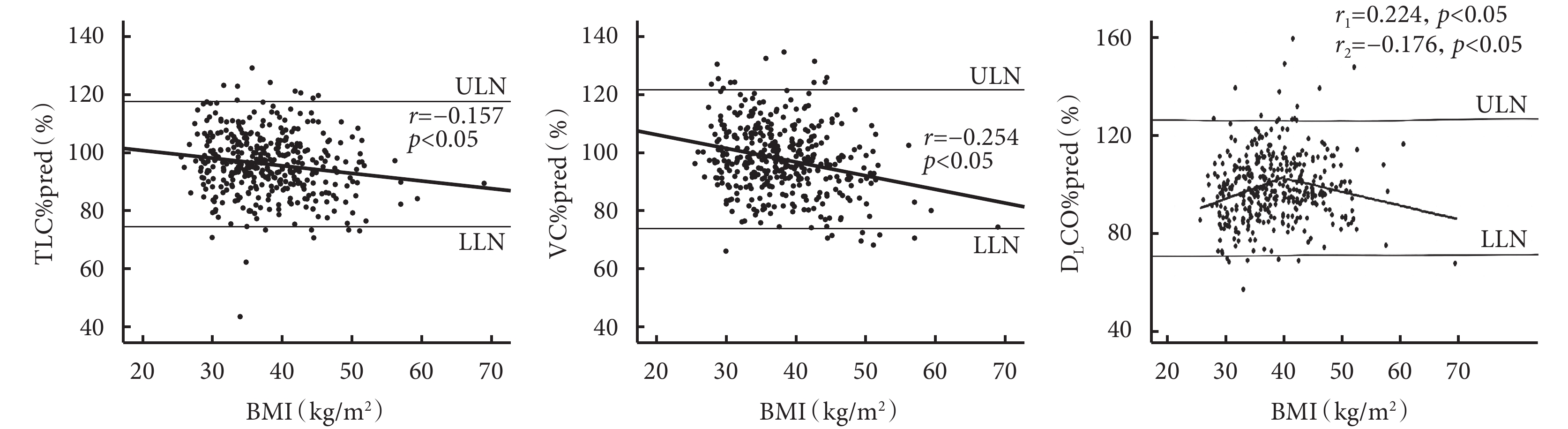
圖1中上下水平實線分別為TLC%pred、VC%pred和DLCO %pred的平均正常上限值和正常下限值(正常上限值為均值與兩倍標準差之和,正常下限值為均值與兩倍標準差之差)。簡單線性回歸分析顯示TLC%pred(r=–0.157,P<0.05)、VC%pred(r=–0.254,P<0.05)與BMI呈負相關。分段線性回歸分析顯示,BMI<40 kg/m2時,DLCO %pred(r1=0.224,P<0.05)與BMI呈正相關;BMI≥40 kg/m2時,DLCO %pred(r2=–0.176,P<0.05)與BMI呈負相關。結果見圖1。
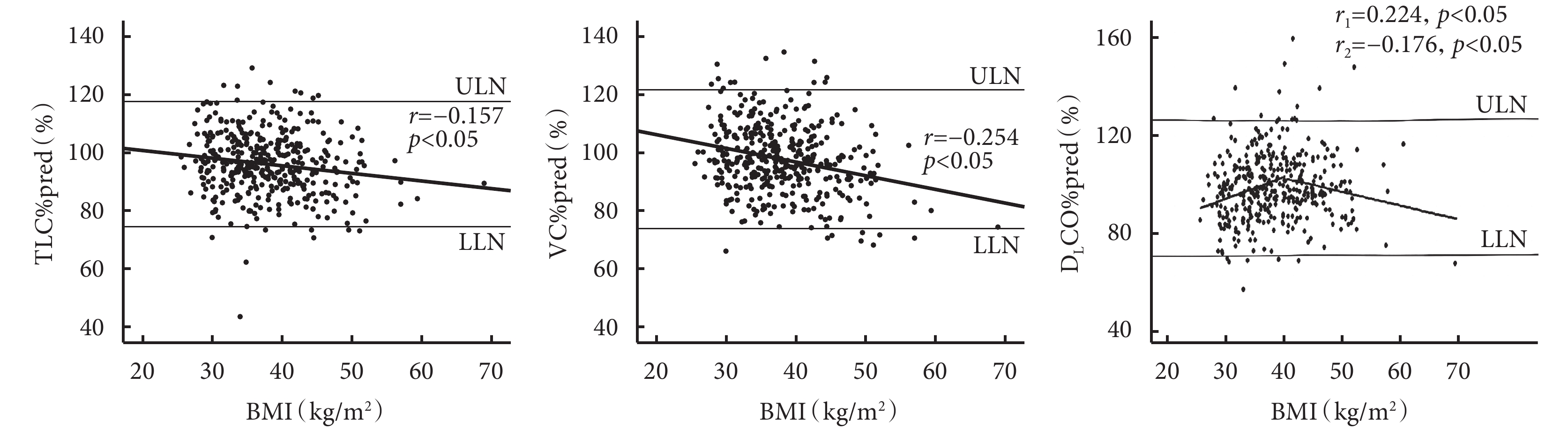 圖1
BMI與TLC%pred、VC%pred、DLCO%pred之間的關系
圖1
BMI與TLC%pred、VC%pred、DLCO%pred之間的關系
TLC%pred、VC%pred與BMI呈負相關。BMI<40 kg/m2時,DLCO%pred與BMI呈正相關;BMI≥40 kg/m2時,DLCO%pred與BMI呈負相關。
3 討論
本研究通過分析我院390例成人超重與肥胖患者BMI與肺功能參數之間的關系,發現超重和肥胖患者BMI增加時,FVC%pred、TLC%pred、VC%pred下降,伴隨FEV1%pred、PEF%pred和IC%pred下降,主要表現為限制性通氣功能障礙。同時,本研究通過BMI與DLCO%pred的分段線性回歸分析,發現BMI=40 kg/m2可以作為BMI與DLCO%pred變化趨勢的截點。即BMI<40 kg/m2時,DLCO%pred隨BMI增加而增加;BMI≥40 kg/m2時,DLCO%pred隨BMI增加而降低。
Jones等[11]對373例呼吸功能正常、BMI分布范圍廣的患者的肺功能結果進行研究,發現25 kg/m2≤BMI<30 kg/m2組的VC%pred高于30 kg/m2≤BMI<35 kg/m2組、35 kg/m2≤BMI<40 kg/m2組和BMI≥40 kg/m2組,25 kg/m2≤BMI<30 kg/m2組的TLC%pred高于35 kg/m2≤BMI<40 kg/m2組和BMI≥40 kg/m2組,且BMI與VC%pred和TLC%pred存在較明顯的負相關關系(r=–0.48和r=–0.50,P<0.000 1)。徐春燕等[18]對60例受試者(中心性肥胖組30例,正常體重組30例)的肺功能結果進行分析,發現中心性肥胖組較正常體重組FVC、TLC明顯下降(P<0.05)。王金祥等[19]對94例非吸煙受試者(正常體重組22例、超重組24例、中度肥胖組48例)進行肺功能的研究,結果顯示中度肥胖組FVC%pred、TLC%pred比正常體重組的相應指標顯著降低(P<0.05)。這與本研究結果相一致。可能原因是超重和肥胖患者脂肪的分布限制了胸廓的擴張和收縮,增加呼吸肌負荷和呼吸驅動,從而影響了呼吸肌的正常運動[20]。由于脂肪的堆積作用,肺容積減少,特別是呼氣末期肺容積功能殘氣量(functional residual capacity,FRC)減少,進而影響了通氣功能。同時,脂肪浸潤使得炎癥因子活躍,導致慢性炎癥和纖維化,肺組織順應性受到影響,進一步加重了限制性通氣功能障礙[21-22]。此外,Boriek等[23]對48名慢性阻塞性肺疾病(簡稱慢阻肺)患者和29名不伴慢阻肺且非吸煙者進行研究,通過接受肺容積從FRC到TLC范圍內的胸部計算機斷層掃描并計算左側橫膈膜中胸部區域的最大主曲率(Rmax),發現膈肌的最大曲率半徑在慢阻肺和非慢阻肺受試者中均隨BMI增加而增加。按照拉普拉斯定律的假設,肥胖受試者的Rmax越大,其肌肉將興奮轉化為收縮的能力就越低,從而使得呼吸功增加。Pelosi等[24]研究表明肥胖者基線腹內壓(>9~15 mm Hg)(1 mm Hg=0.133 kPa)的增加顯著影響胸壁的機械性能,從而增加呼吸功。本研究中的超重和肥胖患者BMI增加時限制性通氣功能障礙伴IC%pred減少,考慮可能原因為肥胖患者腹內壓增高,胸廓上抬,出現限制性功能障礙;同時,膈肌的最大曲率半徑增加,導致膈肌將呼吸中樞發出、沿膈神經傳導的興奮轉化為收縮的能力減弱,膈肌的活動度也受限,因此超重和肥胖患者有效呼吸做功減少,故肺功能表現為限制性通氣功能障礙和IC%pred減少。
超重和肥胖患者受脂肪分布限制胸廓運動和炎癥因子的影響,出現限制性通氣功能障礙,肺功能表現為FVC%pred、VC%pred、TLC%pred、IC%pred下降,基礎肺容量降低。受此影響,超重和肥胖患者的彌散能力也隨之降低。Enache等[14]對98例成人肥胖組和48例正常對照組進行BMI、腰圍、肺活量和DLCO%pred測定,發現肥胖患者平均DLCO%pred、平均肺泡通氣量(alveolar ventilation,VA)%pred略低于對照組,平均滲透性因子(kCO,Krogh因子)高于對照組,其解釋為研究中的肥胖患者基礎肺容量較低,彌散能力也較低,同時肥胖相關的疾病也可能導致彌散受限。例如肺泡-毛細血管屏障受損,2型糖尿病導致肺泡微血管儲備和肺容量的減少等。Chance等[15]針對69例2型糖尿病組(BMI<30 kg/m2者32例、BMI≥30 kg/m2者37例)和45例正常對照組進行研究,發現肥胖患者DLCO%pred低于對照組。可能原因是2型糖尿病患者肺泡壁內結締組織沉積,這一實質改變使肺泡毛細血管募集功能受損,而肥胖相關的脂肪浸潤、脂質沉積等放大了這一因素的影響,進而影響彌散功能。本研究中BMI≥40 kg/m2時,患者DLCO%pred隨BMI增加而下降,可能原因是極度肥胖時肺泡組織受脂肪浸潤或結締組織沉積導致的擴散障礙,或肥胖相關的其他疾病導致的彌散受限[25]。
然而,本研究顯示BMI<40 kg/m2時,DLCO%pred隨BMI增加而增加,可能原因是超重和肥胖患者總循環血量增加,肺血容量增高,肺毛細血管床募集增多,彌散量也隨之增加[22]。國外也有學者認為肥胖患者彌散功能隨肥胖程度增加而增加。Saydain等[10]對高DLCO組(即>140%的預測值)和正常DLCO組(即85%~115%的預測值)各245例的一般信息、肺功能數據、臨床診斷進行分析,發現高DLCO與更大的BMI值和肥胖等診斷相關。Jones等[11]研究發現BMI增加時DLCO%pred有輕度升高(r=0.31,P<0.000 1)。Ray等[12]對43名非吸煙肥胖患者的肺功能數據進行分析,發現體重/身高比為0.6~1.2 kg/cm的范圍內,DLCO%pred隨著肥胖程度的增加而增加。這與我們的結果部分一致。肺彌散功能檢查指南中也提到,肥胖、世居高原、平臥體位、早期的紅細胞增多癥等均屬于能使正常情況下很少開放的肺毛細血管開放的生理或病理狀態,其肺毛細血管流量增加,彌散量增加[13]。
本研究存在一些不足。其一,該研究為回顧性、單中心研究,納入的患者較多為女性(62.3%),在男性群體中結果的外推性還需考慮。未來的研究需要更多大樣本、多中心的前瞻性研究或隨機對照試驗。其二,除常規肺功能檢測外,還可以考慮使用脈沖震蕩等更為先進的技術來進行測試,以明確肥胖對呼吸系統的影響,探索可能的病理生理學機制。
本研究的亮點在于,樣本肥胖分級基于2000年WHO西太平洋地區亞洲成人體重分級建議,并結合了2002年亞太地區WHO專家顧問組針對亞太地區人群的體質及與肥胖有關疾病的建議,較為細化。可以識別不同肥胖程度下患者的肺功能特征和表現,為個性化治療、風險預測和研究結果的可比性提供更有力的支持。此外,本研究關注到極度肥胖時的彌散功能改變這一研究較少的問題,并就目前存在爭議的BMI與DLCO的關系,提出了以BMI=40 kg/m2為截點的分段線性回歸關系圖,并解釋了彌散隨BMI變化可能的病理生理學機制,有賴于更多的研究做進一步的討論和論證。
綜上所述,本研究結果表明DLCO%pred隨BMI的增加表現為雙向變化,存在變化截點。當BMI<40 kg/m2時,DLCO %pred與BMI存在正相關關系,可能原因是超重和肥胖患者總循環血量增加使得肺血容量增高,從而增大了肺毛細血管床的募集,提高了彌散量;當BMI≥40 kg/m2時,DLCO %pred與BMI則存在負相關關系,可能原因是極度肥胖時肺泡組織受脂肪浸潤或結締組織沉積,從而導致氣體擴散能力受限,降低了彌散量,或者考慮肥胖相關的其他疾病導致的彌散受限。
利益沖突:本研究不涉及任何利益沖突。
肥胖的發生率在全球呈上升趨勢[1]。據《中國居民營養與慢性病狀況報告(2020年)》指出,我國成年居民超重或肥胖人數占比已經超過一半,肥胖已成為我國最嚴重的公共衛生問題之一[2]。研究表明肥胖可導致機體各個系統出現慢性生理損傷,是哮喘等呼吸系統疾病發病的危險因素[3]。肥胖可以通過多種機制損傷呼吸系統,導致肺功能降低,出現限制性通氣功能障礙和呼吸調節功能失調等問題[4-6]。目前關于肥胖影響肺功能的主流假說有力學機制和炎癥途徑兩類,其確切機制尚未明確[7]。體重指數(body mass index,BMI)通常用于對肥胖的診斷,并可用于粗略判斷機體的營養狀況。根據BMI數值可以定義超重和肥胖:BMI≥25 kg/m2時診斷為超重,BMI≥30 kg/m2時可診斷為肥胖[8-9];在肥胖范圍內可按照世界衛生組織(World Health Organization,WHO)肥胖分級對BMI再次分級:30 kg/m2≤BMI<35 kg/m2為Ⅰ級肥胖,35 kg/m2≤BMI<40 kg/m2為Ⅱ級肥胖,BMI≥40 kg/m2為Ⅲ級肥胖,又稱極度肥胖。超重和肥胖患者BMI與肺功能是否存在相關關系,以及BMI增加時患者彌散功能如何變化,國外此類研究結果尚未統一。有學者認為隨著BMI增加患者肺一氧化碳彌散量占預計值百分比(DLCO%pred)也隨之增加[10-13],另一些學者則認為隨著BMI增加患者DLCO%pred不變或降低[13-15]。此外,關注極度肥胖患者彌散功能的研究較少。本研究通過對390例超重和肥胖患者的一般資料和基礎肺功能結果進行分析,以了解它們之間的相互關系,并試圖分析極度肥胖患者彌散功能的改變。
1 資料與方法
1.1 一般資料
回顧性收集2021年1月—2023年12月間到我院進行了全套肺功能測定的390例成年超重和肥胖患者的一般資料和肺功能數據。其中男147例,女243例,平均年齡(32.28±9.13)歲。
1.2 方法
1.2.1 收集資料和分組
記錄患者的年齡、性別、身高、體重、吸煙史、職業,并計算BMI。根據BMI數值可以定義超重和肥胖:BMI≥25 kg/m2時診斷為超重,BMI≥30 kg/m2時可診斷為肥胖[9-10];在肥胖范圍內可按照WHO肥胖分級對BMI再次分級:30 kg/m2≤BMI<35kg/m2為Ⅰ級肥胖,35 kg/m2≤BMI<40 kg/m2為Ⅱ級肥胖,BMI≥ 40 kg/m2為Ⅲ級肥胖,又稱極度肥胖。并據此將患者分為4組:超重組、Ⅰ級肥胖組、Ⅱ級肥胖組和Ⅲ級肥胖組。職業劃分為三類,第一類是非體力勞動為主職業,包括職員、企業管理人員、專業技術人員、教師、公務員;第二類是體力勞動為主職業,包括個體經營者、工人、自由職業者、農民;第三類是其他,包括在校學生、待業、離退休人員。
1.2.2 肺功能測定
在本院肺功能室進行肺功能測定。每日在測試開始前對肺功能測試儀器(Jaeger Corp,Germany)進行校準檢查。由專人進行肺功能檢測,并根據美國胸科協會/歐洲呼吸協會的質量標準[16]和中國肺活量測定指南推薦的參考方程[17]指導測試和確定預計值。測定每位患者的最大呼氣流量—容積曲線,連續測定3次,取最佳值為基礎值;使用單次呼吸法測定彌散能力;使用體積描記法測定肺容量。記錄肺功能指標,包括用力肺活量(forced vital capacity,FVC)、第1秒用力呼氣容積(forced expiratory volume in the first second,FEV1)、FEV1/FVC、最大呼氣流量(peak expiratory flow,PEF)、最大呼氣中段流量(maximal mid-expiratory flow,MMEF)、深吸氣量(inspiratory capacity,IC)、肺活量(vital capacity,VC)和肺總量(total lung capacity,TLC)、肺一氧化碳彌散量(diffusion capacity of carbon monoxide of lung,DLCO)等。除FEV1/FVC用實測值表示外,其余數值均以實測值/預計值的百分比(as a percentage of predicted value,%pred)表示。
1.3 統計學方法
使用SPSS20.0軟件進行統計學分析。呈正態分布的定量資料以均數±標準差(x±s)表示。采用方差分析或Wilcoxon配對符號秩檢驗比較根據BMI不同分組間患者的肺功能指標。BMI與肺功能參數之間的關系分析用Spearman或Pearson相關性判定法,并使用簡單線性回歸或分段線性回歸進行相關性分析。P<0.05為差異有統計學意義。
2 結果
2.1 患者一般情況
390例患者中,超重組37例,Ⅰ級肥胖組106例,Ⅱ級肥胖組110例,Ⅲ級肥胖組137例。不同BMI分組在超重和肥胖患者中年齡、性別和吸煙史的差異有統計學意義(P<0.05)。結果見表1。
2.2 根據BMI值分組后超重和肥胖患者的基礎肺功能測定
四組患者的基礎肺功能測定結果見表2。Ⅲ級肥胖組FVC%pred、TLC%pred、VC%pred、FEV1%pred、PEF%pred低于超重組、Ⅰ級肥胖組(P<0.05),超重組IC%pred值高于Ⅰ級肥胖組、Ⅱ級肥胖組和Ⅲ級肥胖組(P<0.05),Ⅱ級肥胖組DLCO%pred高于超重組和Ⅰ級肥胖組(P<0.05),FEV1/FVC、MMEF%pred在四組之間沒有明顯差異。
2.3 BMI與TLC%pred、VC%pred、DLCO SB%pred之間的關系
圖1中上下水平實線分別為TLC%pred、VC%pred和DLCO %pred的平均正常上限值和正常下限值(正常上限值為均值與兩倍標準差之和,正常下限值為均值與兩倍標準差之差)。簡單線性回歸分析顯示TLC%pred(r=–0.157,P<0.05)、VC%pred(r=–0.254,P<0.05)與BMI呈負相關。分段線性回歸分析顯示,BMI<40 kg/m2時,DLCO %pred(r1=0.224,P<0.05)與BMI呈正相關;BMI≥40 kg/m2時,DLCO %pred(r2=–0.176,P<0.05)與BMI呈負相關。結果見圖1。
 圖1
BMI與TLC%pred、VC%pred、DLCO%pred之間的關系
圖1
BMI與TLC%pred、VC%pred、DLCO%pred之間的關系
TLC%pred、VC%pred與BMI呈負相關。BMI<40 kg/m2時,DLCO%pred與BMI呈正相關;BMI≥40 kg/m2時,DLCO%pred與BMI呈負相關。
3 討論
本研究通過分析我院390例成人超重與肥胖患者BMI與肺功能參數之間的關系,發現超重和肥胖患者BMI增加時,FVC%pred、TLC%pred、VC%pred下降,伴隨FEV1%pred、PEF%pred和IC%pred下降,主要表現為限制性通氣功能障礙。同時,本研究通過BMI與DLCO%pred的分段線性回歸分析,發現BMI=40 kg/m2可以作為BMI與DLCO%pred變化趨勢的截點。即BMI<40 kg/m2時,DLCO%pred隨BMI增加而增加;BMI≥40 kg/m2時,DLCO%pred隨BMI增加而降低。
Jones等[11]對373例呼吸功能正常、BMI分布范圍廣的患者的肺功能結果進行研究,發現25 kg/m2≤BMI<30 kg/m2組的VC%pred高于30 kg/m2≤BMI<35 kg/m2組、35 kg/m2≤BMI<40 kg/m2組和BMI≥40 kg/m2組,25 kg/m2≤BMI<30 kg/m2組的TLC%pred高于35 kg/m2≤BMI<40 kg/m2組和BMI≥40 kg/m2組,且BMI與VC%pred和TLC%pred存在較明顯的負相關關系(r=–0.48和r=–0.50,P<0.000 1)。徐春燕等[18]對60例受試者(中心性肥胖組30例,正常體重組30例)的肺功能結果進行分析,發現中心性肥胖組較正常體重組FVC、TLC明顯下降(P<0.05)。王金祥等[19]對94例非吸煙受試者(正常體重組22例、超重組24例、中度肥胖組48例)進行肺功能的研究,結果顯示中度肥胖組FVC%pred、TLC%pred比正常體重組的相應指標顯著降低(P<0.05)。這與本研究結果相一致。可能原因是超重和肥胖患者脂肪的分布限制了胸廓的擴張和收縮,增加呼吸肌負荷和呼吸驅動,從而影響了呼吸肌的正常運動[20]。由于脂肪的堆積作用,肺容積減少,特別是呼氣末期肺容積功能殘氣量(functional residual capacity,FRC)減少,進而影響了通氣功能。同時,脂肪浸潤使得炎癥因子活躍,導致慢性炎癥和纖維化,肺組織順應性受到影響,進一步加重了限制性通氣功能障礙[21-22]。此外,Boriek等[23]對48名慢性阻塞性肺疾病(簡稱慢阻肺)患者和29名不伴慢阻肺且非吸煙者進行研究,通過接受肺容積從FRC到TLC范圍內的胸部計算機斷層掃描并計算左側橫膈膜中胸部區域的最大主曲率(Rmax),發現膈肌的最大曲率半徑在慢阻肺和非慢阻肺受試者中均隨BMI增加而增加。按照拉普拉斯定律的假設,肥胖受試者的Rmax越大,其肌肉將興奮轉化為收縮的能力就越低,從而使得呼吸功增加。Pelosi等[24]研究表明肥胖者基線腹內壓(>9~15 mm Hg)(1 mm Hg=0.133 kPa)的增加顯著影響胸壁的機械性能,從而增加呼吸功。本研究中的超重和肥胖患者BMI增加時限制性通氣功能障礙伴IC%pred減少,考慮可能原因為肥胖患者腹內壓增高,胸廓上抬,出現限制性功能障礙;同時,膈肌的最大曲率半徑增加,導致膈肌將呼吸中樞發出、沿膈神經傳導的興奮轉化為收縮的能力減弱,膈肌的活動度也受限,因此超重和肥胖患者有效呼吸做功減少,故肺功能表現為限制性通氣功能障礙和IC%pred減少。
超重和肥胖患者受脂肪分布限制胸廓運動和炎癥因子的影響,出現限制性通氣功能障礙,肺功能表現為FVC%pred、VC%pred、TLC%pred、IC%pred下降,基礎肺容量降低。受此影響,超重和肥胖患者的彌散能力也隨之降低。Enache等[14]對98例成人肥胖組和48例正常對照組進行BMI、腰圍、肺活量和DLCO%pred測定,發現肥胖患者平均DLCO%pred、平均肺泡通氣量(alveolar ventilation,VA)%pred略低于對照組,平均滲透性因子(kCO,Krogh因子)高于對照組,其解釋為研究中的肥胖患者基礎肺容量較低,彌散能力也較低,同時肥胖相關的疾病也可能導致彌散受限。例如肺泡-毛細血管屏障受損,2型糖尿病導致肺泡微血管儲備和肺容量的減少等。Chance等[15]針對69例2型糖尿病組(BMI<30 kg/m2者32例、BMI≥30 kg/m2者37例)和45例正常對照組進行研究,發現肥胖患者DLCO%pred低于對照組。可能原因是2型糖尿病患者肺泡壁內結締組織沉積,這一實質改變使肺泡毛細血管募集功能受損,而肥胖相關的脂肪浸潤、脂質沉積等放大了這一因素的影響,進而影響彌散功能。本研究中BMI≥40 kg/m2時,患者DLCO%pred隨BMI增加而下降,可能原因是極度肥胖時肺泡組織受脂肪浸潤或結締組織沉積導致的擴散障礙,或肥胖相關的其他疾病導致的彌散受限[25]。
然而,本研究顯示BMI<40 kg/m2時,DLCO%pred隨BMI增加而增加,可能原因是超重和肥胖患者總循環血量增加,肺血容量增高,肺毛細血管床募集增多,彌散量也隨之增加[22]。國外也有學者認為肥胖患者彌散功能隨肥胖程度增加而增加。Saydain等[10]對高DLCO組(即>140%的預測值)和正常DLCO組(即85%~115%的預測值)各245例的一般信息、肺功能數據、臨床診斷進行分析,發現高DLCO與更大的BMI值和肥胖等診斷相關。Jones等[11]研究發現BMI增加時DLCO%pred有輕度升高(r=0.31,P<0.000 1)。Ray等[12]對43名非吸煙肥胖患者的肺功能數據進行分析,發現體重/身高比為0.6~1.2 kg/cm的范圍內,DLCO%pred隨著肥胖程度的增加而增加。這與我們的結果部分一致。肺彌散功能檢查指南中也提到,肥胖、世居高原、平臥體位、早期的紅細胞增多癥等均屬于能使正常情況下很少開放的肺毛細血管開放的生理或病理狀態,其肺毛細血管流量增加,彌散量增加[13]。
本研究存在一些不足。其一,該研究為回顧性、單中心研究,納入的患者較多為女性(62.3%),在男性群體中結果的外推性還需考慮。未來的研究需要更多大樣本、多中心的前瞻性研究或隨機對照試驗。其二,除常規肺功能檢測外,還可以考慮使用脈沖震蕩等更為先進的技術來進行測試,以明確肥胖對呼吸系統的影響,探索可能的病理生理學機制。
本研究的亮點在于,樣本肥胖分級基于2000年WHO西太平洋地區亞洲成人體重分級建議,并結合了2002年亞太地區WHO專家顧問組針對亞太地區人群的體質及與肥胖有關疾病的建議,較為細化。可以識別不同肥胖程度下患者的肺功能特征和表現,為個性化治療、風險預測和研究結果的可比性提供更有力的支持。此外,本研究關注到極度肥胖時的彌散功能改變這一研究較少的問題,并就目前存在爭議的BMI與DLCO的關系,提出了以BMI=40 kg/m2為截點的分段線性回歸關系圖,并解釋了彌散隨BMI變化可能的病理生理學機制,有賴于更多的研究做進一步的討論和論證。
綜上所述,本研究結果表明DLCO%pred隨BMI的增加表現為雙向變化,存在變化截點。當BMI<40 kg/m2時,DLCO %pred與BMI存在正相關關系,可能原因是超重和肥胖患者總循環血量增加使得肺血容量增高,從而增大了肺毛細血管床的募集,提高了彌散量;當BMI≥40 kg/m2時,DLCO %pred與BMI則存在負相關關系,可能原因是極度肥胖時肺泡組織受脂肪浸潤或結締組織沉積,從而導致氣體擴散能力受限,降低了彌散量,或者考慮肥胖相關的其他疾病導致的彌散受限。
利益沖突:本研究不涉及任何利益沖突。