引用本文: 徐朗, 蘇健芬, 張燦華, 王冰娜, 付喜花, 彭新生. 基于生物信息學與機器學習挖掘急性肺損傷相關標志物. 中國呼吸與危重監護雜志, 2024, 23(11): 784-790. doi: 10.7507/1671-6205.202404045 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
急性肺損傷(acute lung injury,ALI)及更嚴重的急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)是常見的危重癥,臨床上表現為進行性低氧血癥和呼吸窘迫,其發病率和病死率極高,且無特效治療方法[1]。據估計,在美國每年有190 600例ALI病例并有74 500人死亡[2]。目前認為在ARDS早期,中性粒細胞會黏附于血管內皮細胞表面并釋放大量促炎介質加劇炎癥,因此遏制炎癥反應是治療的必要措施[3]。機器學習廣義上是指將模型擬合到數據中或識別數據中信息分組的過程,其中監督學習可以將模型擬合至已標記的數據當中。本研究采用最小絕對收縮和選擇算子(LASSO)回歸與支持向量機遞歸特征消除(SVM-RFE)兩種機器學習方法。LASSO回歸是一種壓縮估計方法,通過構造懲罰函數來達到防止過度擬合的目的[4-5]。SVM-RFE是一種基于SVM的高效的特征選擇算法[6]。
1 材料與方法
1.1 數據下載與預處理
以“acute lung injury”和“lipopolysaccharide”為關鍵詞,從基因表達數據庫(GEO)(
1.2 差異基因鑒定
使用Limma[7]包對數據集GSE2411和GSE111241進行差異表達分析,差異表達基因(differentially expressed genes,DEGs)的篩選標準為P<0.05,|log2fold change|>1,使用“pheatmap”和“ggplot”包繪制熱圖和火山圖。取數據集GSE2411和GSE111241的DEGs做交集繪制韋恩圖。
1.3 功能富集分析
使用“clusterProfiler”[8]包對DEGs進行基因本體(gene ontology,GO)和京都基因與基因組百科全書(Kyoto Encyclopedia of Genes and Genomes,KEGG)分析,并用ggplot2包可視化。
1.4 GSEA富集分析
使用MSigDB數據庫中小鼠的M5數據集作為參考數據,使用“clusterProfiler”包對DEGs進行GSEA富集分析,可以進一步確定LPS誘導ALI/ARDS的生物學過程和途徑。
1.5 蛋白互作網絡
為了收集蛋白質相互作用的數據,我們將于1.2中取交集后的DEGs上傳到STRING數據庫(Search Tool for Retrieval of Interacting Genes/Proteins)中構建蛋白互作網絡(protein-protein interaction,PPI),其中將互作分數大于0.9鑒定為高互作分數標志物。
1.6 機器學習鑒定關鍵標志物
使用兩種機器學習的方法來進一步鑒定關鍵標志物。使用“glmnet”包進行LASSO回歸分析,使用“e1071”包進行SVM-RFE分析,然后將LASSO回歸與SVM-RFE的篩選基因進行交集作為關鍵標志物,隨后將關鍵標志物與高互作分數標志物進行交集,并使用“pROC”包繪制受試者操作特征曲線(receiver operating characteristic curve,ROC曲線)。
1.7 CIBERSORT免疫浸潤
使用R語言中的“CIBERSORT”算法確定免疫細胞浸潤程度,然后采用“corrplot”包研究關鍵基因與免疫細胞的相關性。
2 結果
2.1 DEGs的識別
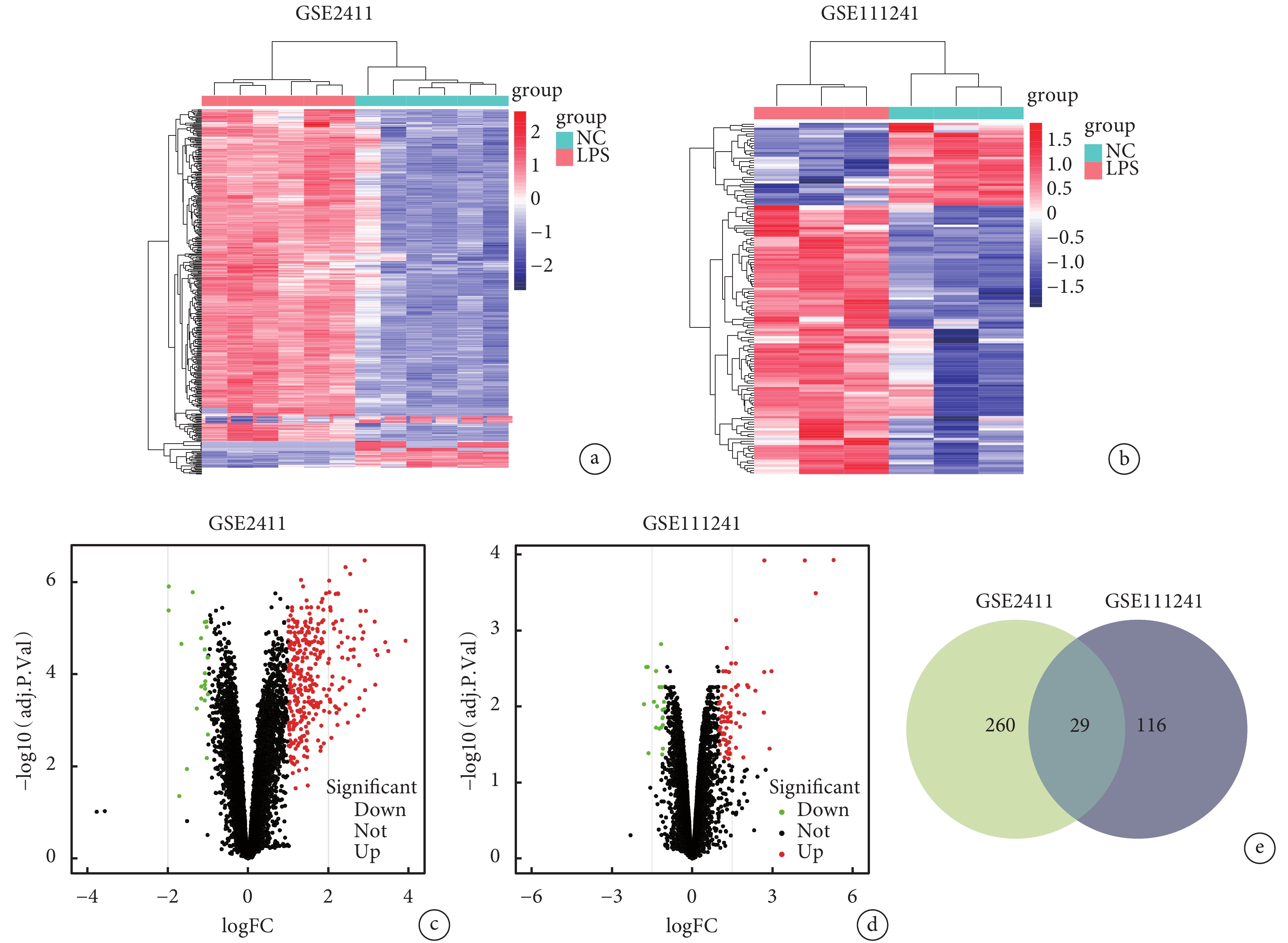
GSE2411共獲得289個DEGs,其中266個上調基因,23個下調基因。GSE111241共獲得145個DEGs,其中111個上調基因,34個下調基因。并繪制熱圖和火山圖(圖1a~d)。將兩個數據集獲得的DEGs取交集后共獲得29個DEGs(圖1e)。
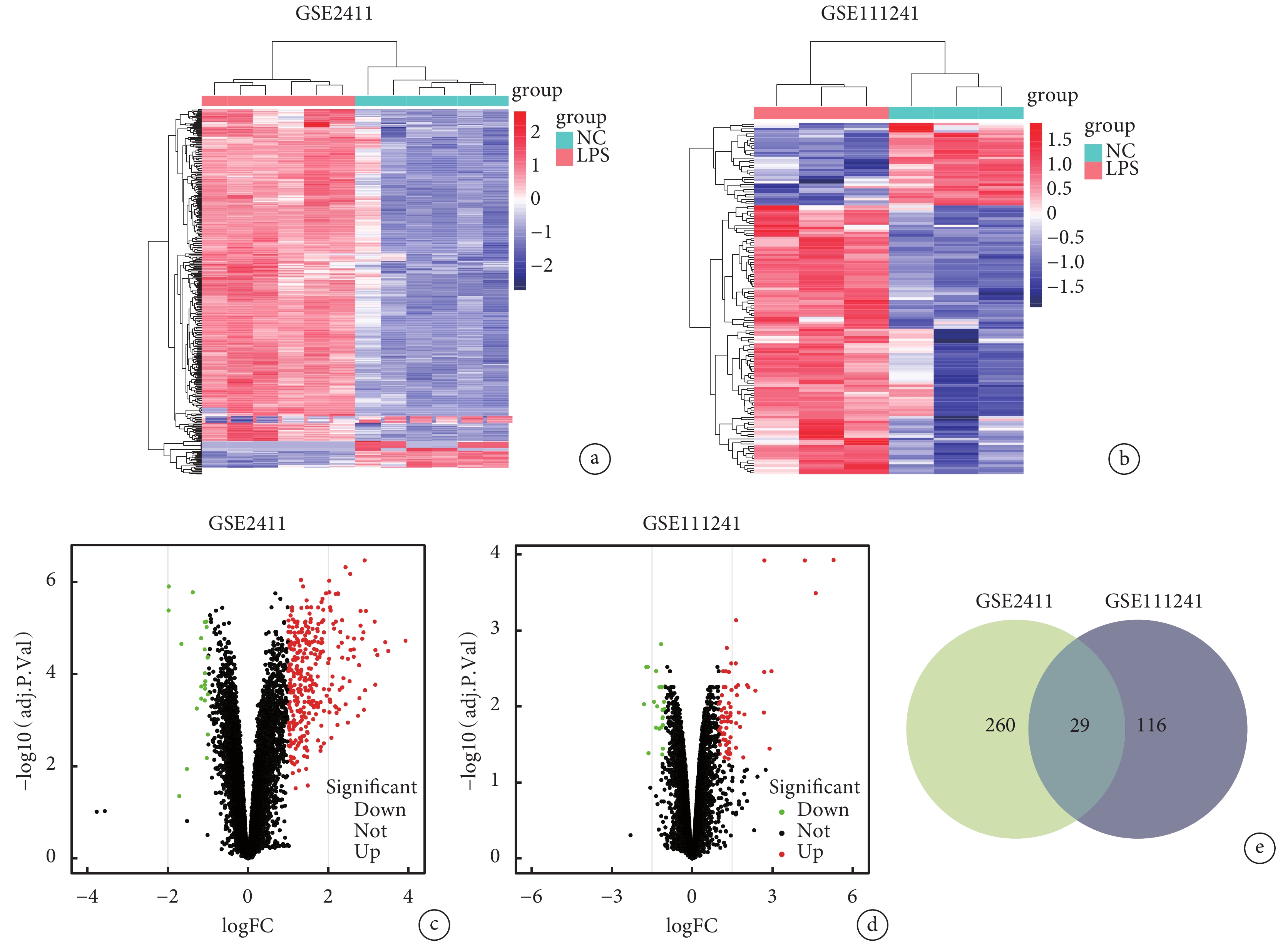 圖1
DEGs熱圖、火山圖和交集所得韋恩圖
圖1
DEGs熱圖、火山圖和交集所得韋恩圖
a~b. DEGs表達熱圖;c~d. DEGs表達火山圖;e. GSE2411獲得的260個DEGs與GSE111241獲得的116個DEGs進行交集獲得29個共同DEGs。NC:對照組;LPS:LPS誘導ALI組。
2.2 功能富集分析
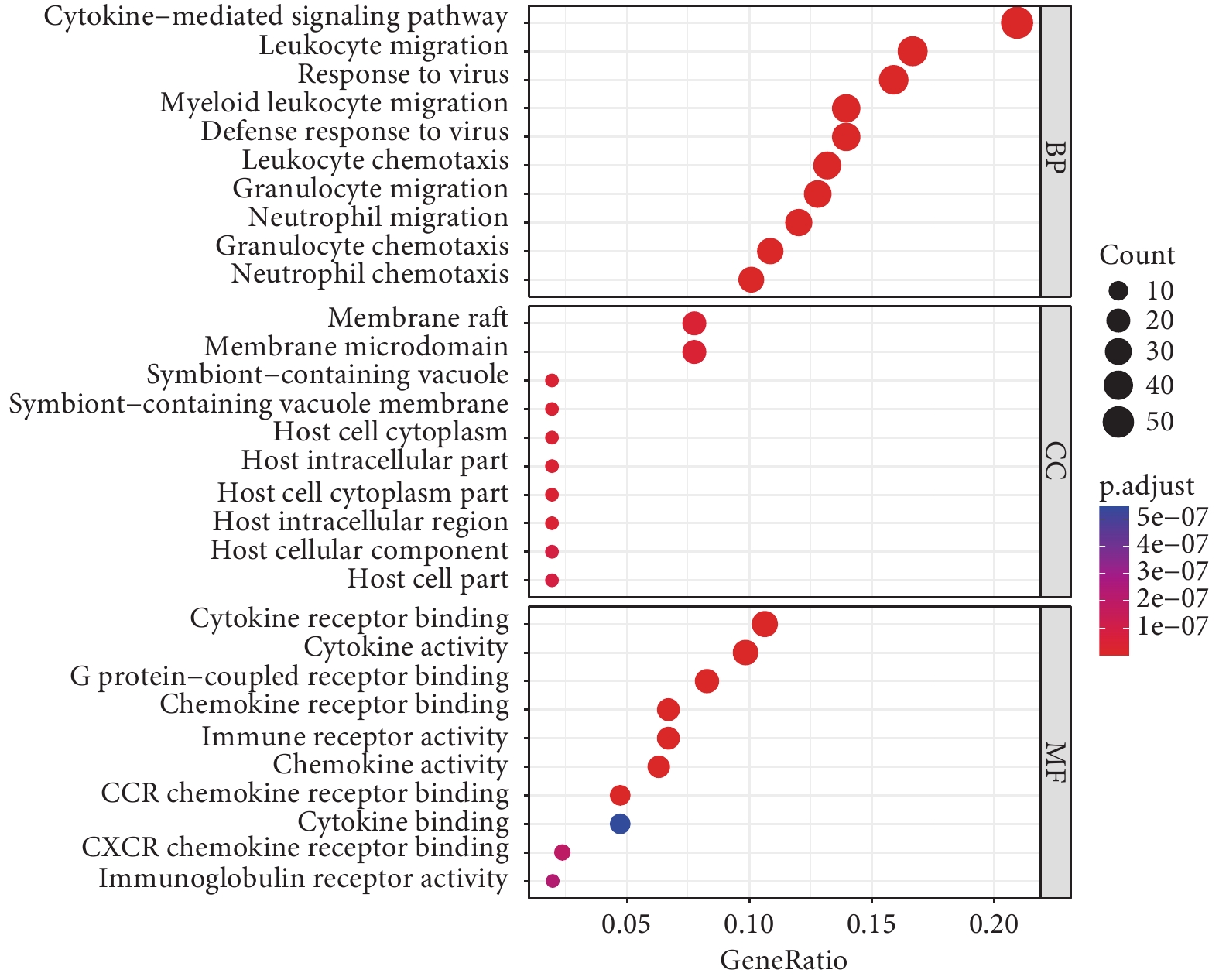
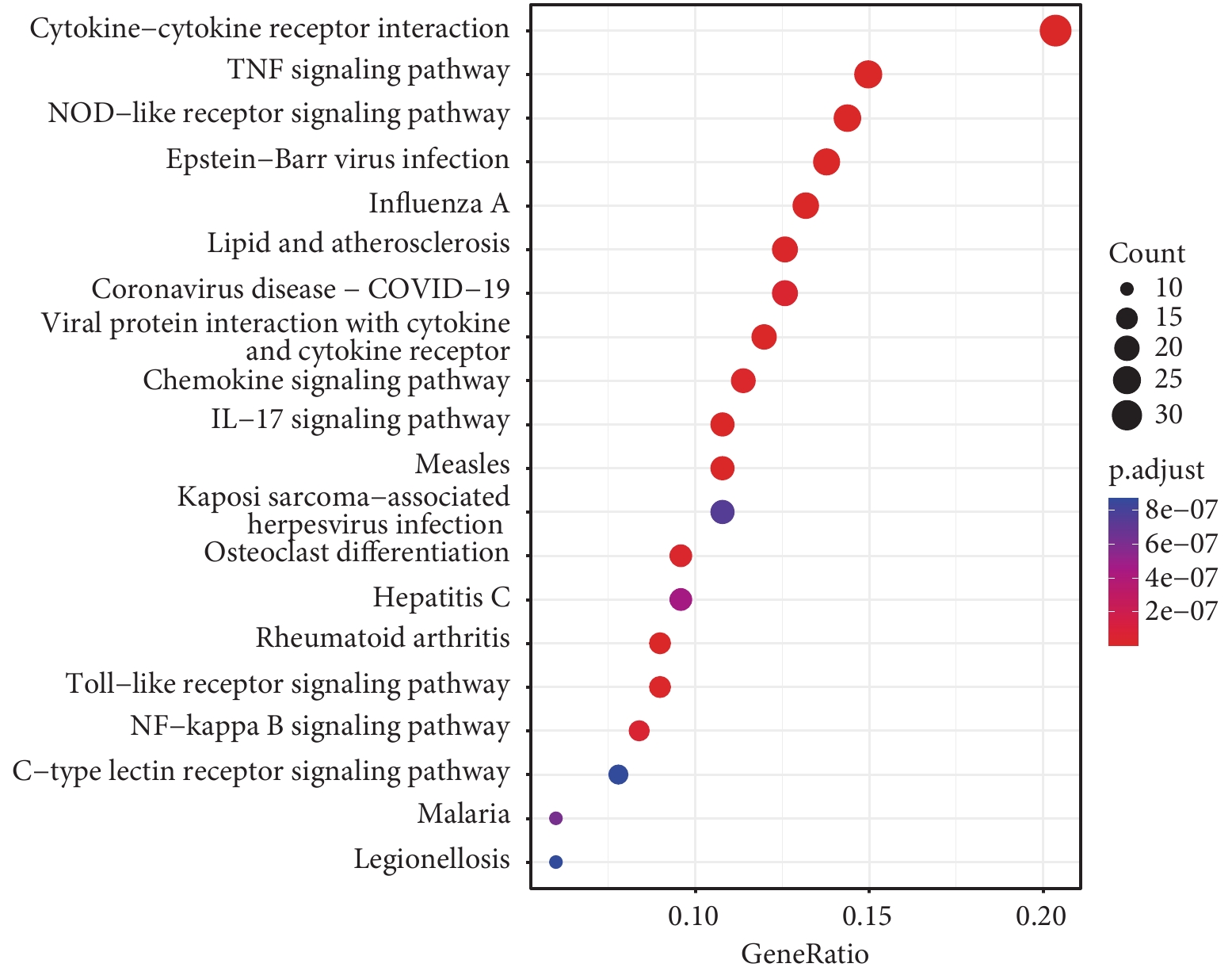
GO(圖2)生物過程研究發現,這些DEGs顯著參與細胞因子介導的信號通路、白細胞游走和EB病毒遺傳缺陷反應后的免疫缺陷(response to virus)等;細胞組分研究發現參與膜筏和膜微區等;分子功能研究發現參與細胞因子受體結合、細胞因子活性和G蛋白-偶聯受體結合等。KEGG(圖3)研究發現參與細胞因子-細胞因子受體相互作用、腫瘤壞死因子(tumor necrosis factor,TNF)信號通路和NOD樣受體信號等通路。
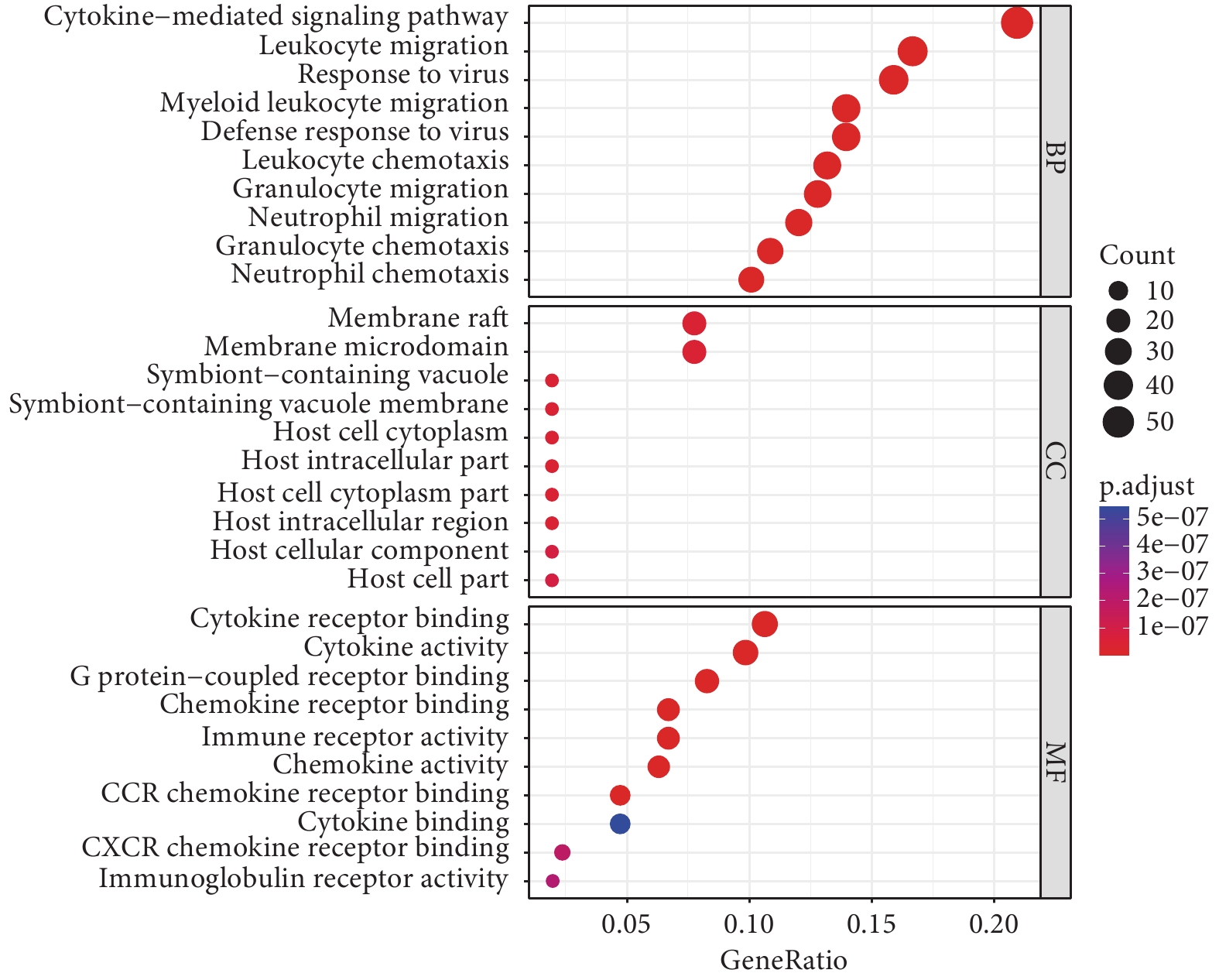 圖2
GO分析氣泡圖
圖2
GO分析氣泡圖
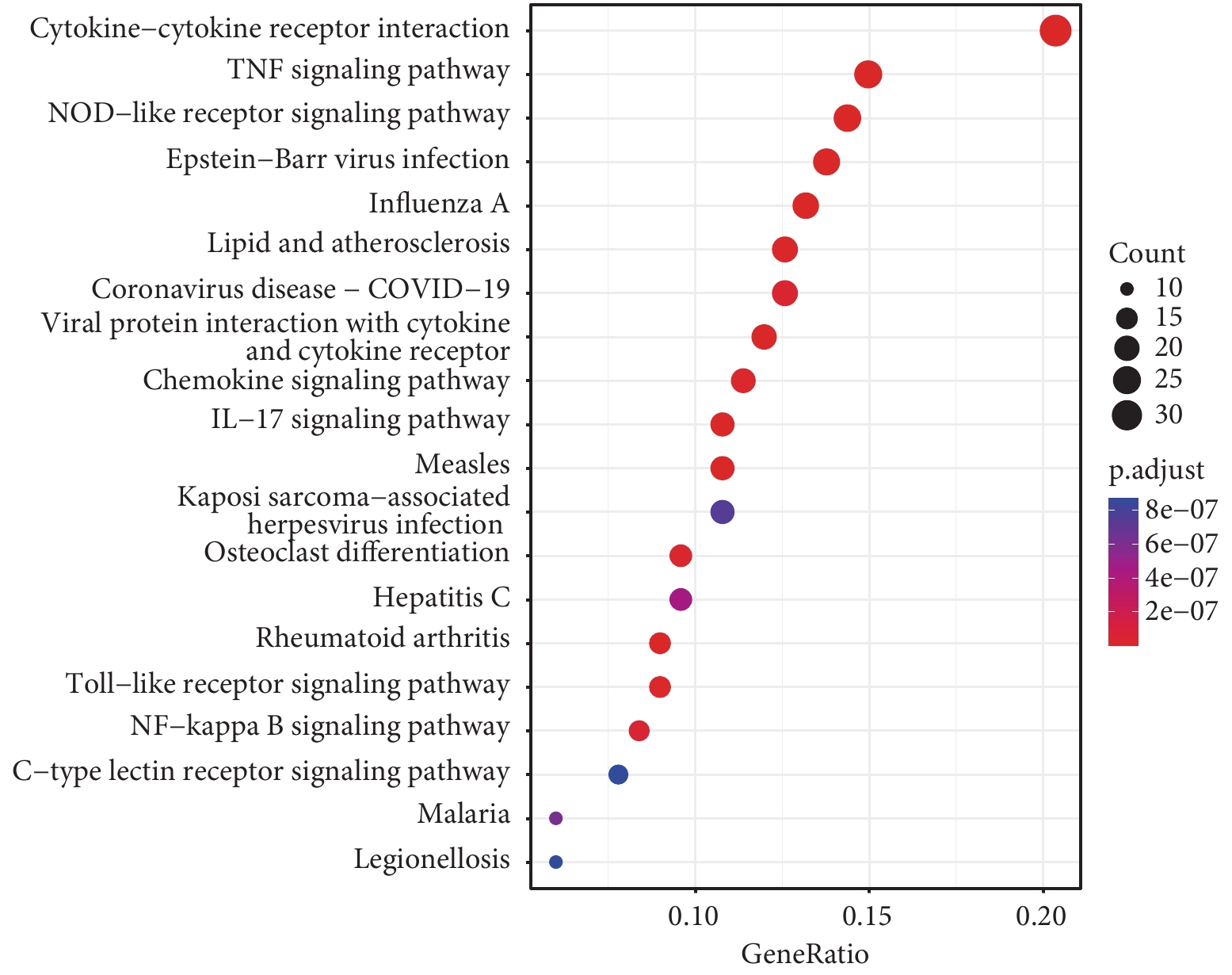 圖3
KEGG分析氣泡圖
圖3
KEGG分析氣泡圖
2.3 GSEA富集分析
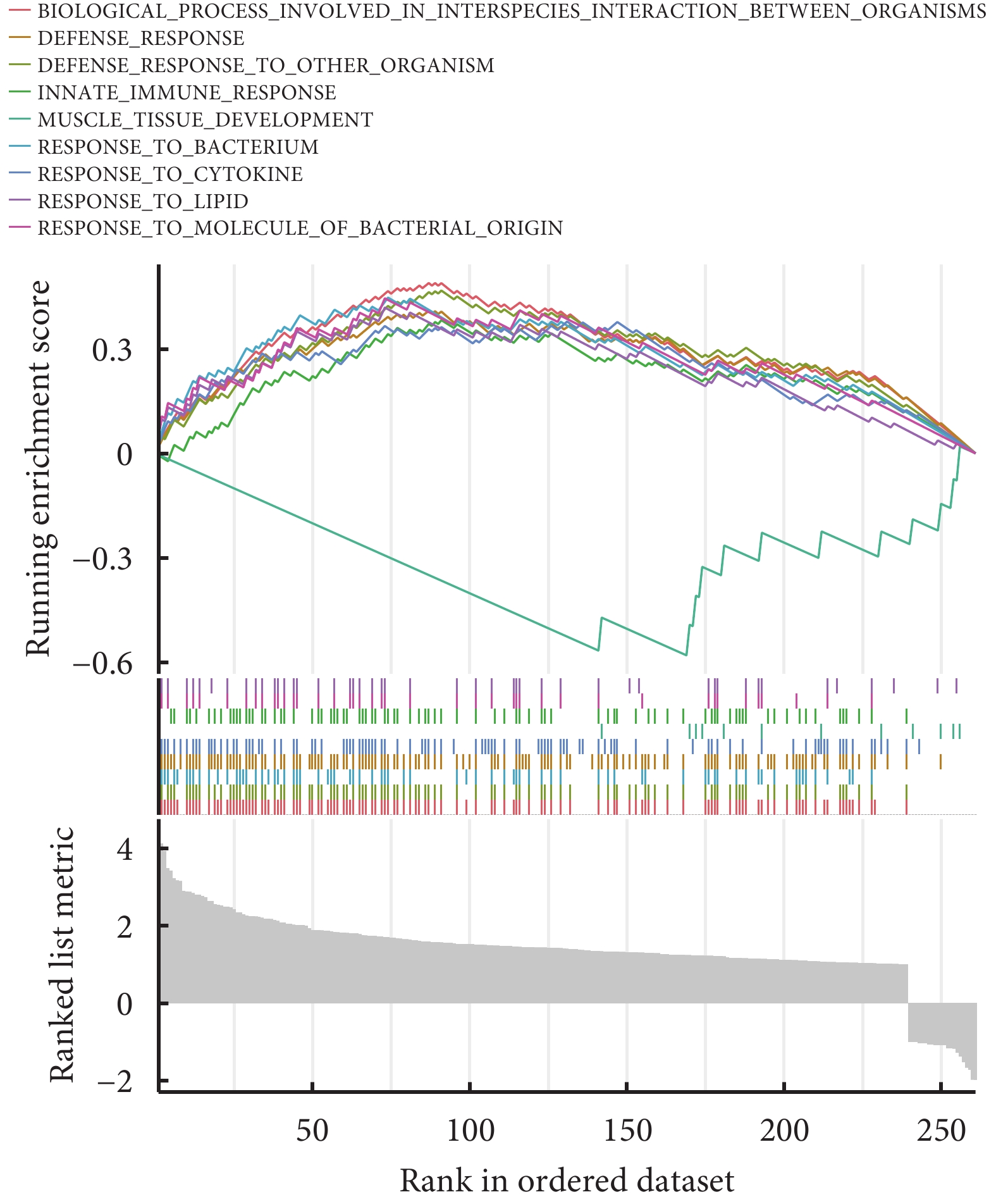
GSEA富集分析(圖4)顯示,這些DEGs顯著參與了生物間相互作用的生物過程、防御反應、對其他生物的防御反應、先天免疫反應、肌肉組織發育、對細菌的反應、細胞因子反應、對脂質的反應、對細菌分子的反應。
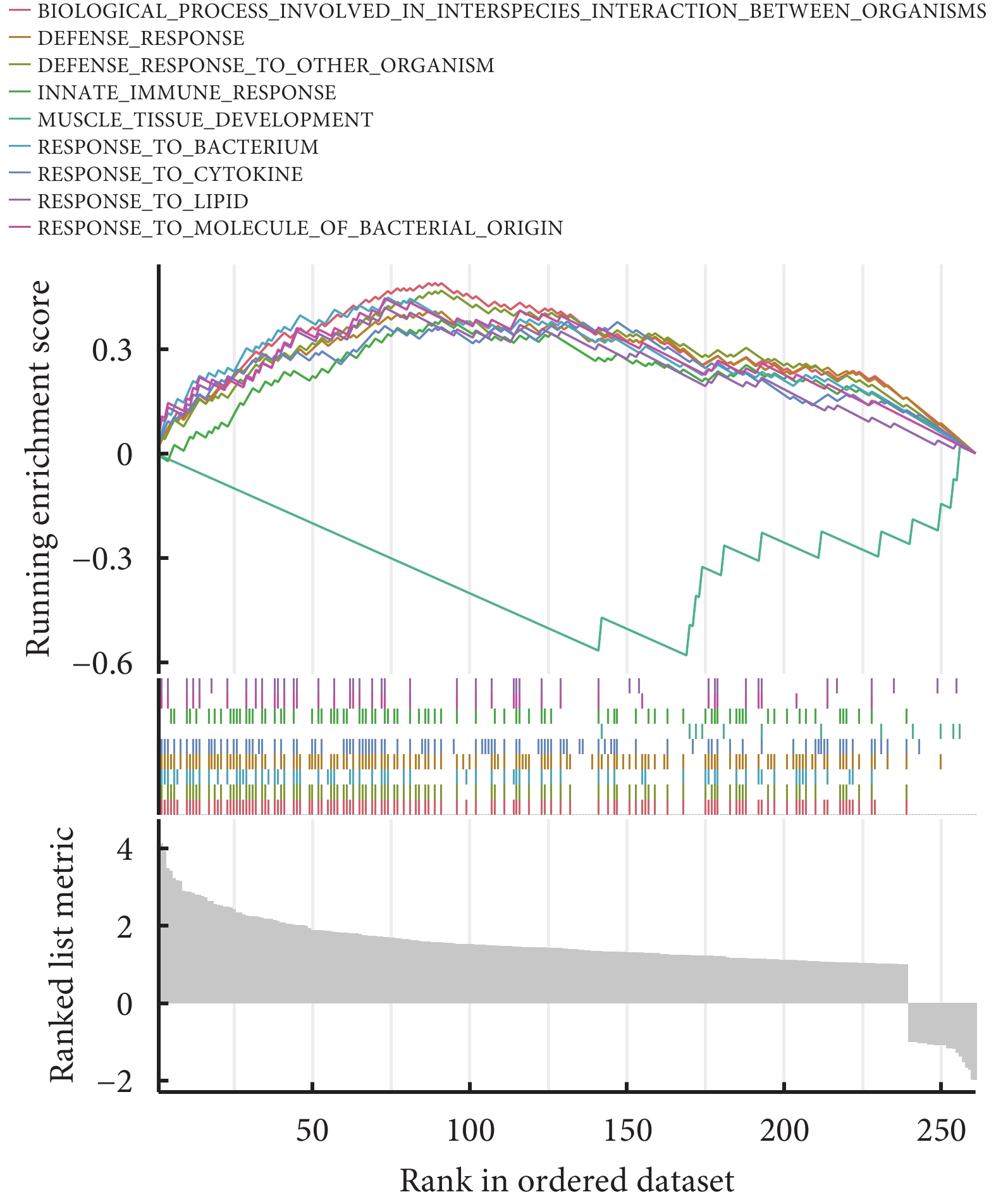 圖4
GSEA富集分析
圖4
GSEA富集分析
2.4 PPI的構建
將獲得的29個交集基因上傳至STRING數據庫,將最低要求交互分數調整為最高可靠性(0.9),最終獲得13個基因:Stat3、Irf7、Mx1、Usp18、Rtp4、Ifi44、Eif2ak2、Ddx60、Sod2、Gpx2、Ccl20、Cxcl1和Il1a。
2.5 鑒定關鍵標志物
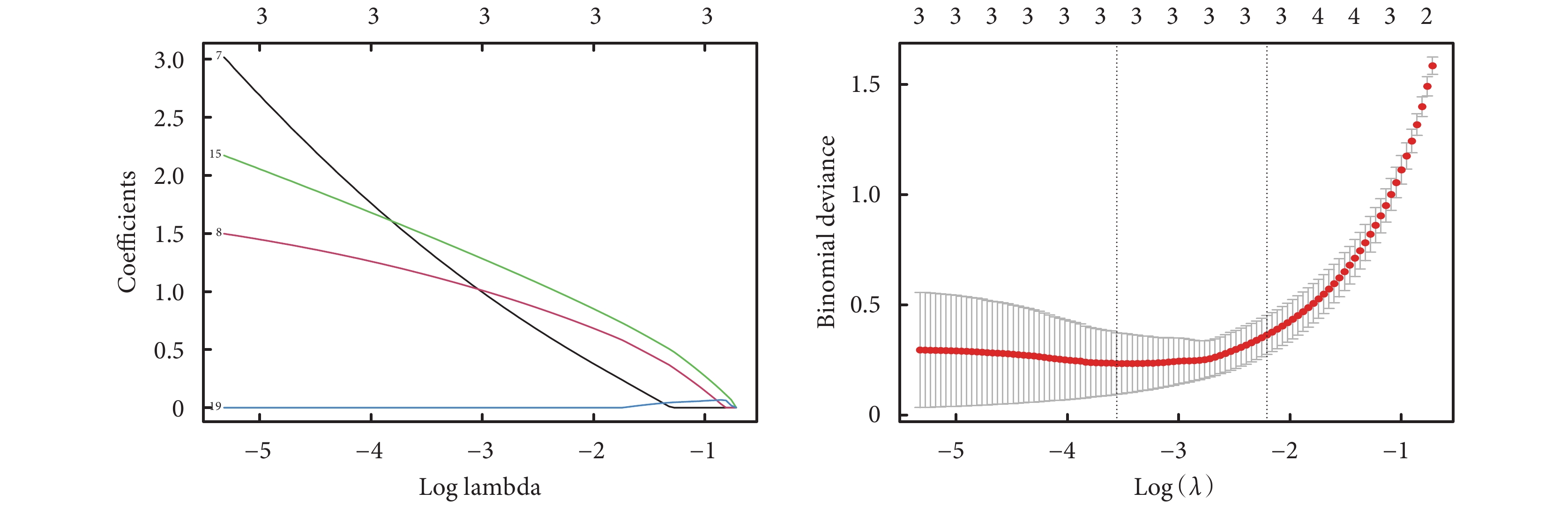
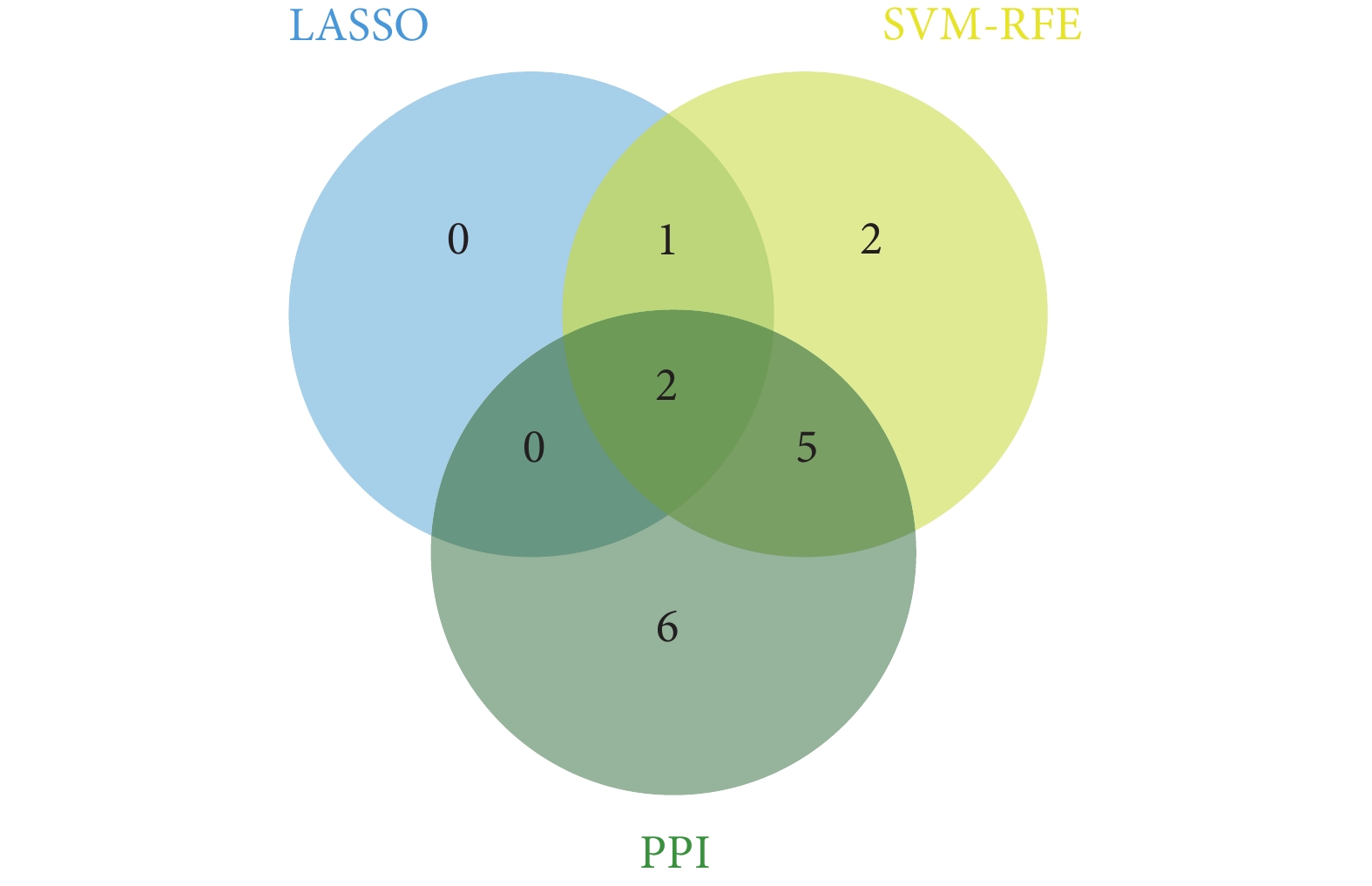
使用兩種機器學習的方式分別鑒定29個交集DEGs中的關鍵標志物。通過LASSO回歸鑒定出3個關鍵基因:Gpx2、Ifi44和Nfkbiz(圖5)。通過SVM-RFE鑒定出其中排名前十的關鍵基因:Gpx2、Nfkbiz、ifi44、Cxcl1、Znfx1、Il1a、Irf7、Usp18、Saa3和Rtp4。將兩種機器學習鑒定出的關鍵基因與PPI中獲得的高互作分數基因進行交集,即獲得關鍵標志物:Gpx2和Ifi44(圖6)。
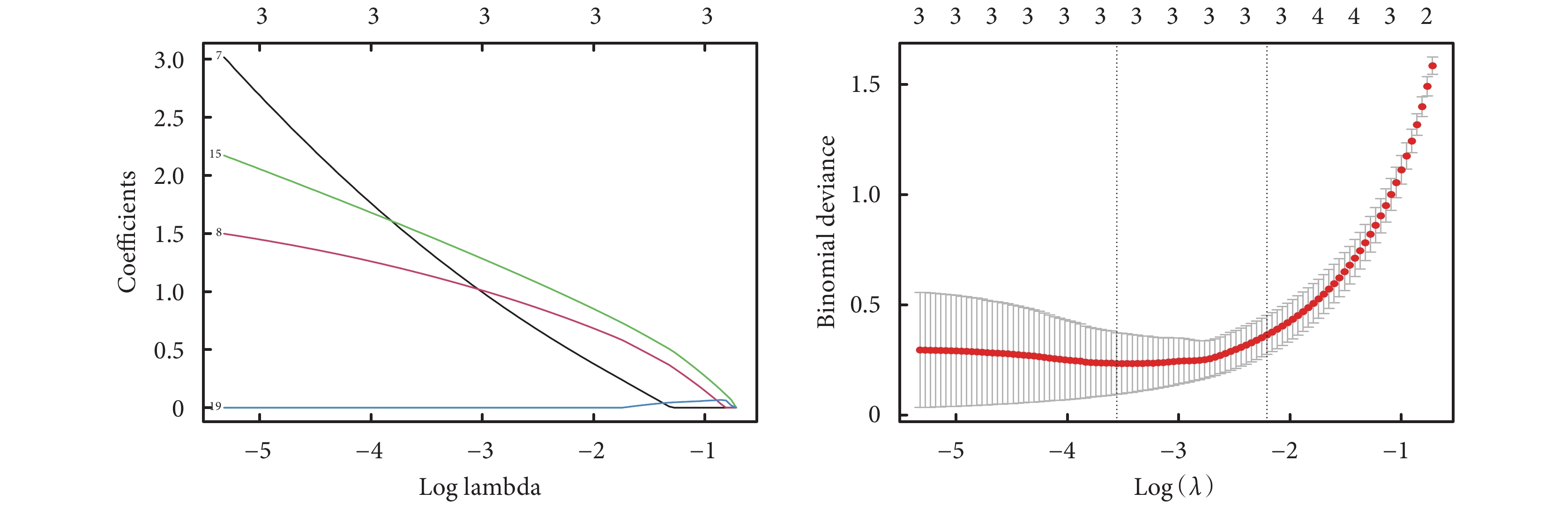 圖5
L ASSO回歸分析
圖5
L ASSO回歸分析
 圖6
韋恩圖
圖6
韋恩圖
2.6 診斷效能及驗證
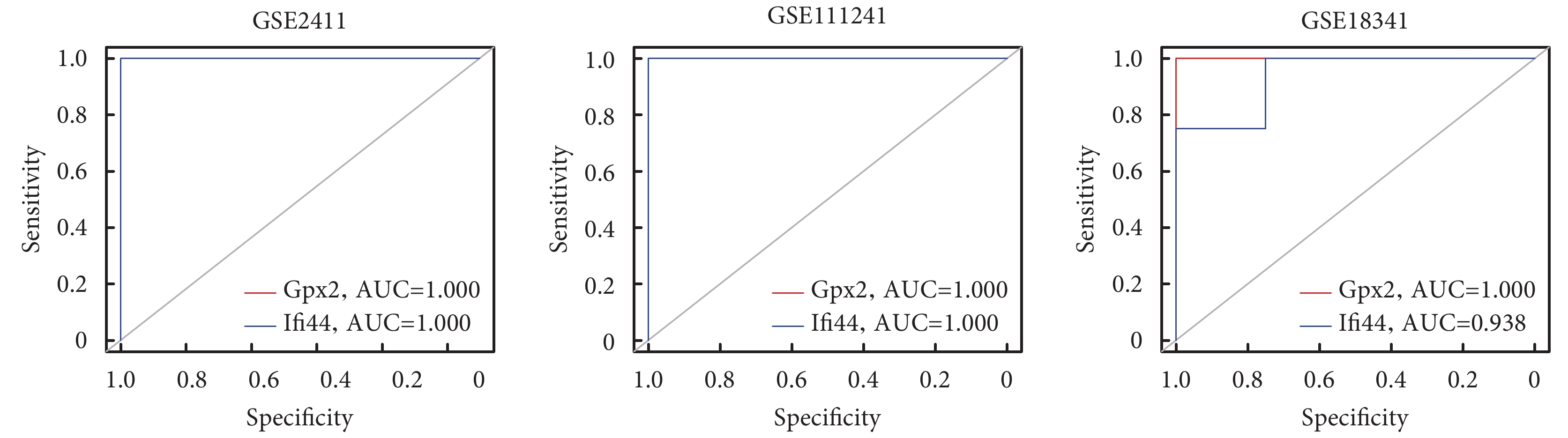
利用“pROC”包對數據集GSE2411、GSE111241和驗證集GSE18341中的關鍵標志物的表達數據進行分析,并繪制ROC曲線。結果顯示Gpx2在三個數據集中的ROC曲線下面積(area under ROC curve,AUC)均為1.0,Ifi44在數據集GSE2411和GSE111241中的AUC為1.0,而在GSE18341中為0.938(圖7)。兩種生物標志物的AUC均大于0.9,具有較高的診斷效能。
 圖7
標志物在數據集GSE2411、GSE111241和GSE18341中的ROC曲線
圖7
標志物在數據集GSE2411、GSE111241和GSE18341中的ROC曲線
2.7 免疫浸潤及其相關性分析
為了研究ALI小鼠免疫浸潤情況,我們以小鼠的免疫細胞細胞數據集作為參考數據集[9],分析了23種免疫細胞的浸潤程度(圖8a)。發現ALI小鼠與正常小鼠的免疫細胞類型存在明顯差異。然后通過免疫相關性分析發現中性粒細胞、CD8陰性T細胞、M1巨噬細胞、單核細胞、活化樹突狀細胞與Ifi44和Gpx2均呈正相關,肥大細胞、嗜酸性粒細胞、幼稚B細胞、漿細胞、CD8陽性T細胞、CD8記憶T細胞、M0巨噬細胞、M2巨噬細胞、調節性T細胞、CD4記憶T細胞、CD4幼稚T細胞、CD4陽性T細胞、輔助性T細胞17、γδT細胞、NK靜息細胞、NK活化細胞、未成熟樹突狀細胞與Ifi44和Gpx2均呈負相關,而B記憶細胞與Ifi44呈負相關,與Gpx2則呈正相關(圖8b)。通過CIBERSORT分析發現ALI小鼠與正常小鼠的中性粒細胞、嗜酸性細胞、調節性T細胞、CD4陰性T細胞、輔助性T細胞17、活化樹突狀細胞、未成熟樹突狀細胞存在顯著差異(圖8c)。
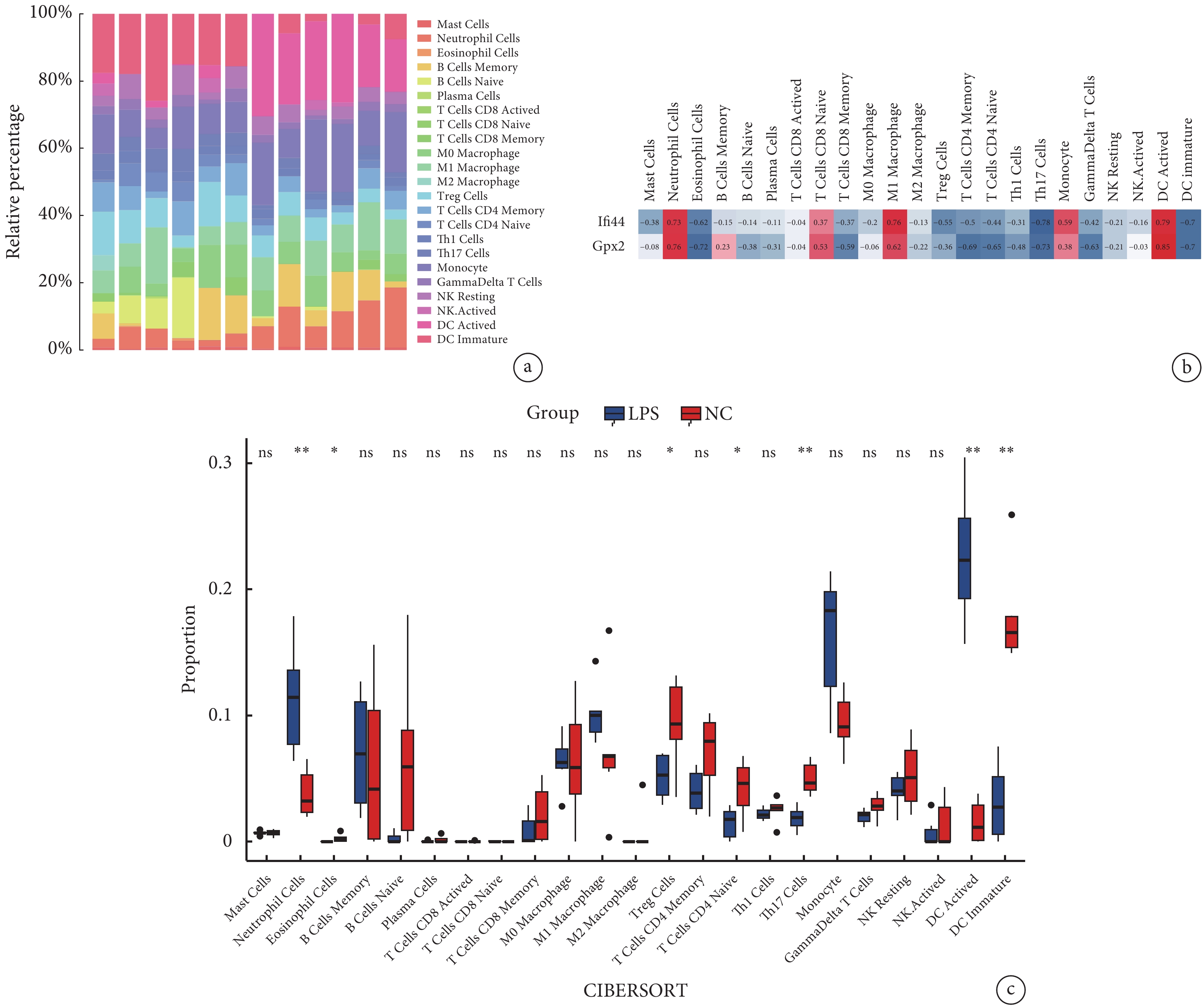 圖8
免疫浸潤分析
圖8
免疫浸潤分析
a. 23種免疫細胞比例;b. 關鍵標志物與23種免疫細胞的相關性;c. 23種免疫細胞的表達差異。NC:對照組;LPS:LPS誘導ALI組;*
3 討論
ARDS是一種急性呼吸系統疾病,具有很大的異質性[10]。雖然近年來在患者護理方面取得了一些進展,降低了患者的發病率和病死率,然而由于目前并沒有針對ARDS的治療藥物被證明可以降低病死率,ARDS依然是常見且十分致命的疾病[11]。因此,開發生物標志物對于改善ALI/ARDS預后是至關重要的。本研究采用了LASSO和SVM-RFE這兩種已被廣泛應用于特征篩選的監督機器學習的方法[12-15]。LASSO可擬合正則線性回歸模型,但同時也會懲罰具有大量非零系數的解[16]。SVM-RFE是一種以權重大小為排序標準的一種遞歸特征消除方法,并由于懲罰機制而不容易出現過擬合[12,17]。本研究對數據集GSE2411和GSE111241分別進行差異分析,取交集后共獲得29個DEGs。隨后通過機器學習及PPI進一步篩選關鍵標志物,最后確定了兩個關鍵標志物:Gpx2和Ifi44。
Gpx2是抗氧化酶谷胱甘肽過氧化物酶家族的成員。研究表明可能通過阻止炎癥介質的分泌來激活Gpx2,其可通過抑制促炎趨化因子和細胞因子來減弱炎癥[18]。根據鐵死亡數據庫(FerrDb),Gpx2被標記為鐵死亡標志物,表明其參與調控鐵死亡,但是尚不清楚其具體作用[19]。鐵死亡是一種最近發現的不同于凋亡、壞死和自噬的細胞死亡類型,其涉及鐵、脂質和氨基酸的異常代謝過程[20]。作為一種鐵依賴過程,鐵超載會驅動鐵死亡進程[21],因為鐵死亡具有免疫原性,發生鐵死亡的細胞會釋放炎癥因子和損傷相關分子模式(damage associated molecular patterns,DAMPs)[22],這一系列促炎作用可能會加劇ALI/ARDS。
Ifi44為干擾素誘導蛋白44,是一種Ⅰ型干擾素(interferon,IFN)誘導蛋白,可以負向調節IFN反應,同時可以負向調控核因子κB通路減少炎癥因子[23-24]。IFN是一種由感染細胞分泌的多肽,具有限制感染因子、調節先天免疫反應和激活適應性免疫系統的功能,在急性病毒感染起到保護作用,而在細菌感染和自身免疫疾病中可能具有保護或有害作用。因此Ⅰ型IFN正在成為慢性感染中炎癥和免疫抑制的關鍵驅動因素[25-26]。Ifi44對IFN的負向調節作用有可能影響ALI/ARDS的發展。
CIBERSORT研究發現對比正常組,LPS組的中性粒細胞和活化樹突細胞浸潤顯著升高,而調節性T細胞、輔助性T細胞17和未分化樹突細胞顯著降低。本研究中免疫相關性分析表明Gpx2與中性粒細胞、輔助性T細胞17、M1巨噬細胞和活化樹突細胞等細胞相關度較高,Ifi44與中性粒細胞、M1巨噬細胞、調節性T細胞、輔助性T細胞17和活化樹突細胞相關度較高。巨噬細胞在ALI/ARDS扮演了十分重要的角色,在ALI/ARDS急性期,巨噬細胞通常從交替活化表型(M2)轉變為經典活化表型(M1),并釋放各種強效促炎介質。在后期,巨噬細胞則會從M1表型交替回M2表型,以消除凋亡細胞并參與纖維化[27]。有研究表明,LPS可使中性粒細胞產生中性粒細胞外陷阱(neutrophil extracellular traps,NETs),而NETs可加劇肺組織損傷以及炎癥[28-29]。調節性T細胞被證實可以促進組織修復,并且可以調節肺部炎癥中的Th免疫應答[30]。輔助性T細胞17被證明可能通過產生白細胞介素(interleukin,IL)-17和IL-22來引起炎癥并介導ALI[31],但是具體分化機制仍不清楚。
ALI/ARDS可由多種重癥引起,包括但不限于感染、膠原血管疾病、免疫介導的肺出血等[32]。大多數ALI/ARDS患者因全身炎癥反應死于多器官功能障礙綜合征[33]。在此過程中免疫細胞及其分泌的細胞因子起著重要作用[34]。本研究DEGs的富集分析表明這些DEGs與機體免疫高度相關,包括GSEA富集的先天免疫反應與KEGG富集的TNF、IL-17、Toll樣受體(Toll-like receptors,TLR)等信號通路,其中TNF為促炎因子信號通路;IL-17被證實參與ALI/ARDS的發病;TLR可誘導炎癥反應導致ALI[32,35]。
綜上所述,Gpx2與Ifi44具有潛在的免疫調節能力,可作為LPS誘導ALI的小鼠模型治療的潛在生物標志物,可以為探索ALI機制和潛在靶點提供新的方向。但是本研究仍存在一定的局限性,因為研究是基于公共數據庫的小鼠數據進行挖掘,同時還存在納入樣本量偏少的問題,對研究結果的準確性存在一定影響。這些生物標志物需要進一步的擴大樣本研究以及體內外實驗加以驗證。
利益沖突:本研究不涉及任何利益沖突。
急性肺損傷(acute lung injury,ALI)及更嚴重的急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)是常見的危重癥,臨床上表現為進行性低氧血癥和呼吸窘迫,其發病率和病死率極高,且無特效治療方法[1]。據估計,在美國每年有190 600例ALI病例并有74 500人死亡[2]。目前認為在ARDS早期,中性粒細胞會黏附于血管內皮細胞表面并釋放大量促炎介質加劇炎癥,因此遏制炎癥反應是治療的必要措施[3]。機器學習廣義上是指將模型擬合到數據中或識別數據中信息分組的過程,其中監督學習可以將模型擬合至已標記的數據當中。本研究采用最小絕對收縮和選擇算子(LASSO)回歸與支持向量機遞歸特征消除(SVM-RFE)兩種機器學習方法。LASSO回歸是一種壓縮估計方法,通過構造懲罰函數來達到防止過度擬合的目的[4-5]。SVM-RFE是一種基于SVM的高效的特征選擇算法[6]。
1 材料與方法
1.1 數據下載與預處理
以“acute lung injury”和“lipopolysaccharide”為關鍵詞,從基因表達數據庫(GEO)(
1.2 差異基因鑒定
使用Limma[7]包對數據集GSE2411和GSE111241進行差異表達分析,差異表達基因(differentially expressed genes,DEGs)的篩選標準為P<0.05,|log2fold change|>1,使用“pheatmap”和“ggplot”包繪制熱圖和火山圖。取數據集GSE2411和GSE111241的DEGs做交集繪制韋恩圖。
1.3 功能富集分析
使用“clusterProfiler”[8]包對DEGs進行基因本體(gene ontology,GO)和京都基因與基因組百科全書(Kyoto Encyclopedia of Genes and Genomes,KEGG)分析,并用ggplot2包可視化。
1.4 GSEA富集分析
使用MSigDB數據庫中小鼠的M5數據集作為參考數據,使用“clusterProfiler”包對DEGs進行GSEA富集分析,可以進一步確定LPS誘導ALI/ARDS的生物學過程和途徑。
1.5 蛋白互作網絡
為了收集蛋白質相互作用的數據,我們將于1.2中取交集后的DEGs上傳到STRING數據庫(Search Tool for Retrieval of Interacting Genes/Proteins)中構建蛋白互作網絡(protein-protein interaction,PPI),其中將互作分數大于0.9鑒定為高互作分數標志物。
1.6 機器學習鑒定關鍵標志物
使用兩種機器學習的方法來進一步鑒定關鍵標志物。使用“glmnet”包進行LASSO回歸分析,使用“e1071”包進行SVM-RFE分析,然后將LASSO回歸與SVM-RFE的篩選基因進行交集作為關鍵標志物,隨后將關鍵標志物與高互作分數標志物進行交集,并使用“pROC”包繪制受試者操作特征曲線(receiver operating characteristic curve,ROC曲線)。
1.7 CIBERSORT免疫浸潤
使用R語言中的“CIBERSORT”算法確定免疫細胞浸潤程度,然后采用“corrplot”包研究關鍵基因與免疫細胞的相關性。
2 結果
2.1 DEGs的識別
GSE2411共獲得289個DEGs,其中266個上調基因,23個下調基因。GSE111241共獲得145個DEGs,其中111個上調基因,34個下調基因。并繪制熱圖和火山圖(圖1a~d)。將兩個數據集獲得的DEGs取交集后共獲得29個DEGs(圖1e)。
 圖1
DEGs熱圖、火山圖和交集所得韋恩圖
圖1
DEGs熱圖、火山圖和交集所得韋恩圖
a~b. DEGs表達熱圖;c~d. DEGs表達火山圖;e. GSE2411獲得的260個DEGs與GSE111241獲得的116個DEGs進行交集獲得29個共同DEGs。NC:對照組;LPS:LPS誘導ALI組。
2.2 功能富集分析
GO(圖2)生物過程研究發現,這些DEGs顯著參與細胞因子介導的信號通路、白細胞游走和EB病毒遺傳缺陷反應后的免疫缺陷(response to virus)等;細胞組分研究發現參與膜筏和膜微區等;分子功能研究發現參與細胞因子受體結合、細胞因子活性和G蛋白-偶聯受體結合等。KEGG(圖3)研究發現參與細胞因子-細胞因子受體相互作用、腫瘤壞死因子(tumor necrosis factor,TNF)信號通路和NOD樣受體信號等通路。
 圖2
GO分析氣泡圖
圖2
GO分析氣泡圖
 圖3
KEGG分析氣泡圖
圖3
KEGG分析氣泡圖
2.3 GSEA富集分析
GSEA富集分析(圖4)顯示,這些DEGs顯著參與了生物間相互作用的生物過程、防御反應、對其他生物的防御反應、先天免疫反應、肌肉組織發育、對細菌的反應、細胞因子反應、對脂質的反應、對細菌分子的反應。
 圖4
GSEA富集分析
圖4
GSEA富集分析
2.4 PPI的構建
將獲得的29個交集基因上傳至STRING數據庫,將最低要求交互分數調整為最高可靠性(0.9),最終獲得13個基因:Stat3、Irf7、Mx1、Usp18、Rtp4、Ifi44、Eif2ak2、Ddx60、Sod2、Gpx2、Ccl20、Cxcl1和Il1a。
2.5 鑒定關鍵標志物
使用兩種機器學習的方式分別鑒定29個交集DEGs中的關鍵標志物。通過LASSO回歸鑒定出3個關鍵基因:Gpx2、Ifi44和Nfkbiz(圖5)。通過SVM-RFE鑒定出其中排名前十的關鍵基因:Gpx2、Nfkbiz、ifi44、Cxcl1、Znfx1、Il1a、Irf7、Usp18、Saa3和Rtp4。將兩種機器學習鑒定出的關鍵基因與PPI中獲得的高互作分數基因進行交集,即獲得關鍵標志物:Gpx2和Ifi44(圖6)。
 圖5
L ASSO回歸分析
圖5
L ASSO回歸分析
 圖6
韋恩圖
圖6
韋恩圖
2.6 診斷效能及驗證
利用“pROC”包對數據集GSE2411、GSE111241和驗證集GSE18341中的關鍵標志物的表達數據進行分析,并繪制ROC曲線。結果顯示Gpx2在三個數據集中的ROC曲線下面積(area under ROC curve,AUC)均為1.0,Ifi44在數據集GSE2411和GSE111241中的AUC為1.0,而在GSE18341中為0.938(圖7)。兩種生物標志物的AUC均大于0.9,具有較高的診斷效能。
 圖7
標志物在數據集GSE2411、GSE111241和GSE18341中的ROC曲線
圖7
標志物在數據集GSE2411、GSE111241和GSE18341中的ROC曲線
2.7 免疫浸潤及其相關性分析
為了研究ALI小鼠免疫浸潤情況,我們以小鼠的免疫細胞細胞數據集作為參考數據集[9],分析了23種免疫細胞的浸潤程度(圖8a)。發現ALI小鼠與正常小鼠的免疫細胞類型存在明顯差異。然后通過免疫相關性分析發現中性粒細胞、CD8陰性T細胞、M1巨噬細胞、單核細胞、活化樹突狀細胞與Ifi44和Gpx2均呈正相關,肥大細胞、嗜酸性粒細胞、幼稚B細胞、漿細胞、CD8陽性T細胞、CD8記憶T細胞、M0巨噬細胞、M2巨噬細胞、調節性T細胞、CD4記憶T細胞、CD4幼稚T細胞、CD4陽性T細胞、輔助性T細胞17、γδT細胞、NK靜息細胞、NK活化細胞、未成熟樹突狀細胞與Ifi44和Gpx2均呈負相關,而B記憶細胞與Ifi44呈負相關,與Gpx2則呈正相關(圖8b)。通過CIBERSORT分析發現ALI小鼠與正常小鼠的中性粒細胞、嗜酸性細胞、調節性T細胞、CD4陰性T細胞、輔助性T細胞17、活化樹突狀細胞、未成熟樹突狀細胞存在顯著差異(圖8c)。
 圖8
免疫浸潤分析
圖8
免疫浸潤分析
a. 23種免疫細胞比例;b. 關鍵標志物與23種免疫細胞的相關性;c. 23種免疫細胞的表達差異。NC:對照組;LPS:LPS誘導ALI組;*
3 討論
ARDS是一種急性呼吸系統疾病,具有很大的異質性[10]。雖然近年來在患者護理方面取得了一些進展,降低了患者的發病率和病死率,然而由于目前并沒有針對ARDS的治療藥物被證明可以降低病死率,ARDS依然是常見且十分致命的疾病[11]。因此,開發生物標志物對于改善ALI/ARDS預后是至關重要的。本研究采用了LASSO和SVM-RFE這兩種已被廣泛應用于特征篩選的監督機器學習的方法[12-15]。LASSO可擬合正則線性回歸模型,但同時也會懲罰具有大量非零系數的解[16]。SVM-RFE是一種以權重大小為排序標準的一種遞歸特征消除方法,并由于懲罰機制而不容易出現過擬合[12,17]。本研究對數據集GSE2411和GSE111241分別進行差異分析,取交集后共獲得29個DEGs。隨后通過機器學習及PPI進一步篩選關鍵標志物,最后確定了兩個關鍵標志物:Gpx2和Ifi44。
Gpx2是抗氧化酶谷胱甘肽過氧化物酶家族的成員。研究表明可能通過阻止炎癥介質的分泌來激活Gpx2,其可通過抑制促炎趨化因子和細胞因子來減弱炎癥[18]。根據鐵死亡數據庫(FerrDb),Gpx2被標記為鐵死亡標志物,表明其參與調控鐵死亡,但是尚不清楚其具體作用[19]。鐵死亡是一種最近發現的不同于凋亡、壞死和自噬的細胞死亡類型,其涉及鐵、脂質和氨基酸的異常代謝過程[20]。作為一種鐵依賴過程,鐵超載會驅動鐵死亡進程[21],因為鐵死亡具有免疫原性,發生鐵死亡的細胞會釋放炎癥因子和損傷相關分子模式(damage associated molecular patterns,DAMPs)[22],這一系列促炎作用可能會加劇ALI/ARDS。
Ifi44為干擾素誘導蛋白44,是一種Ⅰ型干擾素(interferon,IFN)誘導蛋白,可以負向調節IFN反應,同時可以負向調控核因子κB通路減少炎癥因子[23-24]。IFN是一種由感染細胞分泌的多肽,具有限制感染因子、調節先天免疫反應和激活適應性免疫系統的功能,在急性病毒感染起到保護作用,而在細菌感染和自身免疫疾病中可能具有保護或有害作用。因此Ⅰ型IFN正在成為慢性感染中炎癥和免疫抑制的關鍵驅動因素[25-26]。Ifi44對IFN的負向調節作用有可能影響ALI/ARDS的發展。
CIBERSORT研究發現對比正常組,LPS組的中性粒細胞和活化樹突細胞浸潤顯著升高,而調節性T細胞、輔助性T細胞17和未分化樹突細胞顯著降低。本研究中免疫相關性分析表明Gpx2與中性粒細胞、輔助性T細胞17、M1巨噬細胞和活化樹突細胞等細胞相關度較高,Ifi44與中性粒細胞、M1巨噬細胞、調節性T細胞、輔助性T細胞17和活化樹突細胞相關度較高。巨噬細胞在ALI/ARDS扮演了十分重要的角色,在ALI/ARDS急性期,巨噬細胞通常從交替活化表型(M2)轉變為經典活化表型(M1),并釋放各種強效促炎介質。在后期,巨噬細胞則會從M1表型交替回M2表型,以消除凋亡細胞并參與纖維化[27]。有研究表明,LPS可使中性粒細胞產生中性粒細胞外陷阱(neutrophil extracellular traps,NETs),而NETs可加劇肺組織損傷以及炎癥[28-29]。調節性T細胞被證實可以促進組織修復,并且可以調節肺部炎癥中的Th免疫應答[30]。輔助性T細胞17被證明可能通過產生白細胞介素(interleukin,IL)-17和IL-22來引起炎癥并介導ALI[31],但是具體分化機制仍不清楚。
ALI/ARDS可由多種重癥引起,包括但不限于感染、膠原血管疾病、免疫介導的肺出血等[32]。大多數ALI/ARDS患者因全身炎癥反應死于多器官功能障礙綜合征[33]。在此過程中免疫細胞及其分泌的細胞因子起著重要作用[34]。本研究DEGs的富集分析表明這些DEGs與機體免疫高度相關,包括GSEA富集的先天免疫反應與KEGG富集的TNF、IL-17、Toll樣受體(Toll-like receptors,TLR)等信號通路,其中TNF為促炎因子信號通路;IL-17被證實參與ALI/ARDS的發病;TLR可誘導炎癥反應導致ALI[32,35]。
綜上所述,Gpx2與Ifi44具有潛在的免疫調節能力,可作為LPS誘導ALI的小鼠模型治療的潛在生物標志物,可以為探索ALI機制和潛在靶點提供新的方向。但是本研究仍存在一定的局限性,因為研究是基于公共數據庫的小鼠數據進行挖掘,同時還存在納入樣本量偏少的問題,對研究結果的準確性存在一定影響。這些生物標志物需要進一步的擴大樣本研究以及體內外實驗加以驗證。
利益沖突:本研究不涉及任何利益沖突。