引用本文: 朱巖, 蘭美娟, 梁江淑淵, 蔡凌云, 郭璐瑤, 顧培培, 曾妃. 肺移植受者發生吞咽障礙危險因素的Meta分析和系統評價. 中國呼吸與危重監護雜志, 2024, 23(10): 719-726. doi: 10.7507/1671-6205.202406095 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
吞咽障礙是指多種原因導致口腔、咽喉、食管等部位結構或功能受損,不能將食物或液體送入胃中的過程,獲得性吞咽障礙則是由于疾病治療等醫源性因素導致的吞咽困難[1]。肺移植手術的風險較高,吞咽障礙是肺移植術后嚴重的并發癥之一[2]。近年來,肺移植受者吞咽障礙的發生率逐年升高,其發生率在不同研究中差異較大,為24%~84%[3]。吞咽障礙給肺移植受者帶來誤吸、反流等風險的同時,還會延長住院時間,增加死亡率,而通過早期的識別和干預可降低誤吸、肺炎的發生率[4]。早期識別肺移植受者吞咽障礙的危險因素,制定針對性的干預措施,對于降低吞咽障礙的發生率,改善患者健康結局意義重大。目前關于肺移植受者并發吞咽障礙危險因素的國內研究證據尚不充足,且國外各研究樣本量差異較大[5-6]。因此,本研究對肺移植術后患者發生吞咽障礙的危險因素進行Meta分析,為肺移植術后吞咽障礙的早期識別和制訂預防、治療、護理措施提供借鑒。本研究已在PROSPERO (CRD42023443466)注冊。
1 資料與方法
1.1 文獻納入與排除標準
納入標準:① 入住肺移植科的肺移植受者;② 單肺或雙肺移植術后;③ 年齡≥18歲;④ 研究內容為發生吞咽障礙的危險因素或預測因素;采用1項及以上吞咽障礙評估工具或診斷標準,包括床旁篩查、改良鋇餐篩查、電視X線透視吞咽功能檢查等;⑤ 結局指標為吞咽障礙的發生率和危險因素;⑥ 研究類型為隊列研究或病例對照研究; 排除標準:① 非英文非中文的研究;② 無明確結局指標的文獻;③ 重復發表的文獻。
1.2 文獻檢索策略
檢索中國知網、維普數據庫、萬方數據庫、中國生物醫學文獻數據庫、PubMed、Cochrane Library、Embase、CINAHL、Web of Science、Scopus、ProQuest數據庫中關于肺移植術后吞咽障礙危險因素的文獻,并對納入文獻的參考文獻進行追溯檢索。檢索時限為建庫至2023年7月。使用主題詞結合自由詞制訂檢索策略。中文數據庫以中國知網為例,檢索式:(SU=‘肺移植’ ) AND (SU=‘吞咽困難’ OR SU=‘吞咽障礙’ OR SU=‘吞咽功能’ OR SU=‘吞咽功能障礙’ OR SU=‘吞咽功能減退’ OR SU=‘吞咽功能受損’ OR SU=‘吞咽能力受損’ OR SU=‘吞咽異常’ OR SU=‘吞咽功能異常’ OR SU=‘進食障礙’ OR SU=‘咽下困難’ OR SU=‘咽下障礙’ OR SU=‘吞咽失常’) AND (SU=‘危險因素’ OR SU=‘風險因素’ OR SU=‘影響因素’ OR SU=‘相關因素’ OR SU=‘預測因素’ OR SU=‘高危因素 ’ OR SU=‘病因’ OR SU=‘誘因’ OR SU=‘原因’ OR SU=‘因素’);英文數據庫以PubMed為例,檢索策略見圖1。

1.3 文獻篩選和資料提取
由2名研究者獨立篩選文獻,先剔除重復文獻,再閱讀題目和摘要,排除研究內容、研究類型、研究對象不符合的文獻,閱讀全文,再次復篩。出現意見不一致時由第3名研究者裁決。提取文獻中作者、發表年份、研究地點、研究類型、樣本量、評估工具及危險因素等內容。
1.4 文獻質量評價
由2名研究者采用紐卡斯爾-渥太華量表(the Newcastle-Ottawa Scale,NOS)[2]對文獻進行評價,該量表由3個部分組成,包括研究人群選擇、組間可比性、暴露因素,滿分為9分。總分≥6分的文獻認為文獻質量較高。
1.5 統計學方法
應用Rev Man 5.4和Stata 17.0軟件對提取的數據進行統計分析。本研究中二分類結局變量采用比值比(OR)作為效應量,連續性變量選擇均數差(MD),區間估計用95%可信區間(95%CI)表示。納入研究的異質性采用Q檢驗,若P>0.1 且 I2<50%時,則表示不存在異質性,采用固定效應模型進行分析; 反之,則表示存在異質性,采用隨機效應模型進行分析,顯著性水平為0.05。通過漏斗圖評估發表偏倚,Egger’s Test 對漏斗圖的對稱性進行檢驗,若 P>0.05,意味著漏斗圖對稱,納入研究間不存在發表偏倚。
2 結果
2.1 文獻檢索結果
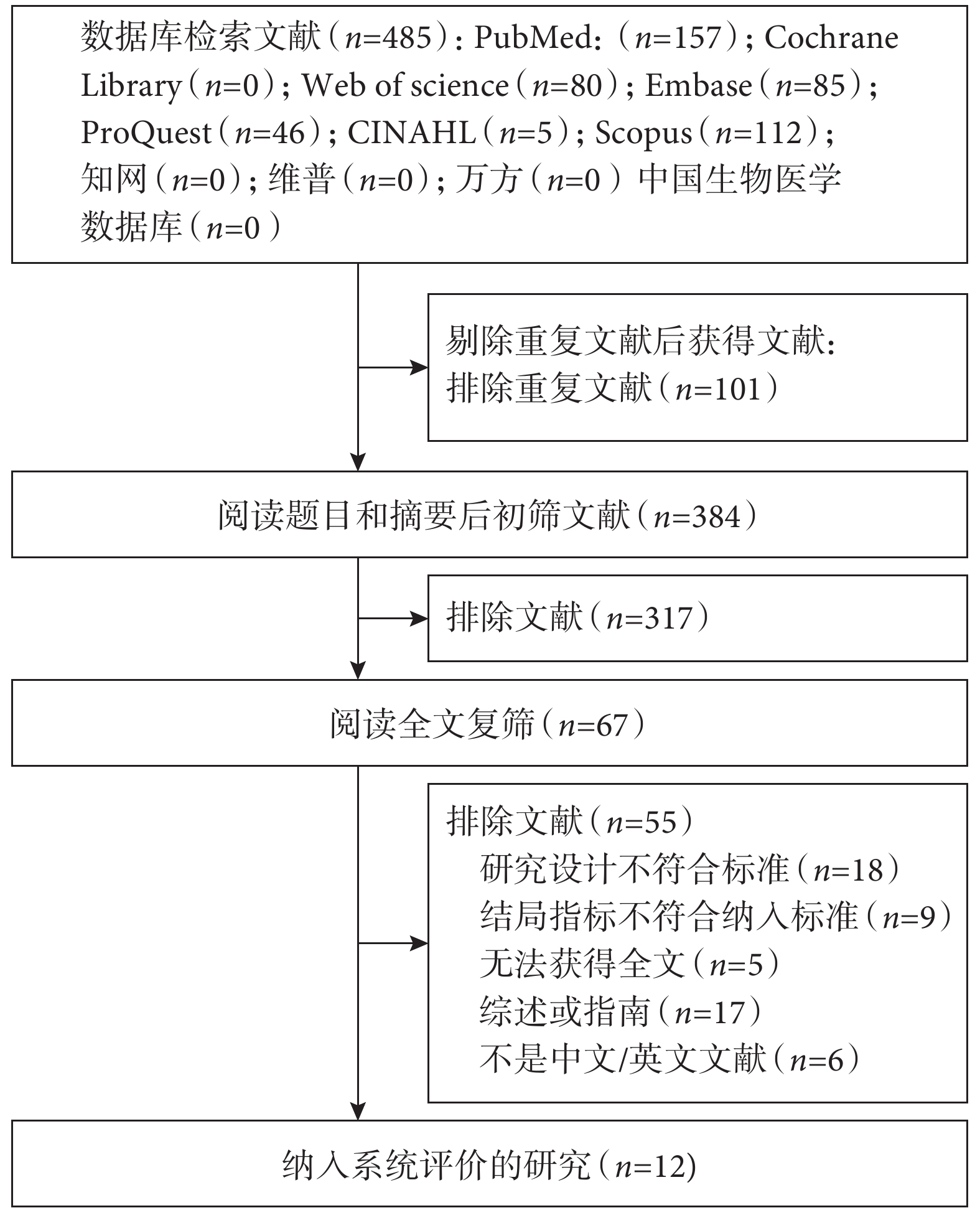
通過檢索文獻共獲得485篇文獻,全部為英文文獻485篇,剔除重復文獻101篇,閱讀題目和摘要后去除文獻317篇,獲取剩余文獻67篇。剔除研究設計不符合標準18篇,結局指標不符合納入指標9篇,無法獲得全文9篇,綜述或指南17篇,不是中文/英文6篇文獻,最終納入 12篇文獻[3,7-17],文獻篩選的流程圖見圖2。
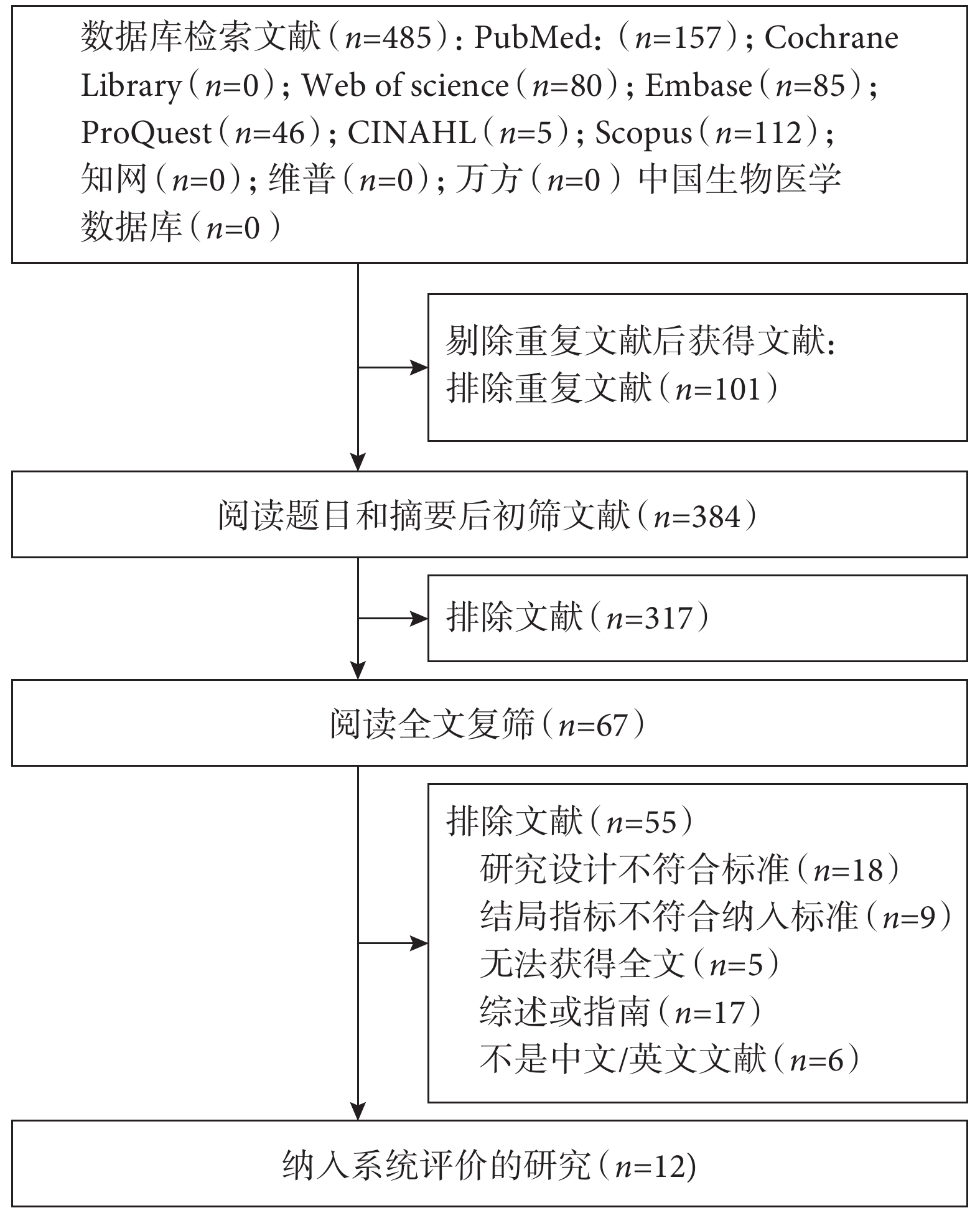 圖2
文獻篩選流程圖
圖2
文獻篩選流程圖
2.2 納入文獻的基本特征及方法學質量評價
納入的12篇文獻中,隊列研究1篇[18],病例對照研究11篇[3,7-16]。合計樣本量為1915例。12篇文獻方法學質量評價得分均≥6分,納入文獻質量較高。納入文獻的基本特征及方法學質量評價見表1。
2.3 Meta分析結果
2.3.1 吞咽障礙的發生率
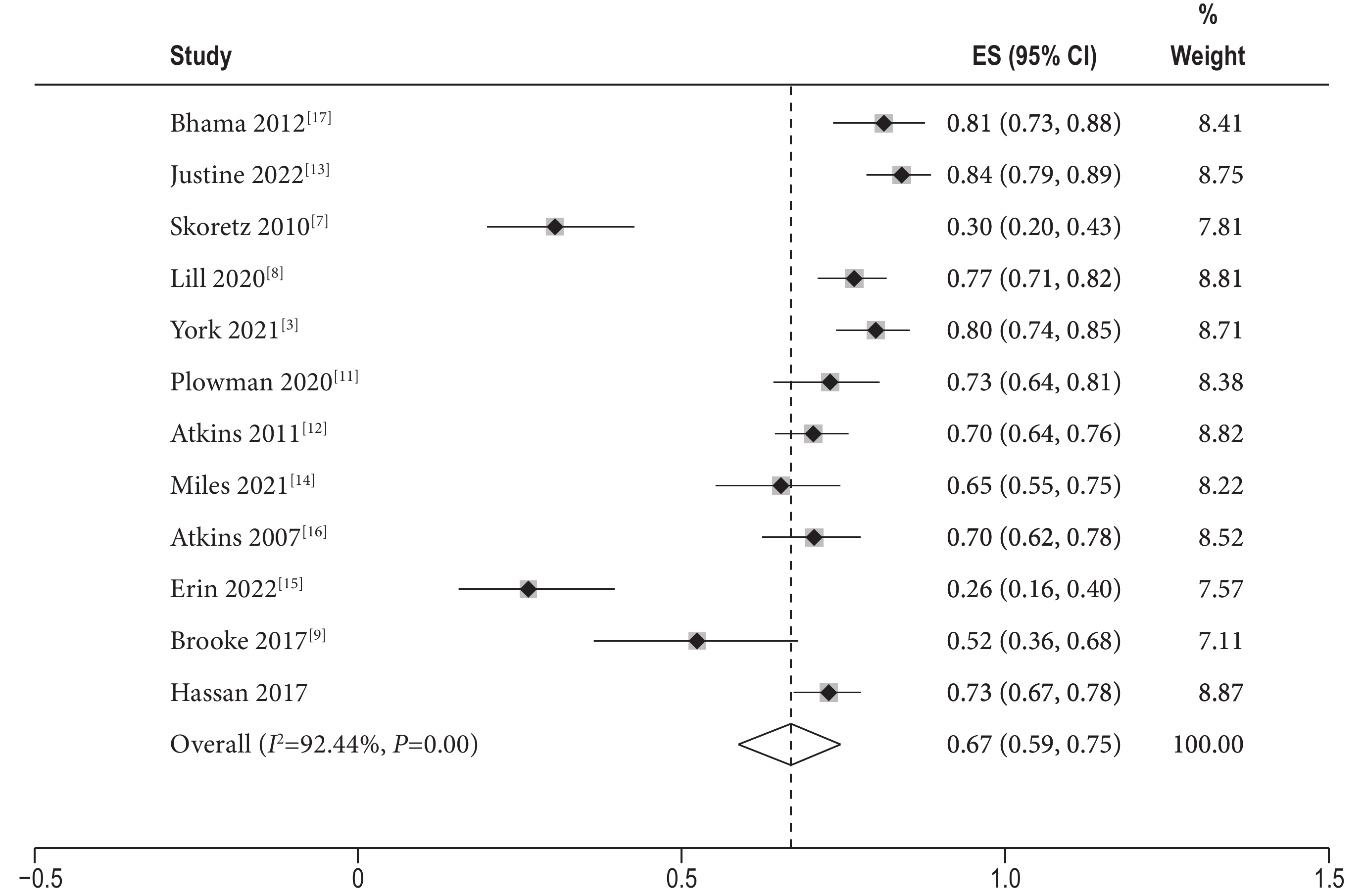
12項研究[3,7-17]報告肺移植受者吞咽障礙的發生率,結果顯示研究間存在異質性,I2=92.44%>50%,且P<0.01,故采用隨機效應進行合并,得到合并后的吞咽障礙的發生率為67%[ES=0.67,95%CI 0.59~0.75]。結果見圖3。
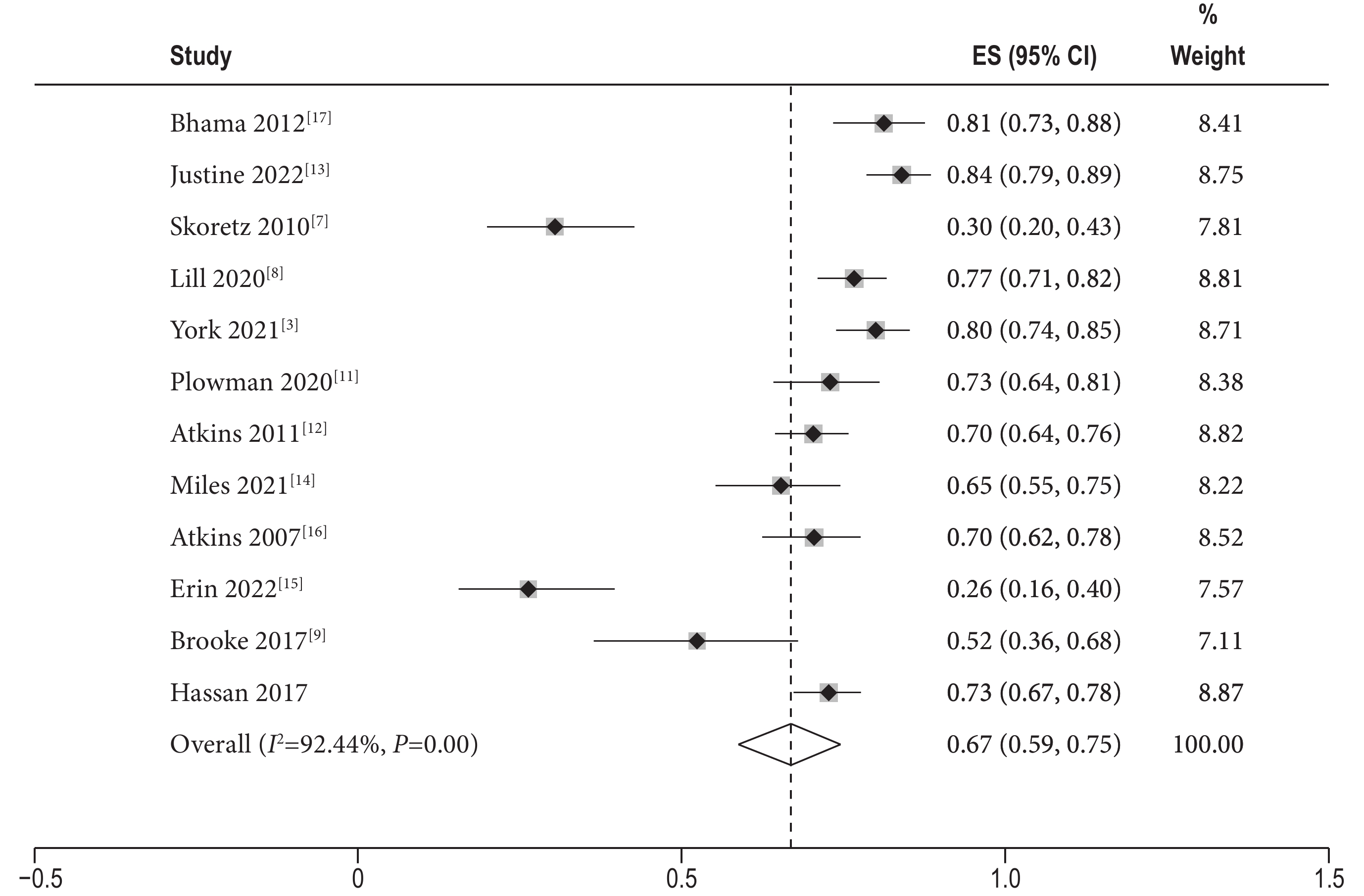 圖3
肺移植受者吞咽障礙的發生率
圖3
肺移植受者吞咽障礙的發生率
2.3.2 危險因素
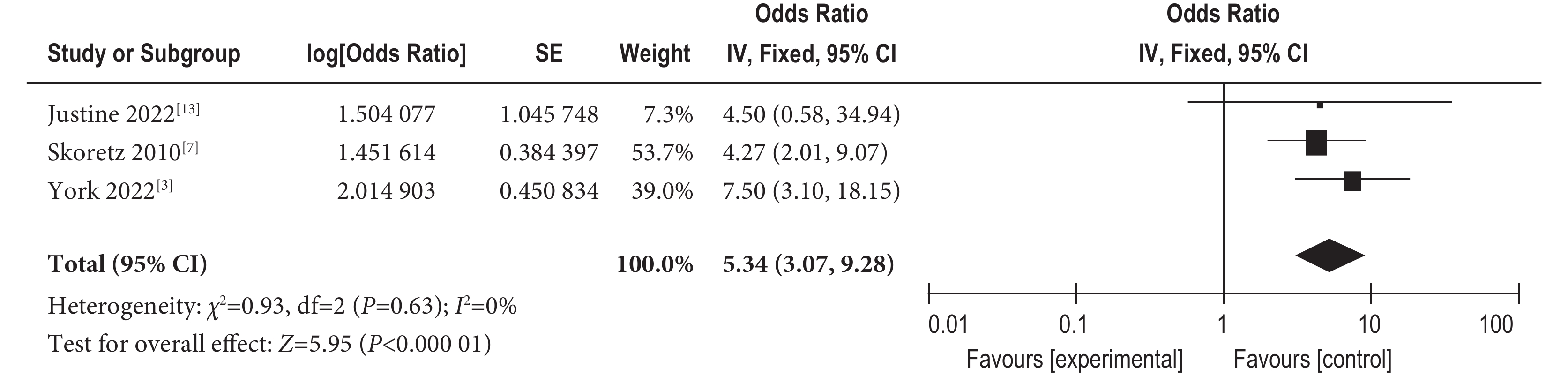
(1)重新插管 3項研究[3,7,13]報告了重新插管對肺移植受者發生吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.63),故采用固定效應進行合并,得到合并后的結果顯示,存在重新插管導致出現吞咽障礙的可能性是沒有重新插管的5.34倍[OR=5.34,95%CI 3.07~9.28,P<0.001]。結果見圖4。
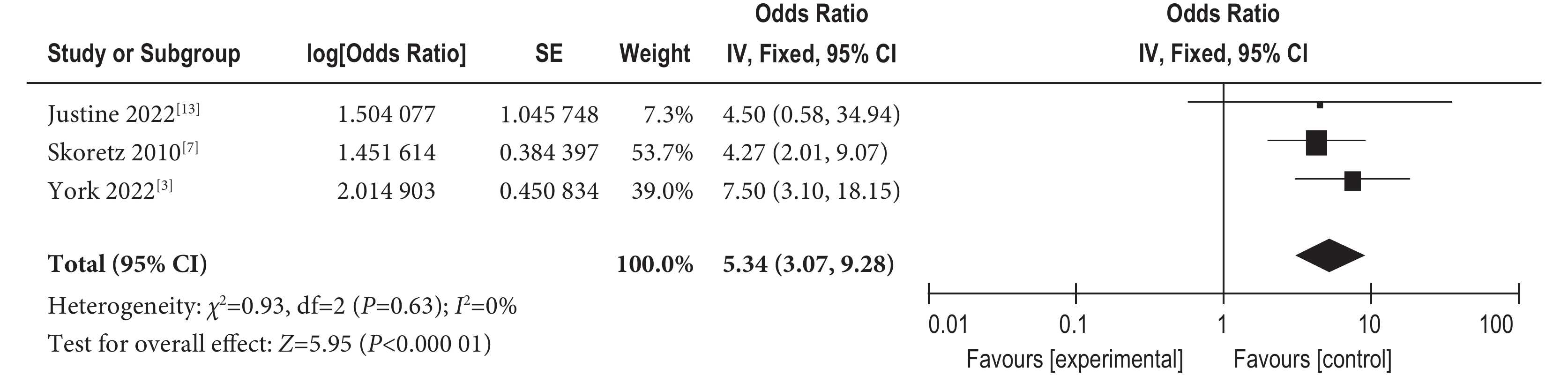 圖4
重新插管對肺移植受者吞咽障礙的影響
圖4
重新插管對肺移植受者吞咽障礙的影響
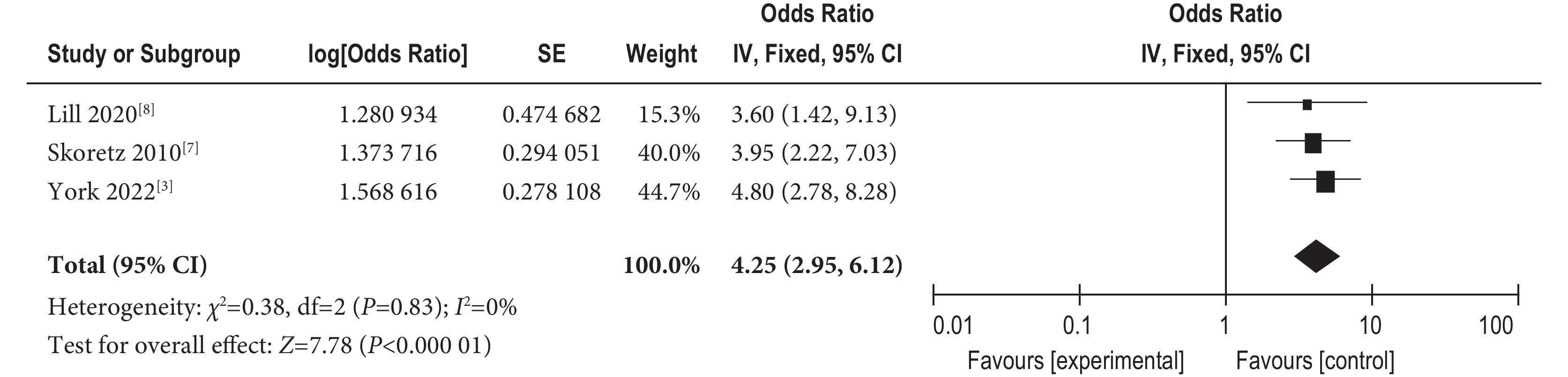
(2)機械通氣3項研究[7,8,13] 報告機械通氣對肺移植受者發生吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.83),故采用固定效應進行合并,得到合并后結果顯示經歷機械通氣導致出現吞咽障礙的可能性是沒有使用機械通氣的4.25倍[OR=4.25,95%CI 2.95~6.12,P<0.001]。結果見圖5。
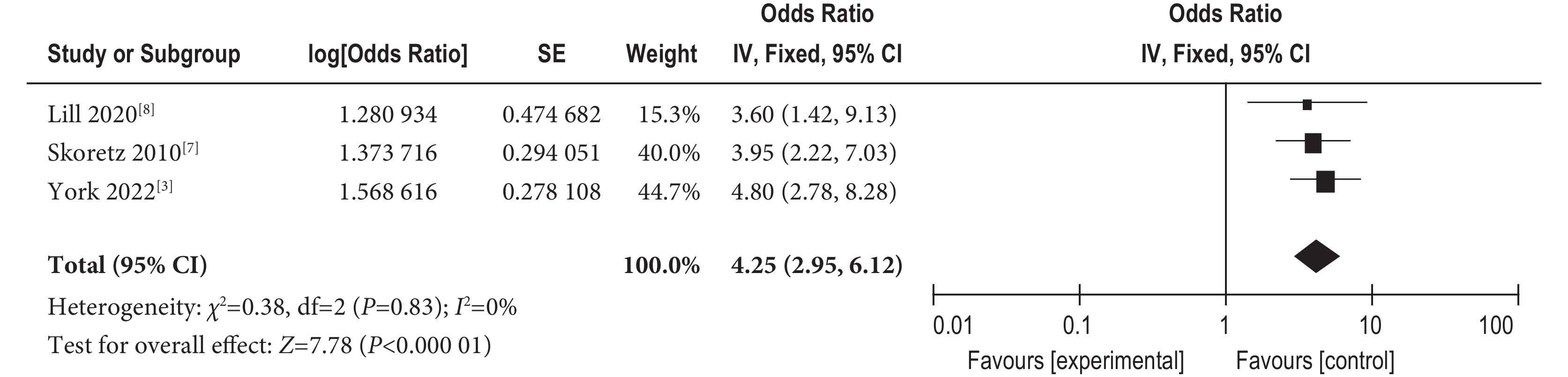 圖5
機械通氣對肺移植受者吞咽障礙的影響
圖5
機械通氣對肺移植受者吞咽障礙的影響
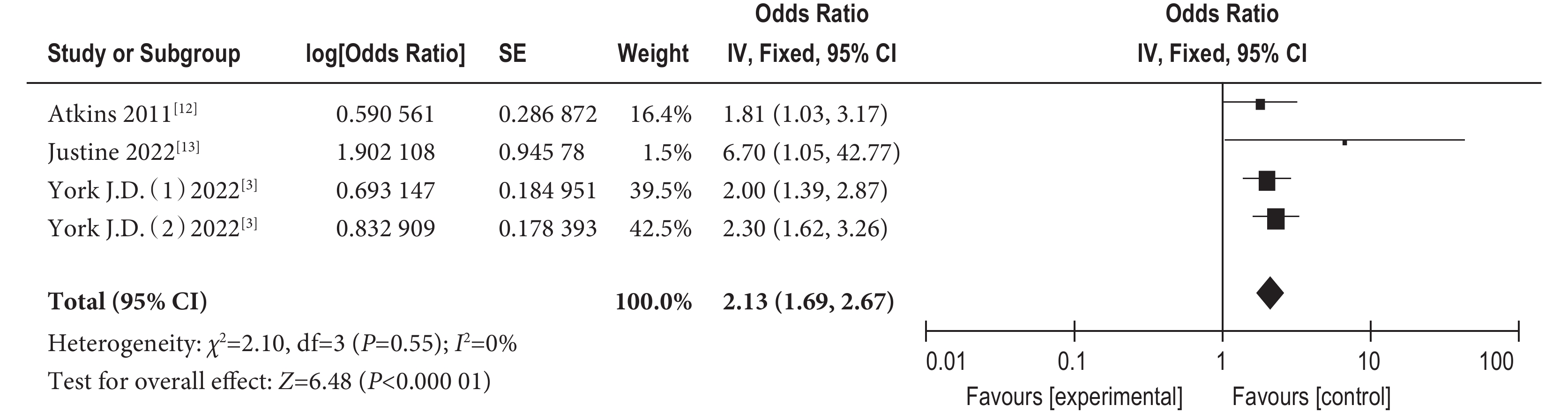
(3)體外生命支持3項研究[3,12-13]報告體外生命支持對吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.55),故采用固定效應進行合并,得到合并后的結果顯示使用體外生命支持導致出現吞咽障礙的可能性是沒有體外生命支持的2.13倍[OR=2.13,95%CI 1.69~2.67,P<0.001]。結果見圖6。
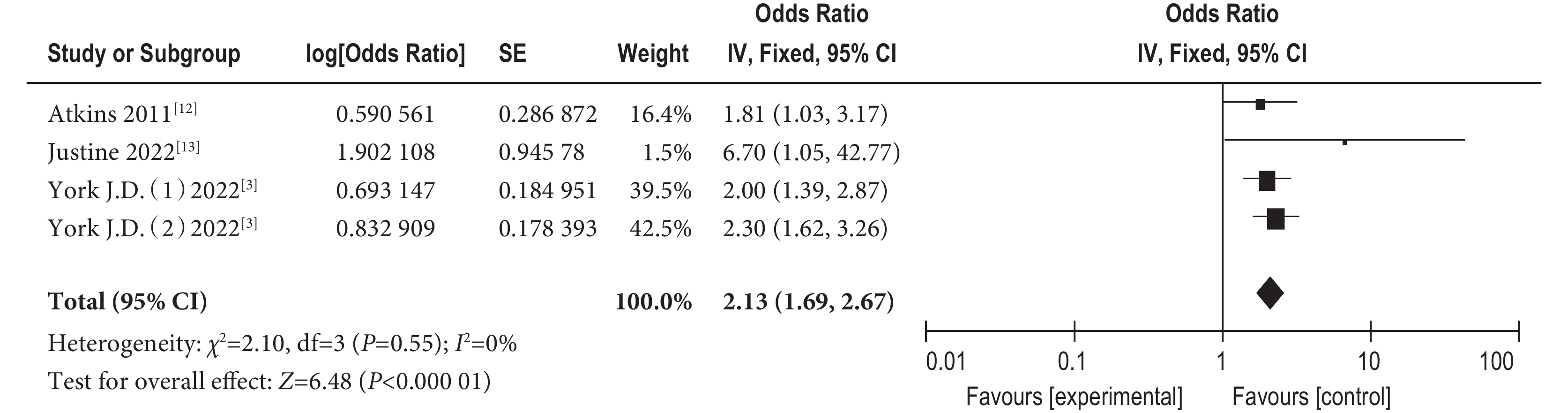 圖6
體外生命支持對肺移植受者吞咽障礙的影響
圖6
體外生命支持對肺移植受者吞咽障礙的影響
2.4 描述性分析結果
本研究發現,有多個因素由于只有單篇文獻報告或數據難以合并,進行描述性分析。其中,用藥方面包括使用5種以上的藥物[14];疾病方面包括聲帶輕癱、胸腔積液、靜脈血栓形成和急性排斥術后并發癥[16]、胃食管反流病、既往心肌梗死[17];其他方面包括住院時間[7]、1年生存率[8]、恢復經口進食時間[11]、年齡[12]、FOIS和IDDSI[15]、女性[17]、體重指數[17]。研究顯示,以上危險因素與肺移植受者發生吞咽障礙呈相關性。
2.5 偏倚檢驗
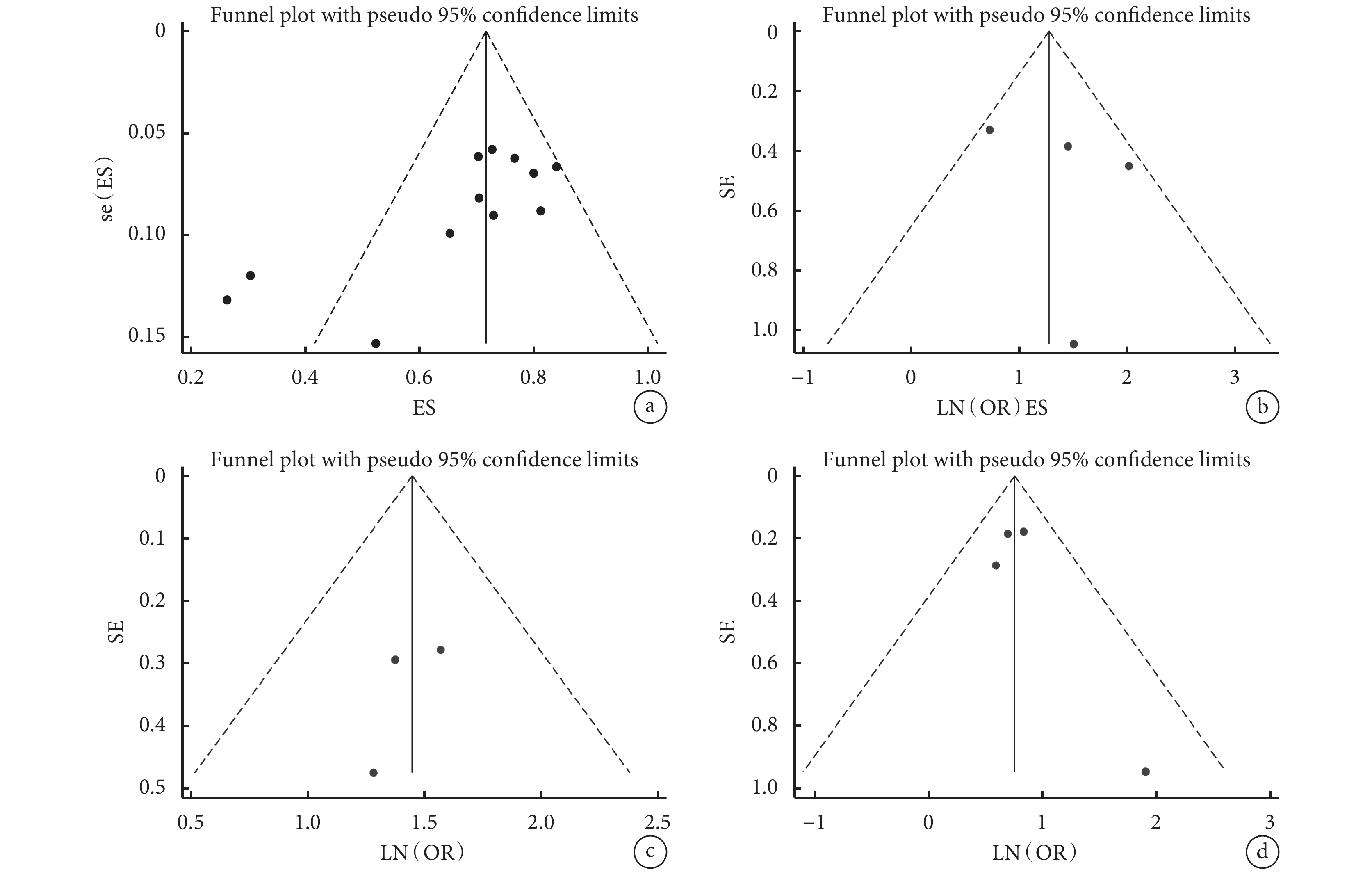
針對肺移植受者發生吞咽障礙的危險因素繪制漏斗圖。結果顯示,吞咽障礙發生率P值小于0.05,說明文獻可能存在發表偏倚。重新插管,機械通氣,體外生命支持的P值全部大于0.05,說明納入文獻不存在發表偏倚。結果見圖7。
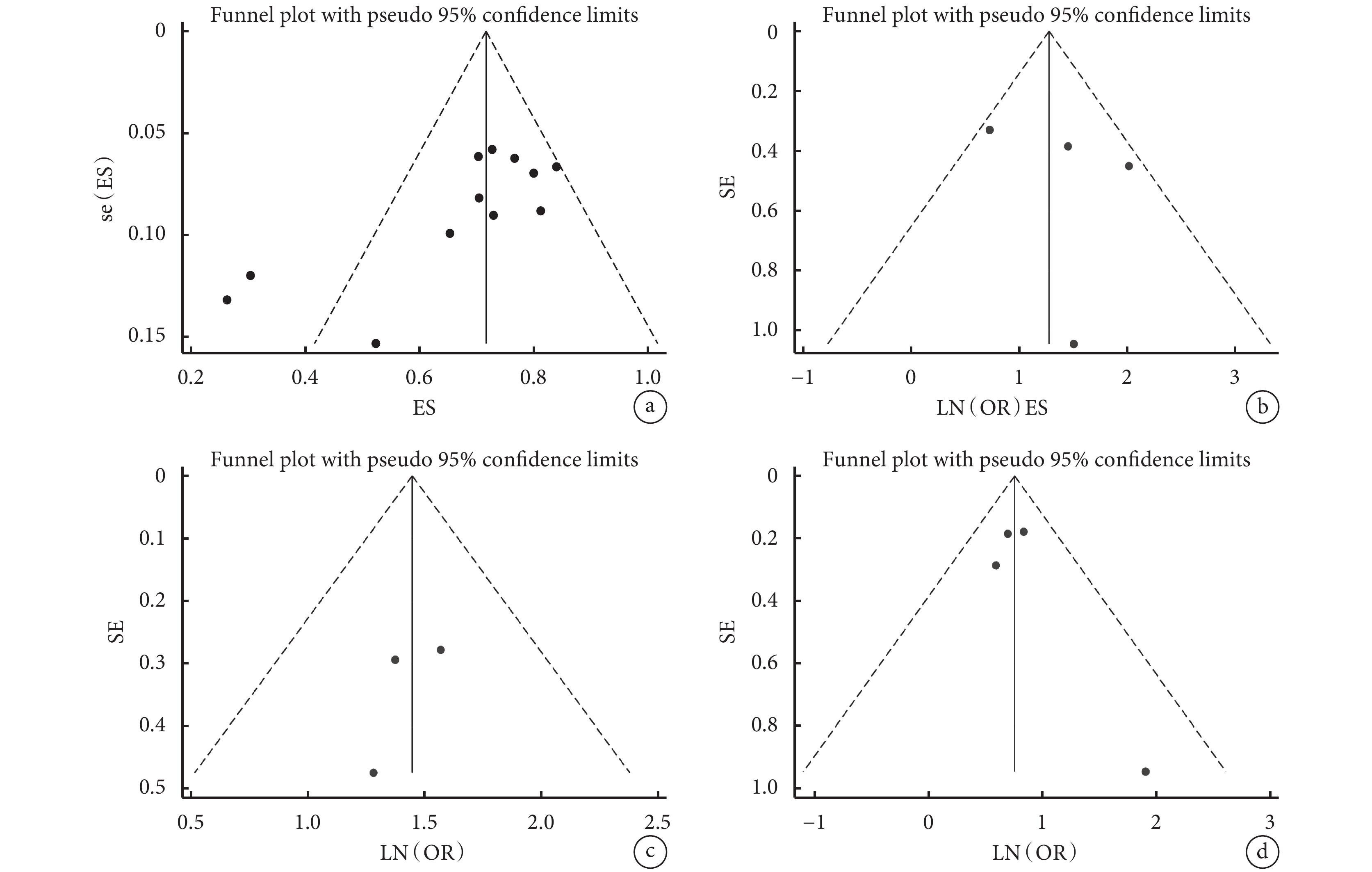 圖7
發生吞咽障礙危險因素的漏斗圖
圖7
發生吞咽障礙危險因素的漏斗圖
注:左上為吞咽障礙發生率的漏斗圖;右上為重新插管的漏斗圖;左下為機械通氣的漏斗圖;右下為體外生命支持的漏斗圖
3 討論
3.1 吞咽障礙是影響肺移植受者預后的重要因素
本研究結果顯示,肺移植后吞咽障礙發生率為67%。吞咽障礙可引起誤吸、反流、咽部食物殘留及口腔分泌物增多等并發癥,同時還可引起住院時間的延長,死亡率的增加。原因為肺迷走神經和喉返神經所支配的喉部的肌肉和感覺,在肺動脈剝離的過程中,易受到術中操作和牽引的損傷[18],也與醫源性因素,例如氣管切開術、長期機械通氣、持續輸注及管飼、行上消化道或支氣管內窺鏡檢查等導致吞咽障礙的發生率增高有關[19-20]。有研究[5]提出,對發生吞咽障礙的肺移植受者進行為期3個月的干預后,肺炎發生率明顯降低。因此,對于肺移植受者不僅僅要篩查與評估有無吞咽障礙,更重要的是評估導致吞咽障礙的風險因素,強調運用團隊合作模式,并進行早期呼吸-吞咽功能的康復訓練。
3.2 重新插管的肺移植受者并發吞咽障礙的風險增高
插管術包括氣管內插管和氣管切開術,而長時間插管已被證實是肺移植受者吞咽障礙的獨立預測因子[21],這2種方法均會破壞肺移植受者口腔及咽喉部正常的生理結構,使其嘴唇、舌部和咽喉出現損傷,從而導致其無法有效地進行吞咽和呼吸功能。研究[22]表明,移植后72小時無法脫離有創機械通氣,或拔管后出現持續的低氧血癥需再次插管。拔管失敗可能是由于吞咽功能障礙導致氣道阻塞,損害患者的咳嗽和咳痰能力。本Meta分析結果顯示,插管每增加1次,肺移植受者吞咽障礙的發生率相應增加了5.34倍。這或許和多次插管會造成口咽部位的反復刺激,導致口咽喉部肌肉醫源性損傷,從而造成咽喉部骨骼肌出現功能障礙。同時管腔反復長期刺激可影響患者呼吸-吞咽協調功能,這反過來又增加了患者拔管失敗的風險[23],造成了惡性循環。在本研究中,重復插管被認為是肺移植受者發生吞咽障礙的獨立危險因素,而重新插管與吞咽障礙的因果關系,需要進一步的研究。
3.3 機械通氣的肺移植受者并發吞咽障礙的風險增高
肺移植患者術后為了改善呼吸功能,促進心肺功能的恢復通常行氣管插管、氣管切開,以及呼吸機進行輔助通氣。本Meta分析結果顯示,長期機械通氣肺移植受者吞咽障礙的發生率相對增加了4.25倍。隨著機械通氣時間延長,患者出現病理性肌肉功能障礙和周圍性神經病變的風險都會增加[24]。機械通氣對吞咽和呼吸功能產生一系列復雜的病理改變,一方面,氣管插管、氣管切開會刺激咽喉部黏膜,導致聲門區解剖結構的改變;另一方面,口咽喉部肌肉長期不活動會出現失用性萎縮,呼吸和吞咽的協調功能減退,進一步導致口咽肌肉無力。長時間插管導致的肌肉無力目前已被認為是咽部功能障礙和誤吸的獨立預測因素[25,26]。此外,這或許還和長期機械通氣期間麻醉鎮靜藥物的使用導致氣道保護反射遲鈍等機制相關聯。脫離機械通氣的吞咽障礙患者早期進行呼吸和吞咽功能的康復訓練,將提高呼吸-吞咽的協調能力,促進肺移植受者吞咽功能的康復[27]。
3.4 體外生命支持的肺移植受者并發吞咽障礙的風險增高
體外生命支持(Extracorporeal life support,ECLS)包括體外循環(Cardiopulmonary bypass ,CPB)及外膜肺氧合(extracorporeal membrane oxygenation,ECMO)。隨著 ECLS 技術的發展,ECMO 作為肺移植橋梁在術中及術后循環支持中的優勢更加突出,幫助受體患者順利度過肺移植窗口期[28]。但當使用機械通氣效果不佳時,ECMO是已越來越多用于肺移植受者搶救治療的一種手段[29]。本Meta分析結果顯示,體外生命支持是肺移植術后患者吞咽障礙的獨立危險因素,與沒有體外生命支持的肺移植受者相比,術后患者吞咽障礙的發生率相對增加了2.13倍。使用體外生命支持的這類患者通常意味著肺移植術后病情更危重,同時體外生命支持伴隨著機械通氣疊加作用,會進一步造成急性恢復期的器官損傷[30,31]。需要體外生命支持的肺移植的受者,會經歷更長的住院時間、更差的身體狀況以及更可能發生ICU獲得性衰弱[32],這或許解釋了肺移植受者發生吞咽障礙的潛在機制。也提示了體外生命支持的使用可以成為預測肺移植受者預后嚴重程度的敏感性指標。Hayanga[33]研究顯示,使用ECMO橋接的肺移植患者比不需要此類支持的患者1年生存率低,即便如此,目前ECMO仍然是肺移植術后唯一的搶救方式。
3.5 局限性
目前國內外關于肺移植受者并發吞咽障礙危險因素的高質量研究較少, 能夠納入Meta分析的文獻數量亦較少,無法全面評估肺移植手術發生吞咽障礙的危險因素。 在研究中還發現肺移植患者既往心肌梗死、心腦血管病史及胃食管反流病[34]等對肺移植受者并發吞咽障礙可能也有一定的影響,但因納入文獻數不足或數據類型不同無法合并分析。此外,納入文獻全部為英文文獻,國內吞咽障礙相關的肺移植研究還處于起步階段。不同類型研究其樣本量大小、病例選擇等會存在差異,可能導致研究間存在異質性,對研究結果產生一定的影響,后期可開展控制混雜因素的前瞻性研究來更全面、更科學地評估肺移植受者并發吞咽障礙的危險因素。
本研究發現,肺移植受者吞咽障礙的發生率為67%,受到重新插管、機械通氣及體外生命支持等多種因素影響。重新插管次數越多、存在機械通氣及體外生命支持的肺移植受者,更易發生吞咽障礙,護理人員可結合危險因素,早期識別并制定干預措施,降低肺移植受者吞咽障礙的發生率。未來研究中還需要根據危險因素,構建風險預測模型,積極制定干預方案,開展多中心、大樣本的隨機對照試驗,為肺移植受者吞咽障礙的早期識別和干預提供理論和實踐依據。
利益沖突:本研究不涉及任何利益沖突。
吞咽障礙是指多種原因導致口腔、咽喉、食管等部位結構或功能受損,不能將食物或液體送入胃中的過程,獲得性吞咽障礙則是由于疾病治療等醫源性因素導致的吞咽困難[1]。肺移植手術的風險較高,吞咽障礙是肺移植術后嚴重的并發癥之一[2]。近年來,肺移植受者吞咽障礙的發生率逐年升高,其發生率在不同研究中差異較大,為24%~84%[3]。吞咽障礙給肺移植受者帶來誤吸、反流等風險的同時,還會延長住院時間,增加死亡率,而通過早期的識別和干預可降低誤吸、肺炎的發生率[4]。早期識別肺移植受者吞咽障礙的危險因素,制定針對性的干預措施,對于降低吞咽障礙的發生率,改善患者健康結局意義重大。目前關于肺移植受者并發吞咽障礙危險因素的國內研究證據尚不充足,且國外各研究樣本量差異較大[5-6]。因此,本研究對肺移植術后患者發生吞咽障礙的危險因素進行Meta分析,為肺移植術后吞咽障礙的早期識別和制訂預防、治療、護理措施提供借鑒。本研究已在PROSPERO (CRD42023443466)注冊。
1 資料與方法
1.1 文獻納入與排除標準
納入標準:① 入住肺移植科的肺移植受者;② 單肺或雙肺移植術后;③ 年齡≥18歲;④ 研究內容為發生吞咽障礙的危險因素或預測因素;采用1項及以上吞咽障礙評估工具或診斷標準,包括床旁篩查、改良鋇餐篩查、電視X線透視吞咽功能檢查等;⑤ 結局指標為吞咽障礙的發生率和危險因素;⑥ 研究類型為隊列研究或病例對照研究; 排除標準:① 非英文非中文的研究;② 無明確結局指標的文獻;③ 重復發表的文獻。
1.2 文獻檢索策略
檢索中國知網、維普數據庫、萬方數據庫、中國生物醫學文獻數據庫、PubMed、Cochrane Library、Embase、CINAHL、Web of Science、Scopus、ProQuest數據庫中關于肺移植術后吞咽障礙危險因素的文獻,并對納入文獻的參考文獻進行追溯檢索。檢索時限為建庫至2023年7月。使用主題詞結合自由詞制訂檢索策略。中文數據庫以中國知網為例,檢索式:(SU=‘肺移植’ ) AND (SU=‘吞咽困難’ OR SU=‘吞咽障礙’ OR SU=‘吞咽功能’ OR SU=‘吞咽功能障礙’ OR SU=‘吞咽功能減退’ OR SU=‘吞咽功能受損’ OR SU=‘吞咽能力受損’ OR SU=‘吞咽異常’ OR SU=‘吞咽功能異常’ OR SU=‘進食障礙’ OR SU=‘咽下困難’ OR SU=‘咽下障礙’ OR SU=‘吞咽失常’) AND (SU=‘危險因素’ OR SU=‘風險因素’ OR SU=‘影響因素’ OR SU=‘相關因素’ OR SU=‘預測因素’ OR SU=‘高危因素 ’ OR SU=‘病因’ OR SU=‘誘因’ OR SU=‘原因’ OR SU=‘因素’);英文數據庫以PubMed為例,檢索策略見圖1。

1.3 文獻篩選和資料提取
由2名研究者獨立篩選文獻,先剔除重復文獻,再閱讀題目和摘要,排除研究內容、研究類型、研究對象不符合的文獻,閱讀全文,再次復篩。出現意見不一致時由第3名研究者裁決。提取文獻中作者、發表年份、研究地點、研究類型、樣本量、評估工具及危險因素等內容。
1.4 文獻質量評價
由2名研究者采用紐卡斯爾-渥太華量表(the Newcastle-Ottawa Scale,NOS)[2]對文獻進行評價,該量表由3個部分組成,包括研究人群選擇、組間可比性、暴露因素,滿分為9分。總分≥6分的文獻認為文獻質量較高。
1.5 統計學方法
應用Rev Man 5.4和Stata 17.0軟件對提取的數據進行統計分析。本研究中二分類結局變量采用比值比(OR)作為效應量,連續性變量選擇均數差(MD),區間估計用95%可信區間(95%CI)表示。納入研究的異質性采用Q檢驗,若P>0.1 且 I2<50%時,則表示不存在異質性,采用固定效應模型進行分析; 反之,則表示存在異質性,采用隨機效應模型進行分析,顯著性水平為0.05。通過漏斗圖評估發表偏倚,Egger’s Test 對漏斗圖的對稱性進行檢驗,若 P>0.05,意味著漏斗圖對稱,納入研究間不存在發表偏倚。
2 結果
2.1 文獻檢索結果
通過檢索文獻共獲得485篇文獻,全部為英文文獻485篇,剔除重復文獻101篇,閱讀題目和摘要后去除文獻317篇,獲取剩余文獻67篇。剔除研究設計不符合標準18篇,結局指標不符合納入指標9篇,無法獲得全文9篇,綜述或指南17篇,不是中文/英文6篇文獻,最終納入 12篇文獻[3,7-17],文獻篩選的流程圖見圖2。
 圖2
文獻篩選流程圖
圖2
文獻篩選流程圖
2.2 納入文獻的基本特征及方法學質量評價
納入的12篇文獻中,隊列研究1篇[18],病例對照研究11篇[3,7-16]。合計樣本量為1915例。12篇文獻方法學質量評價得分均≥6分,納入文獻質量較高。納入文獻的基本特征及方法學質量評價見表1。
2.3 Meta分析結果
2.3.1 吞咽障礙的發生率
12項研究[3,7-17]報告肺移植受者吞咽障礙的發生率,結果顯示研究間存在異質性,I2=92.44%>50%,且P<0.01,故采用隨機效應進行合并,得到合并后的吞咽障礙的發生率為67%[ES=0.67,95%CI 0.59~0.75]。結果見圖3。
 圖3
肺移植受者吞咽障礙的發生率
圖3
肺移植受者吞咽障礙的發生率
2.3.2 危險因素
(1)重新插管 3項研究[3,7,13]報告了重新插管對肺移植受者發生吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.63),故采用固定效應進行合并,得到合并后的結果顯示,存在重新插管導致出現吞咽障礙的可能性是沒有重新插管的5.34倍[OR=5.34,95%CI 3.07~9.28,P<0.001]。結果見圖4。
 圖4
重新插管對肺移植受者吞咽障礙的影響
圖4
重新插管對肺移植受者吞咽障礙的影響
(2)機械通氣3項研究[7,8,13] 報告機械通氣對肺移植受者發生吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.83),故采用固定效應進行合并,得到合并后結果顯示經歷機械通氣導致出現吞咽障礙的可能性是沒有使用機械通氣的4.25倍[OR=4.25,95%CI 2.95~6.12,P<0.001]。結果見圖5。
 圖5
機械通氣對肺移植受者吞咽障礙的影響
圖5
機械通氣對肺移植受者吞咽障礙的影響
(3)體外生命支持3項研究[3,12-13]報告體外生命支持對吞咽障礙的影響,結果顯示研究間不存在異質性(I2=0%,P=0.55),故采用固定效應進行合并,得到合并后的結果顯示使用體外生命支持導致出現吞咽障礙的可能性是沒有體外生命支持的2.13倍[OR=2.13,95%CI 1.69~2.67,P<0.001]。結果見圖6。
 圖6
體外生命支持對肺移植受者吞咽障礙的影響
圖6
體外生命支持對肺移植受者吞咽障礙的影響
2.4 描述性分析結果
本研究發現,有多個因素由于只有單篇文獻報告或數據難以合并,進行描述性分析。其中,用藥方面包括使用5種以上的藥物[14];疾病方面包括聲帶輕癱、胸腔積液、靜脈血栓形成和急性排斥術后并發癥[16]、胃食管反流病、既往心肌梗死[17];其他方面包括住院時間[7]、1年生存率[8]、恢復經口進食時間[11]、年齡[12]、FOIS和IDDSI[15]、女性[17]、體重指數[17]。研究顯示,以上危險因素與肺移植受者發生吞咽障礙呈相關性。
2.5 偏倚檢驗
針對肺移植受者發生吞咽障礙的危險因素繪制漏斗圖。結果顯示,吞咽障礙發生率P值小于0.05,說明文獻可能存在發表偏倚。重新插管,機械通氣,體外生命支持的P值全部大于0.05,說明納入文獻不存在發表偏倚。結果見圖7。
 圖7
發生吞咽障礙危險因素的漏斗圖
圖7
發生吞咽障礙危險因素的漏斗圖
注:左上為吞咽障礙發生率的漏斗圖;右上為重新插管的漏斗圖;左下為機械通氣的漏斗圖;右下為體外生命支持的漏斗圖
3 討論
3.1 吞咽障礙是影響肺移植受者預后的重要因素
本研究結果顯示,肺移植后吞咽障礙發生率為67%。吞咽障礙可引起誤吸、反流、咽部食物殘留及口腔分泌物增多等并發癥,同時還可引起住院時間的延長,死亡率的增加。原因為肺迷走神經和喉返神經所支配的喉部的肌肉和感覺,在肺動脈剝離的過程中,易受到術中操作和牽引的損傷[18],也與醫源性因素,例如氣管切開術、長期機械通氣、持續輸注及管飼、行上消化道或支氣管內窺鏡檢查等導致吞咽障礙的發生率增高有關[19-20]。有研究[5]提出,對發生吞咽障礙的肺移植受者進行為期3個月的干預后,肺炎發生率明顯降低。因此,對于肺移植受者不僅僅要篩查與評估有無吞咽障礙,更重要的是評估導致吞咽障礙的風險因素,強調運用團隊合作模式,并進行早期呼吸-吞咽功能的康復訓練。
3.2 重新插管的肺移植受者并發吞咽障礙的風險增高
插管術包括氣管內插管和氣管切開術,而長時間插管已被證實是肺移植受者吞咽障礙的獨立預測因子[21],這2種方法均會破壞肺移植受者口腔及咽喉部正常的生理結構,使其嘴唇、舌部和咽喉出現損傷,從而導致其無法有效地進行吞咽和呼吸功能。研究[22]表明,移植后72小時無法脫離有創機械通氣,或拔管后出現持續的低氧血癥需再次插管。拔管失敗可能是由于吞咽功能障礙導致氣道阻塞,損害患者的咳嗽和咳痰能力。本Meta分析結果顯示,插管每增加1次,肺移植受者吞咽障礙的發生率相應增加了5.34倍。這或許和多次插管會造成口咽部位的反復刺激,導致口咽喉部肌肉醫源性損傷,從而造成咽喉部骨骼肌出現功能障礙。同時管腔反復長期刺激可影響患者呼吸-吞咽協調功能,這反過來又增加了患者拔管失敗的風險[23],造成了惡性循環。在本研究中,重復插管被認為是肺移植受者發生吞咽障礙的獨立危險因素,而重新插管與吞咽障礙的因果關系,需要進一步的研究。
3.3 機械通氣的肺移植受者并發吞咽障礙的風險增高
肺移植患者術后為了改善呼吸功能,促進心肺功能的恢復通常行氣管插管、氣管切開,以及呼吸機進行輔助通氣。本Meta分析結果顯示,長期機械通氣肺移植受者吞咽障礙的發生率相對增加了4.25倍。隨著機械通氣時間延長,患者出現病理性肌肉功能障礙和周圍性神經病變的風險都會增加[24]。機械通氣對吞咽和呼吸功能產生一系列復雜的病理改變,一方面,氣管插管、氣管切開會刺激咽喉部黏膜,導致聲門區解剖結構的改變;另一方面,口咽喉部肌肉長期不活動會出現失用性萎縮,呼吸和吞咽的協調功能減退,進一步導致口咽肌肉無力。長時間插管導致的肌肉無力目前已被認為是咽部功能障礙和誤吸的獨立預測因素[25,26]。此外,這或許還和長期機械通氣期間麻醉鎮靜藥物的使用導致氣道保護反射遲鈍等機制相關聯。脫離機械通氣的吞咽障礙患者早期進行呼吸和吞咽功能的康復訓練,將提高呼吸-吞咽的協調能力,促進肺移植受者吞咽功能的康復[27]。
3.4 體外生命支持的肺移植受者并發吞咽障礙的風險增高
體外生命支持(Extracorporeal life support,ECLS)包括體外循環(Cardiopulmonary bypass ,CPB)及外膜肺氧合(extracorporeal membrane oxygenation,ECMO)。隨著 ECLS 技術的發展,ECMO 作為肺移植橋梁在術中及術后循環支持中的優勢更加突出,幫助受體患者順利度過肺移植窗口期[28]。但當使用機械通氣效果不佳時,ECMO是已越來越多用于肺移植受者搶救治療的一種手段[29]。本Meta分析結果顯示,體外生命支持是肺移植術后患者吞咽障礙的獨立危險因素,與沒有體外生命支持的肺移植受者相比,術后患者吞咽障礙的發生率相對增加了2.13倍。使用體外生命支持的這類患者通常意味著肺移植術后病情更危重,同時體外生命支持伴隨著機械通氣疊加作用,會進一步造成急性恢復期的器官損傷[30,31]。需要體外生命支持的肺移植的受者,會經歷更長的住院時間、更差的身體狀況以及更可能發生ICU獲得性衰弱[32],這或許解釋了肺移植受者發生吞咽障礙的潛在機制。也提示了體外生命支持的使用可以成為預測肺移植受者預后嚴重程度的敏感性指標。Hayanga[33]研究顯示,使用ECMO橋接的肺移植患者比不需要此類支持的患者1年生存率低,即便如此,目前ECMO仍然是肺移植術后唯一的搶救方式。
3.5 局限性
目前國內外關于肺移植受者并發吞咽障礙危險因素的高質量研究較少, 能夠納入Meta分析的文獻數量亦較少,無法全面評估肺移植手術發生吞咽障礙的危險因素。 在研究中還發現肺移植患者既往心肌梗死、心腦血管病史及胃食管反流病[34]等對肺移植受者并發吞咽障礙可能也有一定的影響,但因納入文獻數不足或數據類型不同無法合并分析。此外,納入文獻全部為英文文獻,國內吞咽障礙相關的肺移植研究還處于起步階段。不同類型研究其樣本量大小、病例選擇等會存在差異,可能導致研究間存在異質性,對研究結果產生一定的影響,后期可開展控制混雜因素的前瞻性研究來更全面、更科學地評估肺移植受者并發吞咽障礙的危險因素。
本研究發現,肺移植受者吞咽障礙的發生率為67%,受到重新插管、機械通氣及體外生命支持等多種因素影響。重新插管次數越多、存在機械通氣及體外生命支持的肺移植受者,更易發生吞咽障礙,護理人員可結合危險因素,早期識別并制定干預措施,降低肺移植受者吞咽障礙的發生率。未來研究中還需要根據危險因素,構建風險預測模型,積極制定干預方案,開展多中心、大樣本的隨機對照試驗,為肺移植受者吞咽障礙的早期識別和干預提供理論和實踐依據。
利益沖突:本研究不涉及任何利益沖突。