引用本文: 傅巍, 蔣尚, 陳蘇衡, 瞿珊珊, 李玉蘭. 琥珀酸誘導小鼠肺泡巨噬細胞極化對高氧上皮間質轉化的影響. 中國呼吸與危重監護雜志, 2025, 24(1): 33-41. doi: 10.7507/1671-6205.202408009 復制
版權信息: ?四川大學華西醫院華西期刊社《中國呼吸與危重監護雜志》版權所有,未經授權不得轉載、改編
氧療是不同急慢性疾病、手術治療和早產相關的低氧血癥的重要步驟[1]。高濃度氧氣會引起高氧性急性肺損傷和病死率的增加[2-4]。高氧急性肺損傷動物模型表現為急性滲出性肺水腫、繼發性纖維組織增生、局部出血和透明膜形成等[5]。肺泡Ⅱ型上皮細胞是高氧介導肺損傷的關鍵靶點[6]。Adamson等[7]提出肺泡Ⅱ型上皮細胞可通過肺內上皮間質轉換變為成纖維細胞,讓我們對肺纖維化的病理有了進一步的理解。高氧肺損傷修復時,殘存的肺泡Ⅱ型上皮細胞可通過上皮間質轉化(epithelial–mesenchymal transition,EMT)機制轉化為成纖維細胞,若EMT增多,則可能發展為肺纖維化[8]。高氧環境下會產生更多的活性氧簇,氧化與抗氧化功能的失衡,發生氧化應激反應,導致組織器官損傷[9-10]。同時高氧還激活機體的細胞凋亡、炎癥反應通道和巨噬細胞,導致細胞凋亡并加劇炎癥反應[11-12]。炎癥、凋亡、組織修復性損傷等因素交織,相互作用共同形成了高氧肺損傷的機制,發生更為嚴重的損傷。巨噬細胞是肺損傷時呼吸系統最豐富的免疫細胞,是炎癥的主要驅動因素[13]。活化的巨噬細胞具有吞噬、消滅病原體和死細胞的能力,并能協調炎癥和愈合過程。根據其活化方式和功能的不同,巨噬細胞可分為兩大極化類型,即M1型(經典活化的巨噬細胞,促炎型)和M2型(交替活化的巨噬細胞,抗炎型)[14-15]。因此,巨噬細胞參與高氧肺組織的破壞,在炎癥過程中發揮重要作用[16]。琥珀酸是宿主和微生物代謝過程中產生的重要代謝物[17],是宿主細胞三羧酸循環的中間體,膳食纖維的發酵過程中也會大量產生琥珀酸。Akram和Connors等[18-19]在機體炎癥和代謝應激部位觀察到了琥珀酸的積累。高氧相關肺損傷后會出現糖酵解、糖酵解儲備和氧化磷酸化等糖代謝異常,影響機體能量供應[20-21]。大量研究支持琥珀酸鹽不僅是代謝的惰性副產物,也在下游細胞反應中發揮積極作用,并且可以作為促炎介質,在調節炎癥終點和解決肺部炎癥方面發揮關鍵作用[22-23]。研究表明,琥珀酸可通過巨噬細胞特異性膜表面受體琥珀酸受體1(succinate receptor 1,GPR91)激活免疫細胞并增強炎癥反應。在腸-肺軸相關研究中,腸道來源的琥珀酸可誘導巨噬細胞極化,加重肺損傷[24]。琥珀酸是否影響高氧造成的肺損傷和肺纖維化,目前未見研究報道。本實驗提出并驗證以下假設:琥珀酸通過誘導巨噬細胞極化,促進高氧誘發的肺上皮EMT,從而促進肺纖維化的形成。
1 材料與方法
1.1 材料與試劑
MLE-12小鼠肺泡上皮細胞,MH-S小鼠肺泡巨噬細胞,琥珀酸(美國Sigma公司),琥珀酸受體抑制劑(SUCNR1-IN-1,美國MCE生物科技公司),CCK-8試劑盒(山東思科捷公司),兔抗[E-鈣黏蛋白(E-cadherin,E-cad)、N-鈣黏蛋白(N-cadherin,N-cad)、波形蛋白(vimentin,Vim)](一抗),辣根過氧化物酶標記的山羊抗兔IgG(二抗)(武漢三鷹生物技術有限公司),Transwell小室(孔徑0.4 μm,美國康寧公司),引物由塞維爾生物工程(上海)股份有限公司合成。酶標儀(iMark,美國BioRad公司),曝光儀(Touch Imager pro,易孛特生命科學有限公司),實時定量PCR儀(StepOne Plus,美國Thermo),流式細胞儀器(CytoFLEX,美國貝克曼)。
1.2 方法
1.2.1 細胞培養
取凍存的MLE-12、MH-S細胞,進行復蘇,分別加入DMEM、RPMI
1.2.2 MLE-12高氧暴露時間篩選
取對數生長期的MLE-12,以1×106/皿鋪于6 cm的細胞培養皿中,分為高氧0 h組(0 h組)、高氧24 h組(24 h組)、高氧48 h組(48 h組)、高氧72 h組(72 h組),置于95% O2的培養箱中孵育不同分組時間。實驗重復3次。
1.2.3 MLE-12和MH-S共培養構建體外高氧肺損傷細胞模型
取對數生長期的MLE-12,以1×105/孔鋪于Transwell下室,分為0 h組、48 h組、與MH-S細胞共培養組(共培養組),將MH-S細胞以1×105/孔鋪于Transwell上室,0 h組、48 h組培養條件如上,共培養組置于95%O2的培養箱中孵育48 h,每組設置3個復孔。
1.2.4 篩選琥珀酸濃度
取MLE-12細胞,調整密度至2×103個/mL,將其接種至96孔板中,每孔加入細胞懸液100 μL。各組分別加入濃度為100 mmol/L、50 mmol/L、25 mmol/L、10 mmol/L、5 mmol/L、2.5 mmol/L、1 mmol/L、500 μmol/L琥珀酸的培養基干預24 h后,加入10 μL CCK-8溶液孵育30 min,使用酶標儀測定各組OD值(450 nm處)。細胞活力(%)=(干預組–空白組)OD值/(對照組–空白組)OD值×100%。實驗重復3次。
1.2.5 RT-qPCR法測定巨噬細胞極化M1、M2相關因子[誘導型一氧化氮合成酶(inducible nitricoxide synthase,iNOS)、CD86、Arg-1、CD206]及GPR91 mRNA相對表達量
將MH-S細胞分為對照組和琥珀酸處理組,對照組常規培養24 h,琥珀酸處理組在對照組基礎上加入上述濃度琥珀酸,采用細胞RNA快速提取試劑盒提取細胞樣本總RNA,NanoDrop檢測RNA的濃度及純度,反轉錄合成模板鏈cDNA,取2 μL反轉錄產物檢測PCR,以β-actin作為內參基因,2–ΔΔCt法計算目的基因相對表達量。實驗重復3次。PCR引物序列見表1。
1.2.6 流式細胞術肺泡巨噬細胞的M1與M2細胞分型與比例分析
–4℃,1 000轉離心5 min,沉淀MH-S細胞,用流式緩沖液重懸(105~106細胞/100 μL),充分混勻,加入APC抗小鼠CD11b抗體作為巨噬細胞共同表面標志;加入PE-Cy7抗小鼠CD86抗體,作為M1型巨噬細胞特異性標志;再加入FITC抗小鼠CD206抗體,作為M2型巨噬細胞特異性標志,室溫孵育30 min,生理鹽水清洗離心,流式細胞儀檢測,并用Flowjo軟件分析檢測結果。
1.2.7 細胞共培養探究琥珀酸的影響
將MLE-12細胞與MH-S細胞在孔徑為0.4 μm的Transwell小室中共培養,分為共培養、琥珀酸處理后共培養組、GPR91抑制劑組(抑制劑組)。共培養組:MLE-12細胞與C組MH-S細胞置于95% O2的培養箱中共培養48 h;琥珀酸處理后共培養組:MLE-12細胞與琥珀酸處理組MH-S細胞置于95% O2的培養箱中共培養48 h;抑制劑組:在琥珀酸處理組基礎上加入GPR91抑制劑(SUCNR1-IN-1)與MLE-12細胞在95% O2的培養箱中共培養48 h。
1.2.8 Western blotting法測定EMT相關蛋白相對表達量
取0 h組、24 h組、48 h組、72 h組、琥珀酸處理后共培養組、共培養組、抑制劑組MLE-12細胞,提取蛋白并進行定量后上樣,進行十二烷基硫酸鈉聚丙烯酰胺凝膠電泳,轉聚偏二氟乙烯膜,封閉90 min后參照抗體說明書加入一定稀釋比例的一抗(E-cad、N-cad、Vim、β-actin),4℃孵育過夜,次日TBST洗滌后加入山羊抗兔IgG二抗,孵育1 h,洗滌3次,最后加入顯影液,使用凝膠成像系統拍照記錄。蛋白灰度值用G表示,蛋白相對表達量=G目的蛋白/G內參蛋白(β-actin)。實驗重復3次。
1.3 統計學方法
采用SPSS 25.0統計學軟件進行數據分析。多組間比較采用One-Way ANOVA方差分析,首先利用Levene法進行方差齊性檢驗,確定方差齊性且整體比較組間差異有統計學意義后進一步作多重比較,多重比較采用LSD法。以P<0.05為差異有統計學意義。采用GraphPad Prism5.0軟件將實驗數據生成統計圖表。
2 結果
2.1 高氧對小鼠肺泡上皮EMT的影響
與0 h相比,24 h、48 h組Vim和N-cad表達量顯著升高,差異有統計學意義(P<0.05),24 h組E-cad表達量顯著升高(P<0.05),48 h組、72 h組E-cad表達量顯著下降(P<0.05),其余各組差異無統計學意義。證明給予小鼠肺泡上皮細胞48 h高濃度氧氣,EMT相關指標均會發生變化。因此,選擇48 h作為后續實驗高氧處理時間。結果見圖1。
 圖1
高氧對小鼠肺泡上皮EMT的影響
圖1
高氧對小鼠肺泡上皮EMT的影響
a. 光學顯微鏡下MLE-12在高氧不同時間變化,隨著高氧時間增加,未分化細胞增多(×100);b. MLE-12不同時間高氧后E-cad、N-cad及Vim蛋白表達水平比較(*
2.2 MH-S對MLE-12細胞EMT的影響
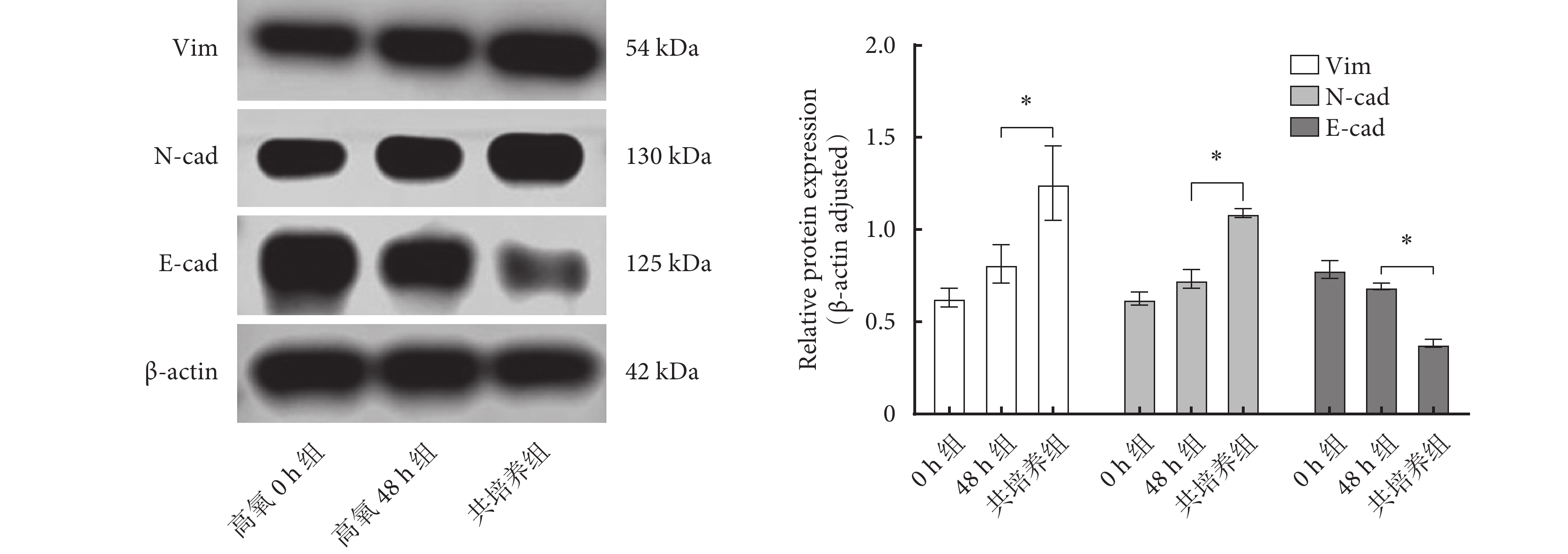
與0 h、48 h相比,共培養組Vim和N-cad表達量顯著升高,E-cad表達量顯著下降,差異有統計學意義(P<0.05)。證明MH-S與MLE-12共培養,MH-S會增強高氧條件下MLE-12細胞EMT。結果見圖2。
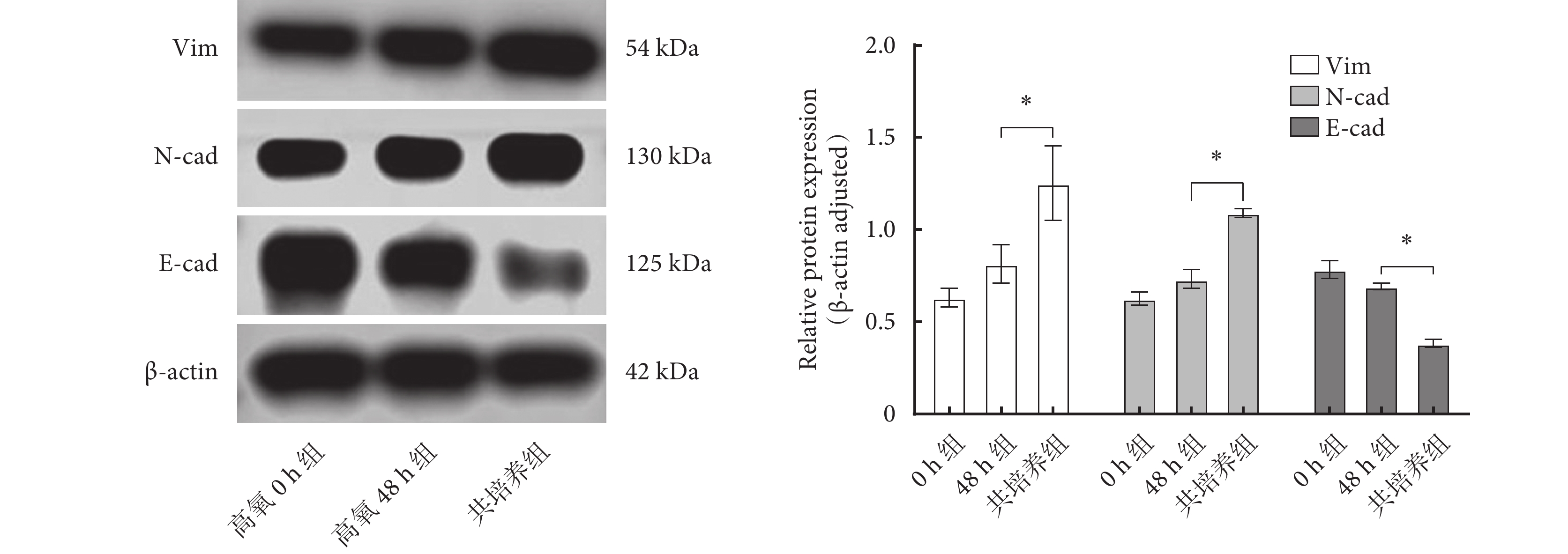 圖2
MLE-12細胞在高氧0 h、高氧48 h以及與MH-S細胞高氧共培養48 h后E-cad、N-cad及Vim蛋白表達水平比較(*P<0.05)
圖2
MLE-12細胞在高氧0 h、高氧48 h以及與MH-S細胞高氧共培養48 h后E-cad、N-cad及Vim蛋白表達水平比較(*P<0.05)
2.3 琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
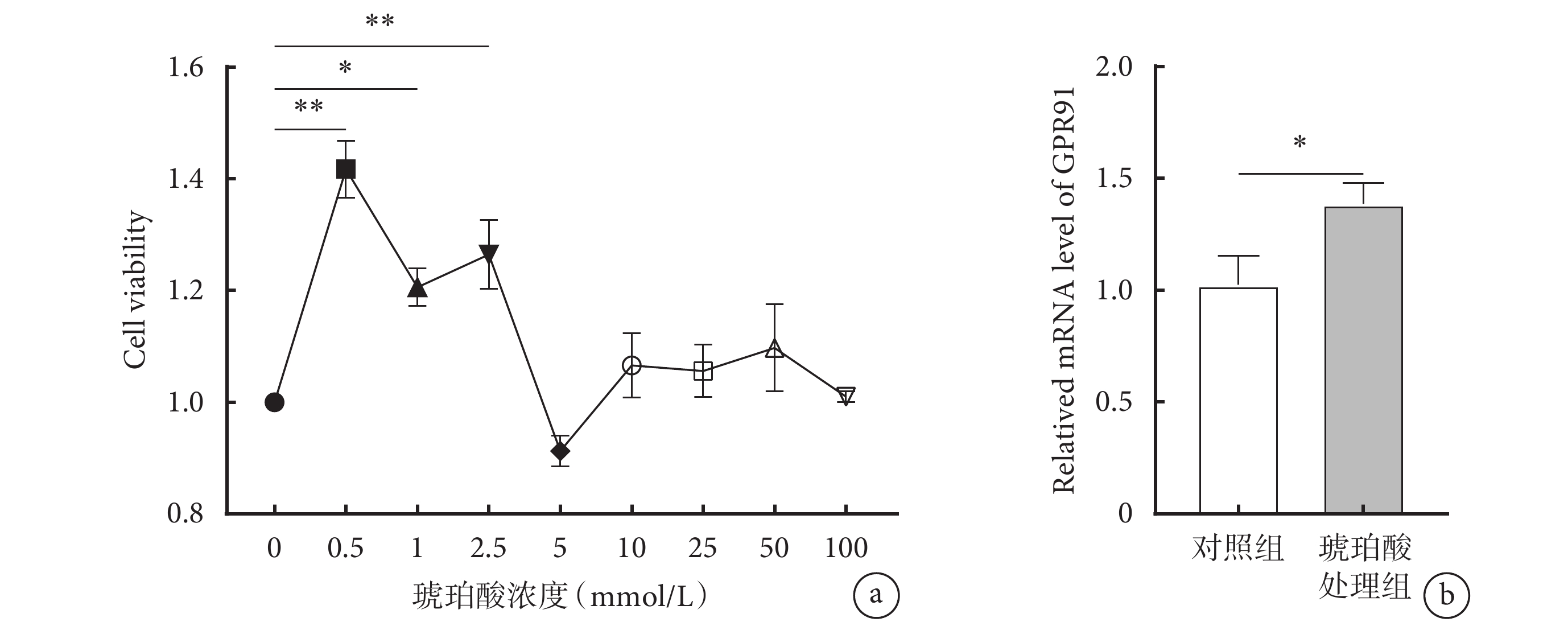
使用不同濃度的琥珀酸干預MLE-12細胞24 h后,各組細胞活力進行比較,與基礎值(0 mmol/L組)相比,100 mmol/L、50 mmol/L、25 mmol/L、10 mmol/L、5 mmol/L組細胞活力差異無統計學意義(P>0.05),2.5 mmol/L、1 mmol/L、500 μmol/L組細胞活力明顯升高(P<0.05)。選取1 mmol/L濃度進行后續實驗。與對照組進行比較,琥珀酸處理組GPR91 mRNA相對表達量顯著升高(P<0.05)。表明1 mmol/L琥珀酸會增加MH-S細胞表面GPR91 mRNA的表達。結果見圖3。
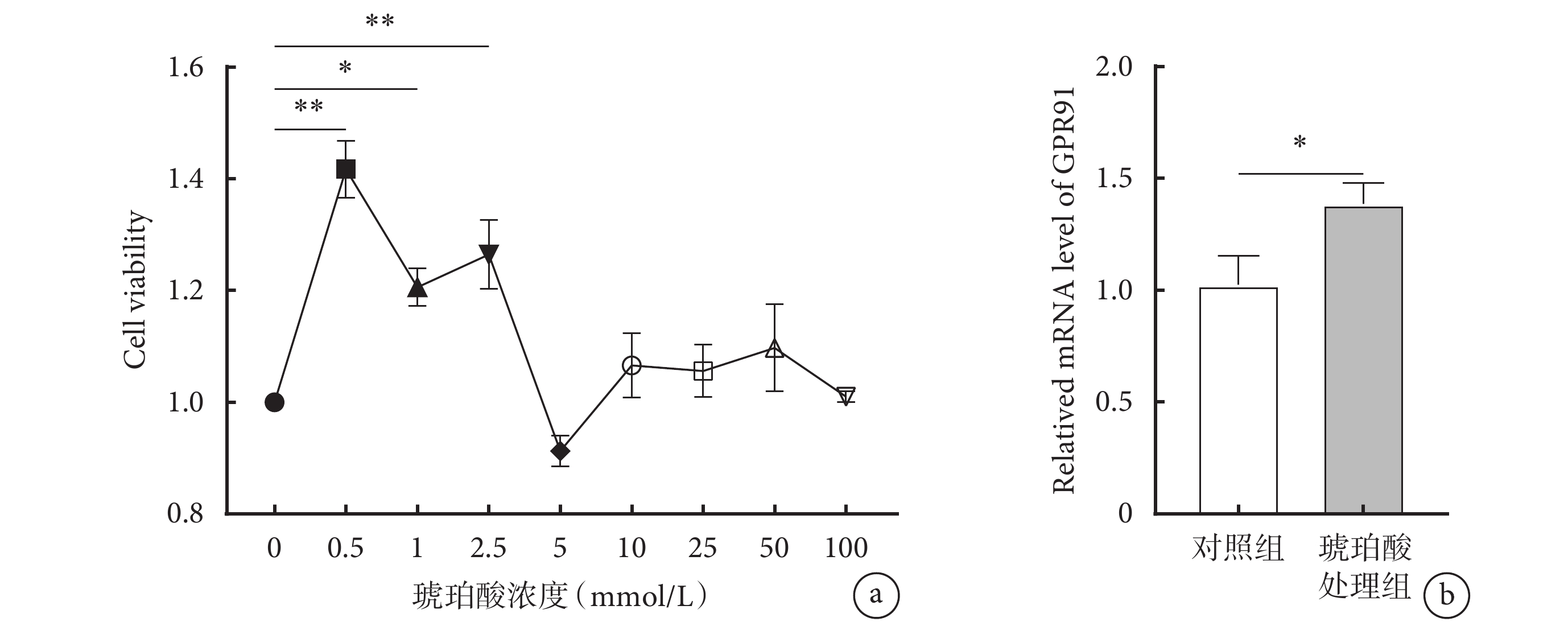 圖3
琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
圖3
琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
a. 不同濃度琥珀酸對MLE-12細胞活力的影響(*
2.4 琥珀酸對MH-S極化的影響
將MH-S置于含有1 mmol/L琥珀酸的完全培養基中24 h(琥珀酸處理組),與對照組比較,檢測M1/M2型巨噬細胞表型標記物。結果琥珀酸處理組iNOS、CD86 mRNA表達量升高(P<0.05),琥珀酸處理組CD206、Arg1 mRNA表達量降低(P<0.05)。證明1 mmol/L琥珀酸會增加巨噬細胞表面M1型標志物mRNA的表達。流式細胞學結果分析提示1 mmol/L的琥珀酸可增加CD86+CD206–肺泡巨噬細胞的數量與比例。結果見圖4。
 圖4
琥珀酸對MH-S極化的影響
圖4
琥珀酸對MH-S極化的影響
a. 光學顯微鏡下對照和琥珀酸處理MH-S細胞變化:與對照相比,琥珀酸處理細胞核較均勻一致(×100);b. 1 mmol/L琥珀酸上調M1極化標記基因(iNOS、CD86)的表達,抑制M2極化標記基因(CD206、Arg1)的表達;c. 1 mmol/L琥珀酸增加CD11b+CD86+M1型肺泡巨噬細胞的數量與比例,降低CD11b+CD206+M2型肺泡巨噬細胞的數量與比例(*
2.5 琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
與共培養組相比,琥珀酸處理后共培養組Vim和N-cad表達量顯著升高,E-cad表達量顯著下降(P<0.05)。與琥珀酸處理后共培養組相比,抑制劑組Vim和N-cad表達量顯著降低,E-cad表達量顯著升高(P<0.05)。結果見圖5。
 圖5
琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
圖5
琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
a. 光學顯微鏡下共培養組、琥珀酸處理后共培養組和抑制劑組MLE-12細胞變化:與共培養組相比,琥珀酸處理后共培養組未分化細胞數增多,與琥珀酸處理后共培養組相比,抑制劑組細胞呈現梭形,形態規則(×100);b. 共培養組、琥珀酸處理后共培養組和抑制劑組MLE-12細胞EMT相關蛋白的表達(*
3 討論
本實驗證實小鼠Ⅱ型肺泡上皮細胞系MLE-12在高氧環境48 h后,發生了明顯的EMT,表現為間質標志物(Vim和N-cad)表達增加,上皮標志物(E-cad)表達減少;MH-S與MLE-12共培養可增強上述EMT變化;1 mmol/L琥珀酸增加MH-S表面GPR91和iNOS、CD86 mRNA的表達,促進MH-S向M1型極化;1 mmol/L琥珀酸處理MH-S與MLE-12在高氧下共培養加重EMT變化,使用琥珀酸受體抑制劑后上述變化逆轉。琥珀酸可通過巨噬細胞表面受體GPR91,誘導小鼠肺泡巨噬細胞M1型極化,增強高氧小鼠肺泡上皮細胞損傷模型EMT,促進高氧纖維化的發生。
從臨床角度講,高氧指吸入氧濃度或動脈血氧水平過高的現象,以動脈血氧分壓高于120 mm Hg(1 mm Hg=0.133 kPa)為界。研究表明,高氧可導致多種細胞反應,如適應、修復、細胞凋亡、死亡和壞死[25]。高氧肺損傷病理表現之一為繼發性纖維組織增生。肺泡Ⅱ型上皮細胞被認為是肺泡上皮的祖細胞,對肺發育受損及損傷后修復具有重要意義[26]。持續的肺泡上皮細胞損傷和修復通過EMT介導的肺纖維化機制中發揮重要作用[27]。已有研究證明,高氧條件肺泡上皮會發生EMT,且EMT與器官纖維化有關[28-33]。EMT系指上皮細胞在特定的生理和病理情況下向間充質細胞轉化的現象,主要表現為上皮細胞丟失上皮標記物,同時逐漸演變成紡錘體的形態,并且獲得間質標記物[34]。高氧誘導肺纖維化的主要機制之一是EMT[27]。本實驗設置不同高氧時間,證明MLE-12可隨時間發生EMT改變,高氧48 h后Vim和N-cad表達量顯著升高,E-cad表達量顯著下降,與之前研究結果相符。
上皮細胞釋放炎癥介質,使炎癥細胞(如中性粒細胞、巨噬細胞等)有效募集到損傷部位,它們產生的多種細胞因子和趨化因子,會放大炎癥反應并引發纖維化[35]。巨噬細胞被整合到纖維化過程的所有階段[36],巨噬細胞通過分泌趨化因子和降解細胞外特異性基質金屬蛋白酶來促進纖維化[37]。高氧在產生氧化損傷的同時激活機體的炎癥反應通道,導致細胞凋亡并加劇炎癥反應,觸發的炎癥反應可激活巨噬細胞。從纖維化肺組織中分離的巨噬細胞也能分泌促纖維化細胞因子[38-40]。高氧條件下單細胞測序顯示巨噬細胞會在高氧環境中向M1型極化[41]。本實驗證明,將小鼠肺泡巨噬細胞和上皮細胞共培養,上皮細胞EMT相關蛋白表達增加,提示巨噬細胞可增強高氧過程中EMT反應,證明巨噬細胞參與高氧纖維化過程。
琥珀酸是細胞內一種重要的代謝產物,亦是炎癥中的一種物質代謝信號分子,并作為一種促炎代謝物參與細胞的各種生化過程,尤其是促進巨噬細胞的炎癥活動[42-46]。研究表明,在應激和炎癥條件下,如缺血再灌注途徑、腸道菌群代謝產物途徑等,琥珀酸會在細胞外大量積累[47-48]。琥珀酸已被證明通過其同源受體GPR91具有重要的細胞外信號功能[49]。GPR91是一種跨膜G蛋白偶聯受體,廣泛表達于多種細胞(巨噬細胞等免疫細胞)和組織(肺、脂肪與心肌等)[50]。這些組織細胞表面的GPR91通過感知細胞外琥珀酸信號,隨之激活下游信號通路,介導肺纖維化等病理生理效應[42,50-51]。本實驗證明琥珀酸可使小鼠肺泡巨噬細胞向促炎M1型極化,且巨噬細胞表面GPR91 mRNA表達增加,并通過EMT機制加重高氧肺損傷。所以,上述增加琥珀酸積累的生理病理狀況均可參與或加重肺纖維化的形成,這為臨床預防或治療纖維化的發生發展提供了理論參考。高氧誘導的肺損傷是一個復雜的綜合征,至今尚未有確切有效的治療方法。減少活性氧的過度產生,減少炎癥細胞的募集入肺,減輕炎癥反應,調節MAPKs等信號轉導通路和轉錄因子的活性是高氧性肺損傷中的重要干預靶點,但尚需要更加深入的研究[52]。
綜上所述,琥珀酸可通過激活肺泡巨噬細胞表面的琥珀酸受體,誘導肺泡巨噬細胞向M1型極化,增加高氧誘導急性肺損傷小鼠肺泡上皮間質轉化,促進肺纖維化的發生發展。
利益沖突:本研究不涉及任何利益沖突。
氧療是不同急慢性疾病、手術治療和早產相關的低氧血癥的重要步驟[1]。高濃度氧氣會引起高氧性急性肺損傷和病死率的增加[2-4]。高氧急性肺損傷動物模型表現為急性滲出性肺水腫、繼發性纖維組織增生、局部出血和透明膜形成等[5]。肺泡Ⅱ型上皮細胞是高氧介導肺損傷的關鍵靶點[6]。Adamson等[7]提出肺泡Ⅱ型上皮細胞可通過肺內上皮間質轉換變為成纖維細胞,讓我們對肺纖維化的病理有了進一步的理解。高氧肺損傷修復時,殘存的肺泡Ⅱ型上皮細胞可通過上皮間質轉化(epithelial–mesenchymal transition,EMT)機制轉化為成纖維細胞,若EMT增多,則可能發展為肺纖維化[8]。高氧環境下會產生更多的活性氧簇,氧化與抗氧化功能的失衡,發生氧化應激反應,導致組織器官損傷[9-10]。同時高氧還激活機體的細胞凋亡、炎癥反應通道和巨噬細胞,導致細胞凋亡并加劇炎癥反應[11-12]。炎癥、凋亡、組織修復性損傷等因素交織,相互作用共同形成了高氧肺損傷的機制,發生更為嚴重的損傷。巨噬細胞是肺損傷時呼吸系統最豐富的免疫細胞,是炎癥的主要驅動因素[13]。活化的巨噬細胞具有吞噬、消滅病原體和死細胞的能力,并能協調炎癥和愈合過程。根據其活化方式和功能的不同,巨噬細胞可分為兩大極化類型,即M1型(經典活化的巨噬細胞,促炎型)和M2型(交替活化的巨噬細胞,抗炎型)[14-15]。因此,巨噬細胞參與高氧肺組織的破壞,在炎癥過程中發揮重要作用[16]。琥珀酸是宿主和微生物代謝過程中產生的重要代謝物[17],是宿主細胞三羧酸循環的中間體,膳食纖維的發酵過程中也會大量產生琥珀酸。Akram和Connors等[18-19]在機體炎癥和代謝應激部位觀察到了琥珀酸的積累。高氧相關肺損傷后會出現糖酵解、糖酵解儲備和氧化磷酸化等糖代謝異常,影響機體能量供應[20-21]。大量研究支持琥珀酸鹽不僅是代謝的惰性副產物,也在下游細胞反應中發揮積極作用,并且可以作為促炎介質,在調節炎癥終點和解決肺部炎癥方面發揮關鍵作用[22-23]。研究表明,琥珀酸可通過巨噬細胞特異性膜表面受體琥珀酸受體1(succinate receptor 1,GPR91)激活免疫細胞并增強炎癥反應。在腸-肺軸相關研究中,腸道來源的琥珀酸可誘導巨噬細胞極化,加重肺損傷[24]。琥珀酸是否影響高氧造成的肺損傷和肺纖維化,目前未見研究報道。本實驗提出并驗證以下假設:琥珀酸通過誘導巨噬細胞極化,促進高氧誘發的肺上皮EMT,從而促進肺纖維化的形成。
1 材料與方法
1.1 材料與試劑
MLE-12小鼠肺泡上皮細胞,MH-S小鼠肺泡巨噬細胞,琥珀酸(美國Sigma公司),琥珀酸受體抑制劑(SUCNR1-IN-1,美國MCE生物科技公司),CCK-8試劑盒(山東思科捷公司),兔抗[E-鈣黏蛋白(E-cadherin,E-cad)、N-鈣黏蛋白(N-cadherin,N-cad)、波形蛋白(vimentin,Vim)](一抗),辣根過氧化物酶標記的山羊抗兔IgG(二抗)(武漢三鷹生物技術有限公司),Transwell小室(孔徑0.4 μm,美國康寧公司),引物由塞維爾生物工程(上海)股份有限公司合成。酶標儀(iMark,美國BioRad公司),曝光儀(Touch Imager pro,易孛特生命科學有限公司),實時定量PCR儀(StepOne Plus,美國Thermo),流式細胞儀器(CytoFLEX,美國貝克曼)。
1.2 方法
1.2.1 細胞培養
取凍存的MLE-12、MH-S細胞,進行復蘇,分別加入DMEM、RPMI
1.2.2 MLE-12高氧暴露時間篩選
取對數生長期的MLE-12,以1×106/皿鋪于6 cm的細胞培養皿中,分為高氧0 h組(0 h組)、高氧24 h組(24 h組)、高氧48 h組(48 h組)、高氧72 h組(72 h組),置于95% O2的培養箱中孵育不同分組時間。實驗重復3次。
1.2.3 MLE-12和MH-S共培養構建體外高氧肺損傷細胞模型
取對數生長期的MLE-12,以1×105/孔鋪于Transwell下室,分為0 h組、48 h組、與MH-S細胞共培養組(共培養組),將MH-S細胞以1×105/孔鋪于Transwell上室,0 h組、48 h組培養條件如上,共培養組置于95%O2的培養箱中孵育48 h,每組設置3個復孔。
1.2.4 篩選琥珀酸濃度
取MLE-12細胞,調整密度至2×103個/mL,將其接種至96孔板中,每孔加入細胞懸液100 μL。各組分別加入濃度為100 mmol/L、50 mmol/L、25 mmol/L、10 mmol/L、5 mmol/L、2.5 mmol/L、1 mmol/L、500 μmol/L琥珀酸的培養基干預24 h后,加入10 μL CCK-8溶液孵育30 min,使用酶標儀測定各組OD值(450 nm處)。細胞活力(%)=(干預組–空白組)OD值/(對照組–空白組)OD值×100%。實驗重復3次。
1.2.5 RT-qPCR法測定巨噬細胞極化M1、M2相關因子[誘導型一氧化氮合成酶(inducible nitricoxide synthase,iNOS)、CD86、Arg-1、CD206]及GPR91 mRNA相對表達量
將MH-S細胞分為對照組和琥珀酸處理組,對照組常規培養24 h,琥珀酸處理組在對照組基礎上加入上述濃度琥珀酸,采用細胞RNA快速提取試劑盒提取細胞樣本總RNA,NanoDrop檢測RNA的濃度及純度,反轉錄合成模板鏈cDNA,取2 μL反轉錄產物檢測PCR,以β-actin作為內參基因,2–ΔΔCt法計算目的基因相對表達量。實驗重復3次。PCR引物序列見表1。
1.2.6 流式細胞術肺泡巨噬細胞的M1與M2細胞分型與比例分析
–4℃,1 000轉離心5 min,沉淀MH-S細胞,用流式緩沖液重懸(105~106細胞/100 μL),充分混勻,加入APC抗小鼠CD11b抗體作為巨噬細胞共同表面標志;加入PE-Cy7抗小鼠CD86抗體,作為M1型巨噬細胞特異性標志;再加入FITC抗小鼠CD206抗體,作為M2型巨噬細胞特異性標志,室溫孵育30 min,生理鹽水清洗離心,流式細胞儀檢測,并用Flowjo軟件分析檢測結果。
1.2.7 細胞共培養探究琥珀酸的影響
將MLE-12細胞與MH-S細胞在孔徑為0.4 μm的Transwell小室中共培養,分為共培養、琥珀酸處理后共培養組、GPR91抑制劑組(抑制劑組)。共培養組:MLE-12細胞與C組MH-S細胞置于95% O2的培養箱中共培養48 h;琥珀酸處理后共培養組:MLE-12細胞與琥珀酸處理組MH-S細胞置于95% O2的培養箱中共培養48 h;抑制劑組:在琥珀酸處理組基礎上加入GPR91抑制劑(SUCNR1-IN-1)與MLE-12細胞在95% O2的培養箱中共培養48 h。
1.2.8 Western blotting法測定EMT相關蛋白相對表達量
取0 h組、24 h組、48 h組、72 h組、琥珀酸處理后共培養組、共培養組、抑制劑組MLE-12細胞,提取蛋白并進行定量后上樣,進行十二烷基硫酸鈉聚丙烯酰胺凝膠電泳,轉聚偏二氟乙烯膜,封閉90 min后參照抗體說明書加入一定稀釋比例的一抗(E-cad、N-cad、Vim、β-actin),4℃孵育過夜,次日TBST洗滌后加入山羊抗兔IgG二抗,孵育1 h,洗滌3次,最后加入顯影液,使用凝膠成像系統拍照記錄。蛋白灰度值用G表示,蛋白相對表達量=G目的蛋白/G內參蛋白(β-actin)。實驗重復3次。
1.3 統計學方法
采用SPSS 25.0統計學軟件進行數據分析。多組間比較采用One-Way ANOVA方差分析,首先利用Levene法進行方差齊性檢驗,確定方差齊性且整體比較組間差異有統計學意義后進一步作多重比較,多重比較采用LSD法。以P<0.05為差異有統計學意義。采用GraphPad Prism5.0軟件將實驗數據生成統計圖表。
2 結果
2.1 高氧對小鼠肺泡上皮EMT的影響
與0 h相比,24 h、48 h組Vim和N-cad表達量顯著升高,差異有統計學意義(P<0.05),24 h組E-cad表達量顯著升高(P<0.05),48 h組、72 h組E-cad表達量顯著下降(P<0.05),其余各組差異無統計學意義。證明給予小鼠肺泡上皮細胞48 h高濃度氧氣,EMT相關指標均會發生變化。因此,選擇48 h作為后續實驗高氧處理時間。結果見圖1。
 圖1
高氧對小鼠肺泡上皮EMT的影響
圖1
高氧對小鼠肺泡上皮EMT的影響
a. 光學顯微鏡下MLE-12在高氧不同時間變化,隨著高氧時間增加,未分化細胞增多(×100);b. MLE-12不同時間高氧后E-cad、N-cad及Vim蛋白表達水平比較(*
2.2 MH-S對MLE-12細胞EMT的影響
與0 h、48 h相比,共培養組Vim和N-cad表達量顯著升高,E-cad表達量顯著下降,差異有統計學意義(P<0.05)。證明MH-S與MLE-12共培養,MH-S會增強高氧條件下MLE-12細胞EMT。結果見圖2。
 圖2
MLE-12細胞在高氧0 h、高氧48 h以及與MH-S細胞高氧共培養48 h后E-cad、N-cad及Vim蛋白表達水平比較(*P<0.05)
圖2
MLE-12細胞在高氧0 h、高氧48 h以及與MH-S細胞高氧共培養48 h后E-cad、N-cad及Vim蛋白表達水平比較(*P<0.05)
2.3 琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
使用不同濃度的琥珀酸干預MLE-12細胞24 h后,各組細胞活力進行比較,與基礎值(0 mmol/L組)相比,100 mmol/L、50 mmol/L、25 mmol/L、10 mmol/L、5 mmol/L組細胞活力差異無統計學意義(P>0.05),2.5 mmol/L、1 mmol/L、500 μmol/L組細胞活力明顯升高(P<0.05)。選取1 mmol/L濃度進行后續實驗。與對照組進行比較,琥珀酸處理組GPR91 mRNA相對表達量顯著升高(P<0.05)。表明1 mmol/L琥珀酸會增加MH-S細胞表面GPR91 mRNA的表達。結果見圖3。
 圖3
琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
圖3
琥珀酸濃度篩選及其對MH-S細胞琥珀酸受體GPR91的影響
a. 不同濃度琥珀酸對MLE-12細胞活力的影響(*
2.4 琥珀酸對MH-S極化的影響
將MH-S置于含有1 mmol/L琥珀酸的完全培養基中24 h(琥珀酸處理組),與對照組比較,檢測M1/M2型巨噬細胞表型標記物。結果琥珀酸處理組iNOS、CD86 mRNA表達量升高(P<0.05),琥珀酸處理組CD206、Arg1 mRNA表達量降低(P<0.05)。證明1 mmol/L琥珀酸會增加巨噬細胞表面M1型標志物mRNA的表達。流式細胞學結果分析提示1 mmol/L的琥珀酸可增加CD86+CD206–肺泡巨噬細胞的數量與比例。結果見圖4。
 圖4
琥珀酸對MH-S極化的影響
圖4
琥珀酸對MH-S極化的影響
a. 光學顯微鏡下對照和琥珀酸處理MH-S細胞變化:與對照相比,琥珀酸處理細胞核較均勻一致(×100);b. 1 mmol/L琥珀酸上調M1極化標記基因(iNOS、CD86)的表達,抑制M2極化標記基因(CD206、Arg1)的表達;c. 1 mmol/L琥珀酸增加CD11b+CD86+M1型肺泡巨噬細胞的數量與比例,降低CD11b+CD206+M2型肺泡巨噬細胞的數量與比例(*
2.5 琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
與共培養組相比,琥珀酸處理后共培養組Vim和N-cad表達量顯著升高,E-cad表達量顯著下降(P<0.05)。與琥珀酸處理后共培養組相比,抑制劑組Vim和N-cad表達量顯著降低,E-cad表達量顯著升高(P<0.05)。結果見圖5。
 圖5
琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
圖5
琥珀酸誘導巨噬細胞極化對高氧肺泡上皮EMT的影響
a. 光學顯微鏡下共培養組、琥珀酸處理后共培養組和抑制劑組MLE-12細胞變化:與共培養組相比,琥珀酸處理后共培養組未分化細胞數增多,與琥珀酸處理后共培養組相比,抑制劑組細胞呈現梭形,形態規則(×100);b. 共培養組、琥珀酸處理后共培養組和抑制劑組MLE-12細胞EMT相關蛋白的表達(*
3 討論
本實驗證實小鼠Ⅱ型肺泡上皮細胞系MLE-12在高氧環境48 h后,發生了明顯的EMT,表現為間質標志物(Vim和N-cad)表達增加,上皮標志物(E-cad)表達減少;MH-S與MLE-12共培養可增強上述EMT變化;1 mmol/L琥珀酸增加MH-S表面GPR91和iNOS、CD86 mRNA的表達,促進MH-S向M1型極化;1 mmol/L琥珀酸處理MH-S與MLE-12在高氧下共培養加重EMT變化,使用琥珀酸受體抑制劑后上述變化逆轉。琥珀酸可通過巨噬細胞表面受體GPR91,誘導小鼠肺泡巨噬細胞M1型極化,增強高氧小鼠肺泡上皮細胞損傷模型EMT,促進高氧纖維化的發生。
從臨床角度講,高氧指吸入氧濃度或動脈血氧水平過高的現象,以動脈血氧分壓高于120 mm Hg(1 mm Hg=0.133 kPa)為界。研究表明,高氧可導致多種細胞反應,如適應、修復、細胞凋亡、死亡和壞死[25]。高氧肺損傷病理表現之一為繼發性纖維組織增生。肺泡Ⅱ型上皮細胞被認為是肺泡上皮的祖細胞,對肺發育受損及損傷后修復具有重要意義[26]。持續的肺泡上皮細胞損傷和修復通過EMT介導的肺纖維化機制中發揮重要作用[27]。已有研究證明,高氧條件肺泡上皮會發生EMT,且EMT與器官纖維化有關[28-33]。EMT系指上皮細胞在特定的生理和病理情況下向間充質細胞轉化的現象,主要表現為上皮細胞丟失上皮標記物,同時逐漸演變成紡錘體的形態,并且獲得間質標記物[34]。高氧誘導肺纖維化的主要機制之一是EMT[27]。本實驗設置不同高氧時間,證明MLE-12可隨時間發生EMT改變,高氧48 h后Vim和N-cad表達量顯著升高,E-cad表達量顯著下降,與之前研究結果相符。
上皮細胞釋放炎癥介質,使炎癥細胞(如中性粒細胞、巨噬細胞等)有效募集到損傷部位,它們產生的多種細胞因子和趨化因子,會放大炎癥反應并引發纖維化[35]。巨噬細胞被整合到纖維化過程的所有階段[36],巨噬細胞通過分泌趨化因子和降解細胞外特異性基質金屬蛋白酶來促進纖維化[37]。高氧在產生氧化損傷的同時激活機體的炎癥反應通道,導致細胞凋亡并加劇炎癥反應,觸發的炎癥反應可激活巨噬細胞。從纖維化肺組織中分離的巨噬細胞也能分泌促纖維化細胞因子[38-40]。高氧條件下單細胞測序顯示巨噬細胞會在高氧環境中向M1型極化[41]。本實驗證明,將小鼠肺泡巨噬細胞和上皮細胞共培養,上皮細胞EMT相關蛋白表達增加,提示巨噬細胞可增強高氧過程中EMT反應,證明巨噬細胞參與高氧纖維化過程。
琥珀酸是細胞內一種重要的代謝產物,亦是炎癥中的一種物質代謝信號分子,并作為一種促炎代謝物參與細胞的各種生化過程,尤其是促進巨噬細胞的炎癥活動[42-46]。研究表明,在應激和炎癥條件下,如缺血再灌注途徑、腸道菌群代謝產物途徑等,琥珀酸會在細胞外大量積累[47-48]。琥珀酸已被證明通過其同源受體GPR91具有重要的細胞外信號功能[49]。GPR91是一種跨膜G蛋白偶聯受體,廣泛表達于多種細胞(巨噬細胞等免疫細胞)和組織(肺、脂肪與心肌等)[50]。這些組織細胞表面的GPR91通過感知細胞外琥珀酸信號,隨之激活下游信號通路,介導肺纖維化等病理生理效應[42,50-51]。本實驗證明琥珀酸可使小鼠肺泡巨噬細胞向促炎M1型極化,且巨噬細胞表面GPR91 mRNA表達增加,并通過EMT機制加重高氧肺損傷。所以,上述增加琥珀酸積累的生理病理狀況均可參與或加重肺纖維化的形成,這為臨床預防或治療纖維化的發生發展提供了理論參考。高氧誘導的肺損傷是一個復雜的綜合征,至今尚未有確切有效的治療方法。減少活性氧的過度產生,減少炎癥細胞的募集入肺,減輕炎癥反應,調節MAPKs等信號轉導通路和轉錄因子的活性是高氧性肺損傷中的重要干預靶點,但尚需要更加深入的研究[52]。
綜上所述,琥珀酸可通過激活肺泡巨噬細胞表面的琥珀酸受體,誘導肺泡巨噬細胞向M1型極化,增加高氧誘導急性肺損傷小鼠肺泡上皮間質轉化,促進肺纖維化的發生發展。
利益沖突:本研究不涉及任何利益沖突。