因果推斷的快速發展正在引起眾多學科領域研究的“范式革命”。“目標試驗模擬”被認為是一種極具前景的觀察性真實世界研究框架,已經受到國內外衛生領域學者和監管部門的廣泛關注。本文旨在概述目標試驗模擬研究進展的基礎上,介紹目標試驗模擬研究在線輔助實施工具CERBOT的基本情況,并通過一項實例對其操作過程進行說明,以期幫助國內研究人員開展目標試驗模擬研究,并為最終促進國內醫療領域真實世界研究質量和醫療服務水平產生積極影響。
引用本文: 盧存存, 柯立鑫, 王子怡, 陳子佳, 王志飛. 目標試驗模擬研究輔助實施工具CERBOT簡介與應用. 中國循證醫學雜志, 2024, 24(2): 237-242. doi: 10.7507/1672-2531.202307121 復制
版權信息: ?四川大學華西醫院華西期刊社《中國循證醫學雜志》版權所有,未經授權不得轉載、改編
因果推斷的快速發展正在引起眾多學科領域研究的“范式革命”[1,2]。長期以來,隨機對照試驗被認為是進行因果推斷的金標準設計[2],醫學領域中通常使用它來獲取醫療干預有效性和安全性的證據,用以支持臨床實踐和監管決策[3-5]。然而,某些情況下,開展隨機對照試驗是不可行或者不符合醫學倫理的,同時經費和時間成本過高,且由于嚴苛的納排標準使得其結果的外部效度常常較低,難以有效地推廣到試驗外的真實世界人群[4-6]。近年來,由于醫療領域“健康大數據”的日益普及和計算與分析能力的進步,使得基于真實世界數據(例如,電子健康記錄)的觀察性研究數量激增[7]。基于真實世界數據開展藥物流行病學和藥物經濟學研究支持醫療監管決策活動已然成為一種趨勢[8,9]。然而,多項方法學研究表明[10-12],已發表的觀察性真實世界研究常常在方法學上存在重大的設計缺陷,同時存在報告質量不高的問題。例如,一項納入了75項觀察性真實世界研究的方法學調查表明[10],57%的研究存在永恒時間偏倚,44%存在現用藥者偏倚。
近年來,各種研究框架(例如,目標試驗模擬[13])、設計要素(例如,陽性對照新用藥者設計[14])、分析策略(例如,“克隆-刪失-逆概率加權”[15])和分析方法(例如,逆概率重疊加權[16])被提出或拓展用以解決基于觀察性數據的因果效應推斷問題。尤其值得關注的是,2016年被正式確立的“目標試驗模擬”研究框架[4,13]。該框架認為評價醫療干預因果效應的觀察性研究都對應著一個假想的可以開展的理想實效性隨機對照試驗(即目標試驗)[5,13]。基于真實世界數據盡可能地模擬該目標試驗開展觀察性研究以明確干預與結局間因果關聯的過程,即目標試驗模擬研究[4,5,13]。近年來,該框架因其明顯的優勢(例如,研究過程透明度高[5,13]、正確模擬時能得到與隨機對照試驗相似的估計值[5,17])已經引起了國內外醫療領域學者和監管部門的廣泛關注[4,18-22]。例如,美國FDA聯合哈佛大學布萊根婦女醫院及Aetion公司開展了RCT-DUPLICATE項目[20,21],旨在利用醫療索賠數據模擬32個藥物隨機對照試驗(其中2個為正在進行的試驗)以評價真實世界研究與隨機對照試驗間的“效果-效力”差距,并探索差距產生的原因,從而幫助明確使用真實世界證據支持監管決策的可行性;該項目最終結果已于近期發表于JAMA[21],研究團隊認為真實世界研究能夠補充隨機對照試驗證據,從而幫助我們更好地理解在真實臨床實踐中藥物是如何發揮作用的。中國藥監局藥品審評中心也在今年2月份發布的《藥物真實世界研究設計與方案框架指導原則(試行)》中明確指出[22],目標試驗模擬是一種值得探索的真實世界研究方法。
盡管目標試驗模擬提供了一種極具前景的開展真實世界研究的框架,但基于真實世界數據開展目標試驗模擬研究并不是一項簡單的工作,往往需要研究團隊具備豐富的臨床/藥物流行病學和生物醫藥知識以及強大的統計計算能力[5,21,23]。因此,為了幫助研究人員和臨床醫生更好地利用該框架開展觀察性真實世界研究,Zhang Y團隊于2019年開發了目標試驗模擬研究的在線輔助實施工具CERBOT(comparative effectiveness research based on observational data to emulate a target trial)[24]。鑒于目標試驗模擬研究的重要價值,且未見到國內有學者使用該工具開展目標試驗模擬研究,本文旨在介紹該工具的基本情況,并通過參考一篇近期發表的目標試驗模擬研究論文演示該工具的使用[25],以期為國內真實世界研究工作者開展研究提供參考,并最終提高國內醫療領域真實世界研究的質量,從而為臨床實踐和監管決策提供可信賴的真實世界證據。
1 CERBOT簡介和注冊與登錄
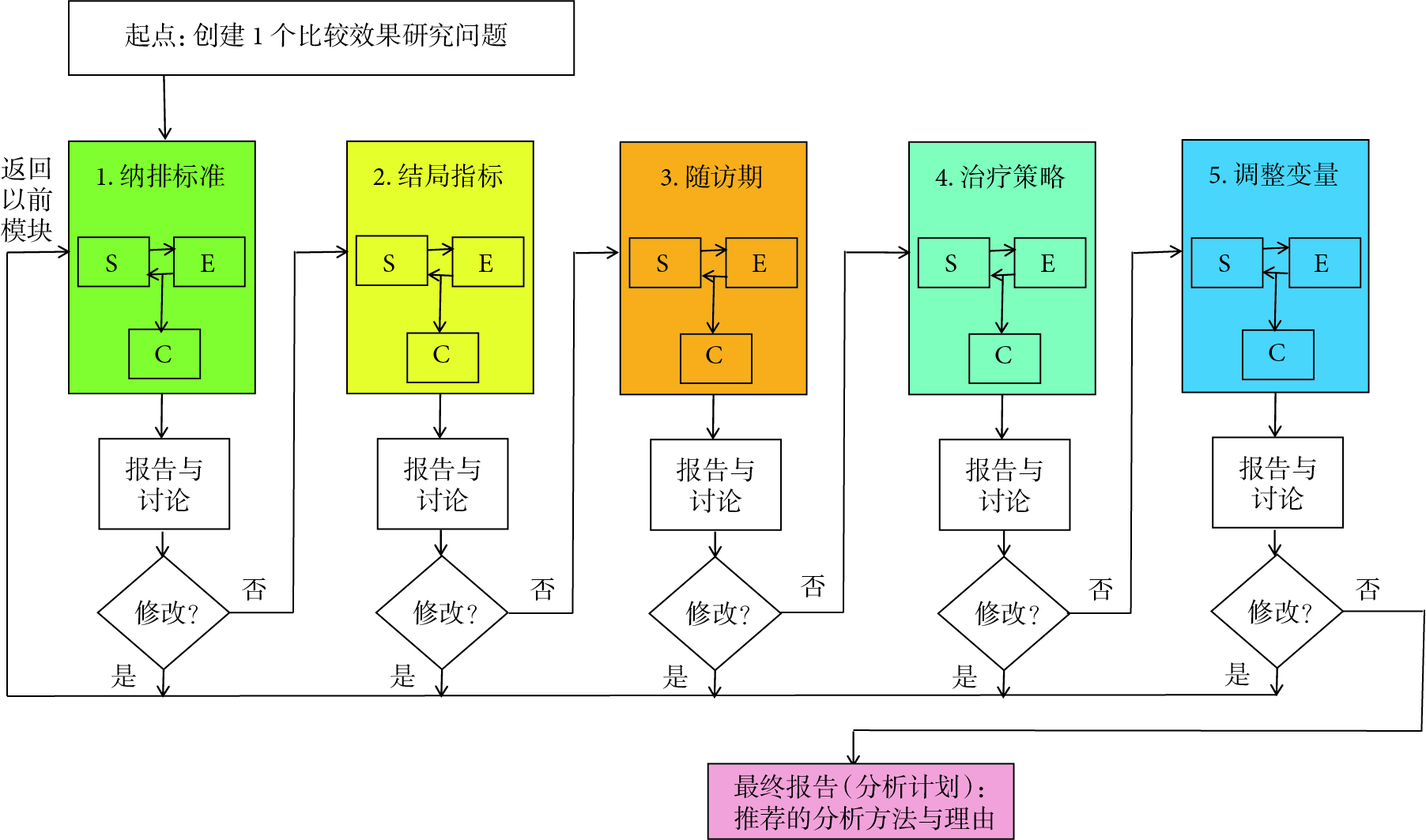
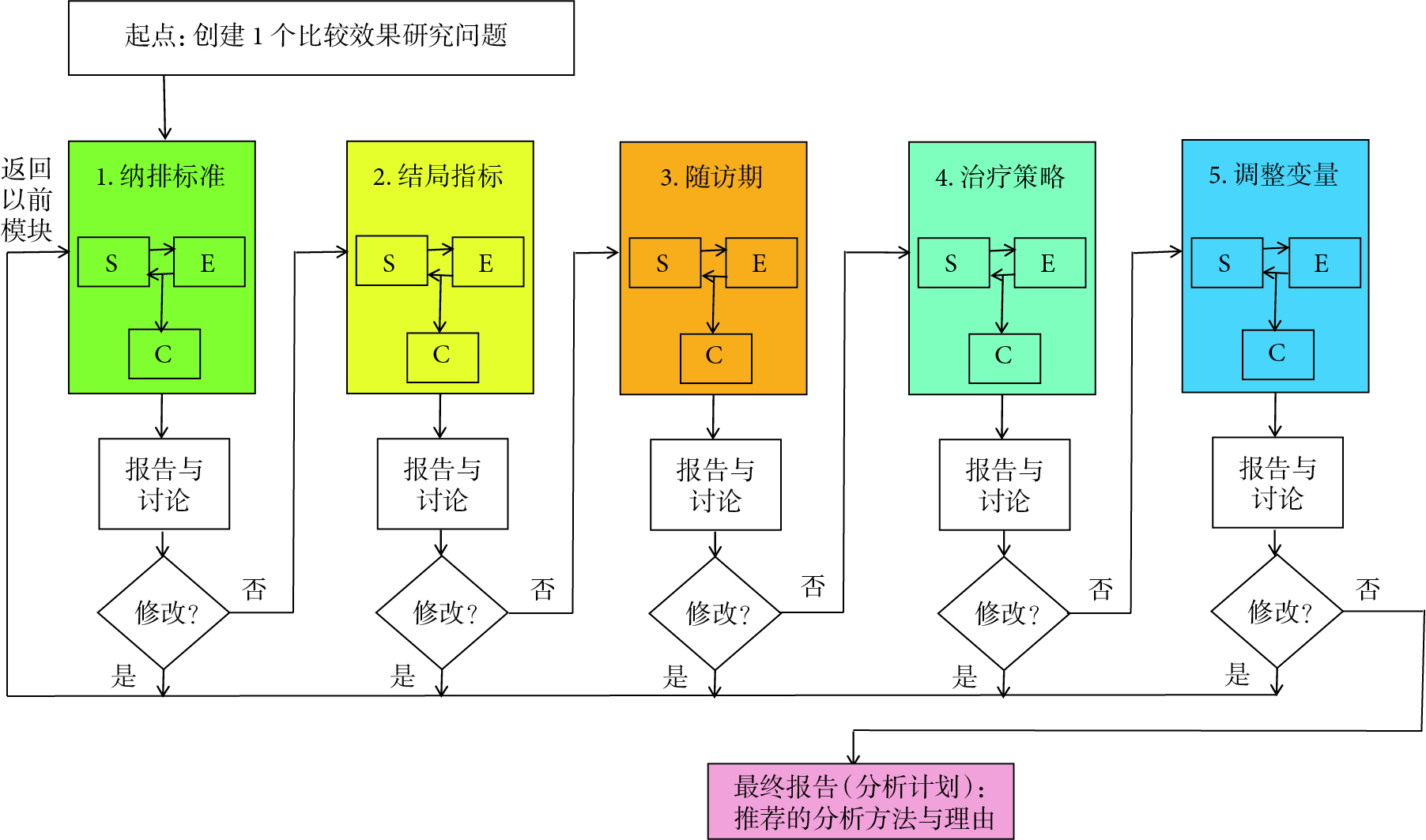
CERBOT為一款在線工具[24],網址為http://cerbot.org/。該工具由納入排除標準(eligibility criteria)、結局指標(outcomes)、隨訪期(follow-up period)、治療策略(treatment strategies)和調整變量(adjustment variables)等5個模塊,再加一個基于5個模塊的選項答案自動生成的“分析計劃”(analysis plan)組成(圖1),它們都是目標試驗模擬研究框架中的重要組成要素[4]。該工具的使用需要進行注冊,可使用機構郵箱或者個人郵箱進行注冊,注冊成功后利用注冊所使用的郵箱和密碼登錄賬戶后即可開始使用,注冊與登錄界面見附件圖1,登錄后的初始界面見附件圖2。
2 CERBOT的具體操作流程
為了演示CERBOT的操作方法,本研究以近期發表于British Journal of Cancer的一項目標試驗模擬研究論文為例[25],其目標試驗模擬研究部分旨在利用CORECT-R癌癥數據集比較診斷后6個月內進行手術和不進行手術治療對在英格蘭2014―2017年診斷為4期結腸癌,年齡為50~84歲的患者診斷后1年內總生存率(全因死亡率)的影響。由于本研究的主要目的僅是為了演示操作流程,且實例中報告的數據集信息有限,因此在下面的演示過程中僅填寫了關鍵信息,其余均填入“-”進行代替。
在登錄該工具后,首先需要通過點擊工具上方的“New Question”打開研究問題創建界面(附件圖3),然后,在“What is your CER question?”框中填入所研究問題的概要描述,再在“What is data source?”框中填入用以支持本次研究開展的數據集來源(該選框必須填寫,否則無法進行下一步操作)。完成上述操作后,用戶可通過名字和郵箱邀請團隊成員加入該項目(附件圖4a、4b),也可直接點擊“Save & Start Module 1”進入模塊1“Eligibility criteria”信息填寫界面進行該模塊的操作。
模塊1“Eligibility criteria”的內容共涉及9個主要方面(見附件圖5、圖6,“Case studies”為該工具提供的2個案例)。分別為“Who is your target population?”(目標人群);“During what time period will you identify study subjects?(招募期)”;“Demographics(人口學特征)”,其下又包括“Age”“Sex”和“Race”3個變量(可點擊“Tip”獲取提示,還可利用“Concerns”對該變量存在的任何疑問進行備注);“Other socioeconomic status?”(其他社會經濟學特征);“Medical condition”(疾病或健康狀況),其下又包括“What medical condition(s) do you want to include?”(目標疾病或健康狀況)和“What medical condition(s) do you want to exclude?”(需要排除的健康狀況);“Any requirements for lab values?”(實驗室指標);“Any requirements for medication use?”(藥物使用);“Any requirements for provider type or site of care?”(干預實施的場所)和“Additional eligibility criteria not listed above?”(其他情況)。用戶使用時可根據自己所研究的具體問題和使用的數據集信息依次完成上述內容的填寫。例如,在第1個問題的框中填入“Patients diagnosed with stage IV colon cancer(CC) in England”;而其他問題需填寫的內容包括4個框,以第2個問題為例,在其第1個框中填入招募期“1st Jan, 2014 to 31th Dec, 2017”,第2個框中填入數據來源“CORECT-R”,第3個框中填入變量名與說明“CCDX_YR (year of CC diagnosis)”,最后,在第4個框中填入缺失數據的處理算法“If time of CC diagnosis is missing, the date of first visit will be used”。完成模塊1所有項目的操作后,點擊位于填寫界面底部的“Review summary”(圖上未展示)可得到該模塊的匯總報告(附件圖6);團隊成員可對其進行討論,并利用“Post comment”備注討論內容,也可利用“Back”返回上一步進行修改。確定無誤后可點擊“Download report”下載該匯總報告,之后點擊“Proceed to module 2”進入模塊2“Outcomes”進行該模塊的操作。
模塊2“Outcomes”的內容共涉及2個方面(附件圖7、圖8)。第1個為“What type is it?”,即結局指標類型,包括二分類(Dichotomous)、連續性(Continuous)和時間-事件(Failure time)3種類型,示例研究的結局指標為“全因死亡率”,故選擇“Failure time”。第2個為“Define your outcome”,即定義結局指標(附件圖7)。在完成所有項目操作后,可參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖8),然后點擊“Proceed to module 3”進入模塊3“Follow-up period”進行該模塊的操作。
模塊3“Follow-up period”的內容共涉及2個主要方面(附件圖9、圖10)。第1個為“Censoring”(刪失),其下又包括“Administrative end of follow-up”(管理性隨訪結束)、“Loss to follow-up”(失訪)、“Other censoring events”(其他刪失事件)和“Do you expect that censoring may result in selection bias?”(刪失是否可能造成選擇偏倚)。第2個為“Competing event”(競爭事件),示例研究的終點結局為“全因死亡率”,不存在競爭事件(附件圖10)。在完成所有項目操作后,可同樣參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖10),然后點擊“Proceed to module 4”進入模塊4“Treatment strategies”進行該模塊的操作。
模塊4“Treatment strategies”的內容同樣涉及2個主要方面,即需要分別對治療組與對照組干預的具體情況進行說明(附件圖11、圖12)。具體操作時,首先在“Strategy label”框中填入干預名稱;其次需要完成“Type”下的多個問題,當所研究的干預為點干預(Point intervention)[5],例如,示例研究中的外科手術;則“Does this treatment strategy consist of an intervention that happens at baseline only?”應該選擇“Yes”;隨后需要完成“Describe the intervention in such a way that other people can implement it”(描述干預的細節,例如,劑量、頻次)以保證別人可以重復干預和回答“Do you allow a certain period of time (grace period) to implement this intervention? ”以明確是否有寬限期(即設定的允許接受干預的某個時間段),示例研究的寬限期為6個月[25],因此選擇“Yes”,并填入“Six months”。但當所研究的干預為持續治療策略(Sustained strategy),例如,從某個時間點開始服用某藥物,并需要一直服用3年,則需要選擇“No”, 隨后需要回答“Does this treatment strategy assign everybody to interventions at fixed times after baseline (regardless of changes in individual characteristics) ?”(是否在基線后的固定時間點對每個患者分配干預),當選擇“Yes”時,需要在“Describe the intervention required by this treatment strategy”下面填入干預的細節信息;以及回答“Do you allow a certain period of time (grace period) to implement this intervention?”(寬限期,同前);當選擇“No”時,則需要回答“What is the trigger and resulting intervention?”(觸發干預實施的事件)和“Do you allow a certain period of time (grace period) to implement this intervention?”(寬限期,同前)。對照組干預信息的填寫過程與治療組一致,參照治療組填寫即可。在完成所有項目操作后,可同樣參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖12),然后點擊“Proceed to module 5”進入模塊5“Adjustment variables”進行該模塊的操作。
模塊5“Adjustment variables”的操作比較復雜(附件圖13、圖14),主要是后續項目是否出現會受到其之前其他項目答案的影響。當“Causal contrasts of interest”(因果比較;當干預為點干預,即模塊4中“Does this treatment strategy consist of an intervention that happens at baseline only?”回答為“Yes”時,不出現該選項)選擇“Intention to treat”(意向治療效應)時,會出現“Patient demographics”(人口學特征)、“Baseline variables related to patient outcomes”(與結局相關的基線變量)、“Additional baseline variables”(其他基線變量)、“Post-baseline variables”(基線后變量;當模塊4中“Does this treatment strategy consist of an intervention that happens at baseline only?”回答為“Yes”時,不出現該選項)、“Loss-to-follow up variables”(失訪變量)和“Which variables are potentially important, but are not measured in your data?”(潛在重要但未測量的變量)6個項目。當選擇“Per protocol”(符合方案效應)時,會額外增加1個項目,即和“Do you have time-dependent confounding?If yes,please describe time-dependent confounders”(時依混雜因素,存在時需要描述)。示例研究的干預為點干預(附件圖13,默認估計符合方案效應),除需要完成“Patient demographics”“Baseline variables related to patient outcomes”“Additional baseline variables”“Loss-to-follow up variables”和“Which variables are potentially important, but are not measured in your data?”5個項目的操作外,還需要回答“Do you have an instrument variable? If yes, please specify”(是否有工具變量,存在時需要描述);在完成所有項目操作后,點擊“Review summary”(未展示,同附件圖7)得到匯總報告,見附件圖14。點擊“Proceed to module analysis”會自動生成建議的統計分析計劃“Analysis plan”(附件圖15),使用者可參考該內容進一步制定詳細的統計分析方案。最后再點擊“Download report”可下載Word版的完整報告進行進一步的編輯和調整。此外,該工具具有保存分析記錄的功能,因此,用戶可在下次重新登入賬戶后對已填寫的內容進行修改和調整。
3 討論
國際人用藥品注冊技術協調會強調藥物臨床研究的本質是因果推斷,而藥物研發和評價的核心問題就是明確藥物治療效應的存在性并估計其大小[26]。盡管已經發表了大量的評價藥物干預效果的觀察性真實世界研究,但調查同一問題的不同真實世界研究之間以及它們與對應的隨機對照試驗之間的結果常常存在較大差異,甚至互相矛盾[5,27,28];如此,不但限制了研究結果的推廣應用,而且導致了可避免的研究資源的巨大浪費和非必要的“碳足跡”的增加,同時還影響了監管部門、臨床醫生及公眾對真實世界證據的信任度[29-31]。造成上述問題的主要原因可能是缺少統一的高質量操作指南,從而使得很多觀察性真實世界研究的透明度不足;或者僅考慮了混雜而未能考慮不良影響更大的偏倚(例如,永恒時間偏倚和現用藥者偏倚,后者為選擇偏倚的一種)[5,28]。
近年來,目標試驗模擬研究框架被正式確立,它能夠使得基于真實世界數據開展的觀察性研究更加透明和嚴格,使得分析結果的因果效應更具可解釋性[5,13,19]。目前,該框架已經被廣泛用于評價不同干預措施(例如,藥物、疫苗、營養、手術和社會政策干預)對各種健康相關問題(例如,心血管疾病、腎病、糖尿病、COVID-19和腫瘤)的因果效應[5,32-34];也有學者將其應用于衛生經濟學評價研究[4,34]。此外,最近有學者認為該框架應該成為評價醫療干預效果的比較觀察性研究的金標準方法,但也有學者對此持反對觀點[5,19]。開展目標試驗模擬研究的關鍵點是同步符合納入標準、干預措施分配和隨訪起點這3個時間點;而在真正的隨機對照試驗研究中,隨機化時就會自動同步它們[5,7]。但是,需要注意的是,目標試驗模擬研究并不是一種新的流行病學研究設計,也不指定具體的統計分析方法,解決不同的研究問題往往需要根據實際情況選擇不同的研究設計和對應的統計分析方法[4,5]。此外,目標試驗模擬研究也具有其局限性[4,5,35],例如,無法模擬沒有臨床數據的新藥物、無法解決數據本身存在的測量偏倚問題和不能保證沒有殘余混雜。Zhang Y團隊于2019年開發了專門用于輔助目標試驗模擬研究實施的CERBOT工具[24],主要由5個模塊組成,通過填寫5個模塊的內容可以有效地指導研究人員設計和實施目標試驗模擬研究和明確真實世界數據的特征;最終該工具可根據所填寫的模塊內容自動生成統計分析計劃建議并提供相應的理由;同時,工具的網頁上還提供了開展目標試驗模擬研究可能涉及的統計方法及統計軟件包的介紹。本研究對該款具有團隊協同操作和記錄保存功能的新工具的基本情況進行了介紹,并基于實例演示了該工具的操作過程,以期幫助提高國內醫療領域真實世界研究的質量,最終為臨床實踐和監管決策提供高質量的真實世界證據。
聲明 本文不存在任何利益沖突。
因果推斷的快速發展正在引起眾多學科領域研究的“范式革命”[1,2]。長期以來,隨機對照試驗被認為是進行因果推斷的金標準設計[2],醫學領域中通常使用它來獲取醫療干預有效性和安全性的證據,用以支持臨床實踐和監管決策[3-5]。然而,某些情況下,開展隨機對照試驗是不可行或者不符合醫學倫理的,同時經費和時間成本過高,且由于嚴苛的納排標準使得其結果的外部效度常常較低,難以有效地推廣到試驗外的真實世界人群[4-6]。近年來,由于醫療領域“健康大數據”的日益普及和計算與分析能力的進步,使得基于真實世界數據(例如,電子健康記錄)的觀察性研究數量激增[7]。基于真實世界數據開展藥物流行病學和藥物經濟學研究支持醫療監管決策活動已然成為一種趨勢[8,9]。然而,多項方法學研究表明[10-12],已發表的觀察性真實世界研究常常在方法學上存在重大的設計缺陷,同時存在報告質量不高的問題。例如,一項納入了75項觀察性真實世界研究的方法學調查表明[10],57%的研究存在永恒時間偏倚,44%存在現用藥者偏倚。
近年來,各種研究框架(例如,目標試驗模擬[13])、設計要素(例如,陽性對照新用藥者設計[14])、分析策略(例如,“克隆-刪失-逆概率加權”[15])和分析方法(例如,逆概率重疊加權[16])被提出或拓展用以解決基于觀察性數據的因果效應推斷問題。尤其值得關注的是,2016年被正式確立的“目標試驗模擬”研究框架[4,13]。該框架認為評價醫療干預因果效應的觀察性研究都對應著一個假想的可以開展的理想實效性隨機對照試驗(即目標試驗)[5,13]。基于真實世界數據盡可能地模擬該目標試驗開展觀察性研究以明確干預與結局間因果關聯的過程,即目標試驗模擬研究[4,5,13]。近年來,該框架因其明顯的優勢(例如,研究過程透明度高[5,13]、正確模擬時能得到與隨機對照試驗相似的估計值[5,17])已經引起了國內外醫療領域學者和監管部門的廣泛關注[4,18-22]。例如,美國FDA聯合哈佛大學布萊根婦女醫院及Aetion公司開展了RCT-DUPLICATE項目[20,21],旨在利用醫療索賠數據模擬32個藥物隨機對照試驗(其中2個為正在進行的試驗)以評價真實世界研究與隨機對照試驗間的“效果-效力”差距,并探索差距產生的原因,從而幫助明確使用真實世界證據支持監管決策的可行性;該項目最終結果已于近期發表于JAMA[21],研究團隊認為真實世界研究能夠補充隨機對照試驗證據,從而幫助我們更好地理解在真實臨床實踐中藥物是如何發揮作用的。中國藥監局藥品審評中心也在今年2月份發布的《藥物真實世界研究設計與方案框架指導原則(試行)》中明確指出[22],目標試驗模擬是一種值得探索的真實世界研究方法。
盡管目標試驗模擬提供了一種極具前景的開展真實世界研究的框架,但基于真實世界數據開展目標試驗模擬研究并不是一項簡單的工作,往往需要研究團隊具備豐富的臨床/藥物流行病學和生物醫藥知識以及強大的統計計算能力[5,21,23]。因此,為了幫助研究人員和臨床醫生更好地利用該框架開展觀察性真實世界研究,Zhang Y團隊于2019年開發了目標試驗模擬研究的在線輔助實施工具CERBOT(comparative effectiveness research based on observational data to emulate a target trial)[24]。鑒于目標試驗模擬研究的重要價值,且未見到國內有學者使用該工具開展目標試驗模擬研究,本文旨在介紹該工具的基本情況,并通過參考一篇近期發表的目標試驗模擬研究論文演示該工具的使用[25],以期為國內真實世界研究工作者開展研究提供參考,并最終提高國內醫療領域真實世界研究的質量,從而為臨床實踐和監管決策提供可信賴的真實世界證據。
1 CERBOT簡介和注冊與登錄
CERBOT為一款在線工具[24],網址為http://cerbot.org/。該工具由納入排除標準(eligibility criteria)、結局指標(outcomes)、隨訪期(follow-up period)、治療策略(treatment strategies)和調整變量(adjustment variables)等5個模塊,再加一個基于5個模塊的選項答案自動生成的“分析計劃”(analysis plan)組成(圖1),它們都是目標試驗模擬研究框架中的重要組成要素[4]。該工具的使用需要進行注冊,可使用機構郵箱或者個人郵箱進行注冊,注冊成功后利用注冊所使用的郵箱和密碼登錄賬戶后即可開始使用,注冊與登錄界面見附件圖1,登錄后的初始界面見附件圖2。
2 CERBOT的具體操作流程
為了演示CERBOT的操作方法,本研究以近期發表于British Journal of Cancer的一項目標試驗模擬研究論文為例[25],其目標試驗模擬研究部分旨在利用CORECT-R癌癥數據集比較診斷后6個月內進行手術和不進行手術治療對在英格蘭2014―2017年診斷為4期結腸癌,年齡為50~84歲的患者診斷后1年內總生存率(全因死亡率)的影響。由于本研究的主要目的僅是為了演示操作流程,且實例中報告的數據集信息有限,因此在下面的演示過程中僅填寫了關鍵信息,其余均填入“-”進行代替。
在登錄該工具后,首先需要通過點擊工具上方的“New Question”打開研究問題創建界面(附件圖3),然后,在“What is your CER question?”框中填入所研究問題的概要描述,再在“What is data source?”框中填入用以支持本次研究開展的數據集來源(該選框必須填寫,否則無法進行下一步操作)。完成上述操作后,用戶可通過名字和郵箱邀請團隊成員加入該項目(附件圖4a、4b),也可直接點擊“Save & Start Module 1”進入模塊1“Eligibility criteria”信息填寫界面進行該模塊的操作。
模塊1“Eligibility criteria”的內容共涉及9個主要方面(見附件圖5、圖6,“Case studies”為該工具提供的2個案例)。分別為“Who is your target population?”(目標人群);“During what time period will you identify study subjects?(招募期)”;“Demographics(人口學特征)”,其下又包括“Age”“Sex”和“Race”3個變量(可點擊“Tip”獲取提示,還可利用“Concerns”對該變量存在的任何疑問進行備注);“Other socioeconomic status?”(其他社會經濟學特征);“Medical condition”(疾病或健康狀況),其下又包括“What medical condition(s) do you want to include?”(目標疾病或健康狀況)和“What medical condition(s) do you want to exclude?”(需要排除的健康狀況);“Any requirements for lab values?”(實驗室指標);“Any requirements for medication use?”(藥物使用);“Any requirements for provider type or site of care?”(干預實施的場所)和“Additional eligibility criteria not listed above?”(其他情況)。用戶使用時可根據自己所研究的具體問題和使用的數據集信息依次完成上述內容的填寫。例如,在第1個問題的框中填入“Patients diagnosed with stage IV colon cancer(CC) in England”;而其他問題需填寫的內容包括4個框,以第2個問題為例,在其第1個框中填入招募期“1st Jan, 2014 to 31th Dec, 2017”,第2個框中填入數據來源“CORECT-R”,第3個框中填入變量名與說明“CCDX_YR (year of CC diagnosis)”,最后,在第4個框中填入缺失數據的處理算法“If time of CC diagnosis is missing, the date of first visit will be used”。完成模塊1所有項目的操作后,點擊位于填寫界面底部的“Review summary”(圖上未展示)可得到該模塊的匯總報告(附件圖6);團隊成員可對其進行討論,并利用“Post comment”備注討論內容,也可利用“Back”返回上一步進行修改。確定無誤后可點擊“Download report”下載該匯總報告,之后點擊“Proceed to module 2”進入模塊2“Outcomes”進行該模塊的操作。
模塊2“Outcomes”的內容共涉及2個方面(附件圖7、圖8)。第1個為“What type is it?”,即結局指標類型,包括二分類(Dichotomous)、連續性(Continuous)和時間-事件(Failure time)3種類型,示例研究的結局指標為“全因死亡率”,故選擇“Failure time”。第2個為“Define your outcome”,即定義結局指標(附件圖7)。在完成所有項目操作后,可參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖8),然后點擊“Proceed to module 3”進入模塊3“Follow-up period”進行該模塊的操作。
模塊3“Follow-up period”的內容共涉及2個主要方面(附件圖9、圖10)。第1個為“Censoring”(刪失),其下又包括“Administrative end of follow-up”(管理性隨訪結束)、“Loss to follow-up”(失訪)、“Other censoring events”(其他刪失事件)和“Do you expect that censoring may result in selection bias?”(刪失是否可能造成選擇偏倚)。第2個為“Competing event”(競爭事件),示例研究的終點結局為“全因死亡率”,不存在競爭事件(附件圖10)。在完成所有項目操作后,可同樣參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖10),然后點擊“Proceed to module 4”進入模塊4“Treatment strategies”進行該模塊的操作。
模塊4“Treatment strategies”的內容同樣涉及2個主要方面,即需要分別對治療組與對照組干預的具體情況進行說明(附件圖11、圖12)。具體操作時,首先在“Strategy label”框中填入干預名稱;其次需要完成“Type”下的多個問題,當所研究的干預為點干預(Point intervention)[5],例如,示例研究中的外科手術;則“Does this treatment strategy consist of an intervention that happens at baseline only?”應該選擇“Yes”;隨后需要完成“Describe the intervention in such a way that other people can implement it”(描述干預的細節,例如,劑量、頻次)以保證別人可以重復干預和回答“Do you allow a certain period of time (grace period) to implement this intervention? ”以明確是否有寬限期(即設定的允許接受干預的某個時間段),示例研究的寬限期為6個月[25],因此選擇“Yes”,并填入“Six months”。但當所研究的干預為持續治療策略(Sustained strategy),例如,從某個時間點開始服用某藥物,并需要一直服用3年,則需要選擇“No”, 隨后需要回答“Does this treatment strategy assign everybody to interventions at fixed times after baseline (regardless of changes in individual characteristics) ?”(是否在基線后的固定時間點對每個患者分配干預),當選擇“Yes”時,需要在“Describe the intervention required by this treatment strategy”下面填入干預的細節信息;以及回答“Do you allow a certain period of time (grace period) to implement this intervention?”(寬限期,同前);當選擇“No”時,則需要回答“What is the trigger and resulting intervention?”(觸發干預實施的事件)和“Do you allow a certain period of time (grace period) to implement this intervention?”(寬限期,同前)。對照組干預信息的填寫過程與治療組一致,參照治療組填寫即可。在完成所有項目操作后,可同樣參照模塊1的相關操作進行討論、修改和導出匯總報告(附件圖12),然后點擊“Proceed to module 5”進入模塊5“Adjustment variables”進行該模塊的操作。
模塊5“Adjustment variables”的操作比較復雜(附件圖13、圖14),主要是后續項目是否出現會受到其之前其他項目答案的影響。當“Causal contrasts of interest”(因果比較;當干預為點干預,即模塊4中“Does this treatment strategy consist of an intervention that happens at baseline only?”回答為“Yes”時,不出現該選項)選擇“Intention to treat”(意向治療效應)時,會出現“Patient demographics”(人口學特征)、“Baseline variables related to patient outcomes”(與結局相關的基線變量)、“Additional baseline variables”(其他基線變量)、“Post-baseline variables”(基線后變量;當模塊4中“Does this treatment strategy consist of an intervention that happens at baseline only?”回答為“Yes”時,不出現該選項)、“Loss-to-follow up variables”(失訪變量)和“Which variables are potentially important, but are not measured in your data?”(潛在重要但未測量的變量)6個項目。當選擇“Per protocol”(符合方案效應)時,會額外增加1個項目,即和“Do you have time-dependent confounding?If yes,please describe time-dependent confounders”(時依混雜因素,存在時需要描述)。示例研究的干預為點干預(附件圖13,默認估計符合方案效應),除需要完成“Patient demographics”“Baseline variables related to patient outcomes”“Additional baseline variables”“Loss-to-follow up variables”和“Which variables are potentially important, but are not measured in your data?”5個項目的操作外,還需要回答“Do you have an instrument variable? If yes, please specify”(是否有工具變量,存在時需要描述);在完成所有項目操作后,點擊“Review summary”(未展示,同附件圖7)得到匯總報告,見附件圖14。點擊“Proceed to module analysis”會自動生成建議的統計分析計劃“Analysis plan”(附件圖15),使用者可參考該內容進一步制定詳細的統計分析方案。最后再點擊“Download report”可下載Word版的完整報告進行進一步的編輯和調整。此外,該工具具有保存分析記錄的功能,因此,用戶可在下次重新登入賬戶后對已填寫的內容進行修改和調整。
3 討論
國際人用藥品注冊技術協調會強調藥物臨床研究的本質是因果推斷,而藥物研發和評價的核心問題就是明確藥物治療效應的存在性并估計其大小[26]。盡管已經發表了大量的評價藥物干預效果的觀察性真實世界研究,但調查同一問題的不同真實世界研究之間以及它們與對應的隨機對照試驗之間的結果常常存在較大差異,甚至互相矛盾[5,27,28];如此,不但限制了研究結果的推廣應用,而且導致了可避免的研究資源的巨大浪費和非必要的“碳足跡”的增加,同時還影響了監管部門、臨床醫生及公眾對真實世界證據的信任度[29-31]。造成上述問題的主要原因可能是缺少統一的高質量操作指南,從而使得很多觀察性真實世界研究的透明度不足;或者僅考慮了混雜而未能考慮不良影響更大的偏倚(例如,永恒時間偏倚和現用藥者偏倚,后者為選擇偏倚的一種)[5,28]。
近年來,目標試驗模擬研究框架被正式確立,它能夠使得基于真實世界數據開展的觀察性研究更加透明和嚴格,使得分析結果的因果效應更具可解釋性[5,13,19]。目前,該框架已經被廣泛用于評價不同干預措施(例如,藥物、疫苗、營養、手術和社會政策干預)對各種健康相關問題(例如,心血管疾病、腎病、糖尿病、COVID-19和腫瘤)的因果效應[5,32-34];也有學者將其應用于衛生經濟學評價研究[4,34]。此外,最近有學者認為該框架應該成為評價醫療干預效果的比較觀察性研究的金標準方法,但也有學者對此持反對觀點[5,19]。開展目標試驗模擬研究的關鍵點是同步符合納入標準、干預措施分配和隨訪起點這3個時間點;而在真正的隨機對照試驗研究中,隨機化時就會自動同步它們[5,7]。但是,需要注意的是,目標試驗模擬研究并不是一種新的流行病學研究設計,也不指定具體的統計分析方法,解決不同的研究問題往往需要根據實際情況選擇不同的研究設計和對應的統計分析方法[4,5]。此外,目標試驗模擬研究也具有其局限性[4,5,35],例如,無法模擬沒有臨床數據的新藥物、無法解決數據本身存在的測量偏倚問題和不能保證沒有殘余混雜。Zhang Y團隊于2019年開發了專門用于輔助目標試驗模擬研究實施的CERBOT工具[24],主要由5個模塊組成,通過填寫5個模塊的內容可以有效地指導研究人員設計和實施目標試驗模擬研究和明確真實世界數據的特征;最終該工具可根據所填寫的模塊內容自動生成統計分析計劃建議并提供相應的理由;同時,工具的網頁上還提供了開展目標試驗模擬研究可能涉及的統計方法及統計軟件包的介紹。本研究對該款具有團隊協同操作和記錄保存功能的新工具的基本情況進行了介紹,并基于實例演示了該工具的操作過程,以期幫助提高國內醫療領域真實世界研究的質量,最終為臨床實踐和監管決策提供高質量的真實世界證據。
聲明 本文不存在任何利益沖突。