引用本文: 曹蘭蘭, 陳悅, 陶麗紅. 癲癇持續狀態伴反復急性腎損傷一例. 癲癇雜志, 2024, 10(4): 360-363. doi: 10.7507/2096-0247.202404002 復制
版權信息: ?四川大學華西醫院華西期刊社《癲癇雜志》版權所有,未經授權不得轉載、改編
癲癇持續狀態(Status epilepticus,SE)被定義為持續5 min或5 min以上的臨床和或腦電圖發作活動或復發性發作活動[1]。癲癇發作有因橫紋肌溶解[2]或急性高尿酸血癥[3]引起急性腎損傷(Acute kidney injury,AKI)的潛在風險。本文將介紹1例因癲癇持續狀態發作引起反復AKI的病例。
病例資料 患者 男,31歲。因“突發肢體抽搐伴意識障礙1 h”于2019年2月首次就診我院,患者出現四肢抽搐、上肢屈曲、下肢伸直、雙眼上翻、牙關緊閉,伴有意識不清,發作持續6 min后緩解,30 min后再次發作,發作間期仍有意識障礙,擬“SE”收治入院,2022年9月因“突發肢體抽搐伴意識障礙2 h”再次就診我院,患者出現四肢抽搐,上肢屈曲,下肢伸直,雙眼上翻,牙關緊閉,伴有意識不清,發作持續10 min后緩解,1 h后再次發作,發作間期有意識障礙,擬“SE”收治入院。既往有車禍外傷致腦部手術病史7年余,予對癥治療后好轉出院。
體格檢查:昏迷狀態,頭顱左側皮膚見陳舊性手術疤痕長約10 cm,雙側瞳孔等大等圓,約2.5 mm,對光反射遲鈍。頸稍抵抗,聽診兩肺呼吸音粗,可聞及濕羅音;心率130次/min,律齊,心臟各瓣膜區未聞及病理性雜音;腹部無膨隆,腹肌無緊張,肝脾肋下未觸及,腸鳴音2~5次/min。四肢肌張力偏高,四肢肌力查體不配合;雙側Babinski征(未引出)。
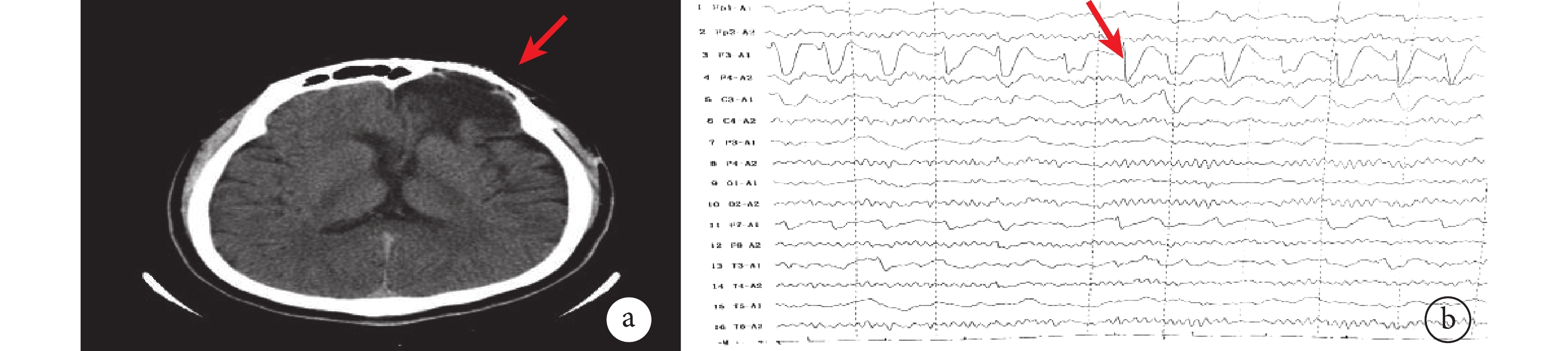 圖1
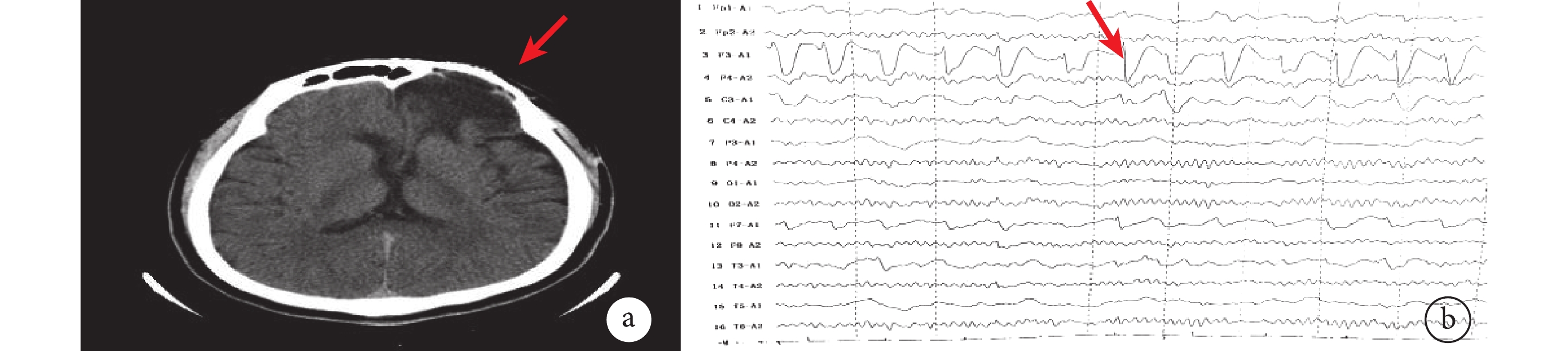
患者頭部CT及腦電圖
圖1
患者頭部CT及腦電圖
a. 患者2022年入院頭顱CT,箭頭示左側額葉陳舊性病灶;b. 患者2022年入院腦電圖,箭頭示棘波放電
患者2019年入院后診斷癲癇持續狀態,予咪達唑侖鎮靜、氣管插管,同時糾正電解質紊亂,營養支持等治療,病程中出現急性腎功能衰竭,予連續腎臟替代療法(Continuous renal replacement therapy,CRRT)治療,治療后復查肌酐較前下降,予停止透析治療,隨后病情好轉出院,出院服用托吡酯100 mg/d、丙戊酸鈉100 mg/d,出院3月后門診查腎功能正常,且癲癇未再發作,直至2022年癲癇再次發作,入院治療情況較上次無明顯區別,2022年出院1個月后門診復查腎功能正常,最近1次2023年門診復查腎功能正常,且癲癇未再發作。
討論 該患者2次在癲癇持續狀態后發生了急性腎損傷,根據患者的生化檢查,考慮2次的急性腎損傷有不同的原因,分別為橫紋肌溶解癥和高尿酸血癥。橫紋肌溶解癥是癲癇的一個常見并發癥[4],有研究曾報道了5例癲癇發作引起的橫紋肌溶解癥,其中4例發生了AKI[5]。橫紋肌溶解癥的定義是骨骼肌的急性破壞、肌纖維凋亡和肌纖維碎片恢復。隨后將肌細胞內容物(包括細胞內代謝物(尿素、鉀和磷))和細胞內蛋白(如肌紅蛋白、肌酸激酶、天冬氨酸轉氨酶和乳酸脫氫酶)釋放到血液循環中[6]。且橫紋肌溶解癥中導致AKI的病因復雜。可能的病因包括肌紅蛋白的直接腎小管毒性、血管收縮、腎小管管型形成以及低血容量引起的腎缺血[6]。它可能導致肌肉疼痛、無力、緊繃和腫脹[7],進而導致一系列以高鉀血癥、高磷血癥、高尿酸血癥、肌酸激酶升高和肌紅蛋白升高為特征的生理病變影響內部環境的穩定性。因為橫紋肌溶解最可靠和最敏感的線索是肌酸激酶水平升高[8],所以需要進行實驗室血清肌酸激酶檢測來確認橫紋肌溶解癥的診斷,血清肌酸激酶在肌肉損傷開始后12 h內升高,在24~72 h達到峰值,并在肌肉損傷后約10 d恢復正常[9]。其他檢查包括血清肌紅蛋白、鉀、鈣、尿素、肌酸、轉氨酶、乳酸脫氫酶和尿試紙。橫紋肌溶解癥的診斷標準:如患者有可疑的病因以及相關的相關癥狀(肌無力、肌肉酸痛、尿液顏色的改變),并同時伴有血清肌酶譜顯著升高,肌酸激酶高于正常峰值的5 倍,并排除其他可能引起肌酸激酶升高的疾病(心肌梗 死等)可診斷[10]。尿隱血陽性,可見紅細胞,也有助于橫紋肌溶解的診斷[11]。
患者在第一次住院期間未見明顯的尿液顏色改變,兩次住院期間尿量未見減少,原因可能是在正常生理學中,血漿肌紅蛋白是一種深紅色蛋白質,與結合珠蛋白結合;循環中肌紅蛋白的血清濃度非常低。在橫紋肌溶解過程中,肌肉細胞的分解導致大量肌紅蛋白釋放到循環中,導致血清肌紅蛋白濃度升高。雖然肌紅蛋白的半衰期很短,但我們仍然發現,在這個案例中,血清肌紅蛋白水平遠高于正常上限,表明嚴重的肌肉損傷。當肌紅蛋白的血漿水平高于0.5~1.5 mg / dL時,它超過了結合珠蛋白結合能力,肌紅蛋白通過尿液排泄,這被稱為肌紅蛋白尿[12]。然而,只有當肌紅蛋白的血漿濃度達到100 mg / dL時,這對應于200 g肌肉組織的破壞,尿液中的肌紅蛋白水平才會呈茶色或可樂色[13]。因此有色尿液不一定總是存在于橫紋肌溶解中,這可以解釋該患者尿液顏色無明顯改變。另外一種可能性是當肌紅蛋白被腎小球濾過時,它可能會形成管型并阻塞小管,最終導致急性腎功能衰竭。腎小管阻塞可能會阻止肌紅蛋白排泄到尿液中,導致尿液清澈伴血漿肌紅蛋白升高[14]。其次該患者2次入院時均處于昏迷狀態,急性腎衰期間意識朦朧,不能提供肌肉酸痛等信息,但是患者在2019年住院第1周左右時查肌酸激酶顯著增高,且高于正常峰值的5 倍 ,其次該患者血清肌紅蛋白顯著增高,也符合橫紋肌溶解的標準[15],并且患者心電圖正常,排除心肌梗死,因此考慮患者在第1次住院中發生了橫紋肌溶解.
Warren等[16]于1975年首次報道了大發作或癲癇持續狀態復發后急性重度高尿酸血癥。隨后在1978年,Luhdorf等[17]發現24例患者在10次或11次以上大發作后12 h內血清尿酸水平(Uric acid,UA)顯著升高,在其中6例嚴重高尿酸血癥患者中,有兩名出現腎功能受損。而血液中 UA 水平升高可能是由血液中 UA 的產生增加或清除率降低引起的。Saugstad等[18]提出,癲癇發作后缺氧組織過度釋放次黃嘌呤可能被黃嘌呤氧化酶轉化為尿酸,從而導致高尿酸血癥。由于尿酸也被認為是一種有效的抗氧化劑,因此尿酸升高可能是為了抵消癲癇發作期間的氧化應激[19]。且伴隨癲癇發作的代謝性酸中毒會產生酸性尿液,其中尿酸的溶解度較低,導致尿酸在腎小管腔內沉淀[17]。其次,癲癇發作期間腎上腺素能狀態的體溫過高和大量出汗可能有利于脫水并增加腎小管水的重吸收,增加腎小管尿酸鹽濃度[20],并且在發作期間血流從內臟器官分流到肌肉所致腎缺血也可能導致腎損傷[17],有病例報道,SE僅2 h后,在初始血液檢查中檢測到高尿酸血癥;然而在以前的報道沒有明確癲癇持續性發作會導致血液UA水平的迅速、大幅度增加[21]。另一種解釋是血液UA清除率降低。UA 被腎小球濾過,幾乎完全重吸收在近端小管的 S1 段。隨后出現腎小管分泌,大多數 UA 的重吸收再次發生在近端小管的 S2 段內,因此尿液中僅出現少量 UA[22]。在高尿酸血癥中,濾過的UA可能進一步濃縮并沉淀在小管中,這可能會加劇肌紅蛋白引起的梗阻。UA晶體和肌紅蛋白的腎小管內沉積增加腎小管壓并減少腎血流量,從而減慢腎小球濾過并導致腎功能不全。因此推測這可能是本例AKI的潛在機制盡管。也表明SE后高尿酸血癥可能會加劇腎衰竭的風險。通過早期檢測,這可能是可以避免的。
綜上所述,癲癇發作后,患者可能有幾個潛在的AKI危險因素,目前國內對癲癇發作后發生橫紋肌溶解導致AKI的報道較多,但是目前無統一的診療指南。 不少研究建議橫紋肌溶解在早期就要進行積極的液體復蘇治療來預防AKI的發生[15,23]。2022年1月,美國創傷外科協會重癥監護委員會發布了橫紋肌溶解癥共識文件,建議乳酸林格氏液或生理鹽水(0.9% 或 0.45%)作為橫紋肌溶解癥復蘇的液體[24]。起始速率為400 mL/h,目標導向治療尿量為 1~3 mL/(kg·h),最高可達 300 cc/h,且應根據尿量滴定,確保患者接受充分復蘇而不會出現液體蠕變。當出現藥物難以控制的嚴重的酸/堿紊亂、電解質異常和血容量過高時,應及時進行CRRT治療。其次,目前對于高尿酸血癥可能會導致AKI的報道較少,因此除了重視癲癇發作后橫紋肌溶解的診斷,也不應延遲或忽視癲癇發作后急性高尿酸血癥的診斷,以預防AKI。
利益沖突聲明 所有作者無利益沖突。
癲癇持續狀態(Status epilepticus,SE)被定義為持續5 min或5 min以上的臨床和或腦電圖發作活動或復發性發作活動[1]。癲癇發作有因橫紋肌溶解[2]或急性高尿酸血癥[3]引起急性腎損傷(Acute kidney injury,AKI)的潛在風險。本文將介紹1例因癲癇持續狀態發作引起反復AKI的病例。
病例資料 患者 男,31歲。因“突發肢體抽搐伴意識障礙1 h”于2019年2月首次就診我院,患者出現四肢抽搐、上肢屈曲、下肢伸直、雙眼上翻、牙關緊閉,伴有意識不清,發作持續6 min后緩解,30 min后再次發作,發作間期仍有意識障礙,擬“SE”收治入院,2022年9月因“突發肢體抽搐伴意識障礙2 h”再次就診我院,患者出現四肢抽搐,上肢屈曲,下肢伸直,雙眼上翻,牙關緊閉,伴有意識不清,發作持續10 min后緩解,1 h后再次發作,發作間期有意識障礙,擬“SE”收治入院。既往有車禍外傷致腦部手術病史7年余,予對癥治療后好轉出院。
體格檢查:昏迷狀態,頭顱左側皮膚見陳舊性手術疤痕長約10 cm,雙側瞳孔等大等圓,約2.5 mm,對光反射遲鈍。頸稍抵抗,聽診兩肺呼吸音粗,可聞及濕羅音;心率130次/min,律齊,心臟各瓣膜區未聞及病理性雜音;腹部無膨隆,腹肌無緊張,肝脾肋下未觸及,腸鳴音2~5次/min。四肢肌張力偏高,四肢肌力查體不配合;雙側Babinski征(未引出)。
 圖1
患者頭部CT及腦電圖
圖1
患者頭部CT及腦電圖
a. 患者2022年入院頭顱CT,箭頭示左側額葉陳舊性病灶;b. 患者2022年入院腦電圖,箭頭示棘波放電
患者2019年入院后診斷癲癇持續狀態,予咪達唑侖鎮靜、氣管插管,同時糾正電解質紊亂,營養支持等治療,病程中出現急性腎功能衰竭,予連續腎臟替代療法(Continuous renal replacement therapy,CRRT)治療,治療后復查肌酐較前下降,予停止透析治療,隨后病情好轉出院,出院服用托吡酯100 mg/d、丙戊酸鈉100 mg/d,出院3月后門診查腎功能正常,且癲癇未再發作,直至2022年癲癇再次發作,入院治療情況較上次無明顯區別,2022年出院1個月后門診復查腎功能正常,最近1次2023年門診復查腎功能正常,且癲癇未再發作。
討論 該患者2次在癲癇持續狀態后發生了急性腎損傷,根據患者的生化檢查,考慮2次的急性腎損傷有不同的原因,分別為橫紋肌溶解癥和高尿酸血癥。橫紋肌溶解癥是癲癇的一個常見并發癥[4],有研究曾報道了5例癲癇發作引起的橫紋肌溶解癥,其中4例發生了AKI[5]。橫紋肌溶解癥的定義是骨骼肌的急性破壞、肌纖維凋亡和肌纖維碎片恢復。隨后將肌細胞內容物(包括細胞內代謝物(尿素、鉀和磷))和細胞內蛋白(如肌紅蛋白、肌酸激酶、天冬氨酸轉氨酶和乳酸脫氫酶)釋放到血液循環中[6]。且橫紋肌溶解癥中導致AKI的病因復雜。可能的病因包括肌紅蛋白的直接腎小管毒性、血管收縮、腎小管管型形成以及低血容量引起的腎缺血[6]。它可能導致肌肉疼痛、無力、緊繃和腫脹[7],進而導致一系列以高鉀血癥、高磷血癥、高尿酸血癥、肌酸激酶升高和肌紅蛋白升高為特征的生理病變影響內部環境的穩定性。因為橫紋肌溶解最可靠和最敏感的線索是肌酸激酶水平升高[8],所以需要進行實驗室血清肌酸激酶檢測來確認橫紋肌溶解癥的診斷,血清肌酸激酶在肌肉損傷開始后12 h內升高,在24~72 h達到峰值,并在肌肉損傷后約10 d恢復正常[9]。其他檢查包括血清肌紅蛋白、鉀、鈣、尿素、肌酸、轉氨酶、乳酸脫氫酶和尿試紙。橫紋肌溶解癥的診斷標準:如患者有可疑的病因以及相關的相關癥狀(肌無力、肌肉酸痛、尿液顏色的改變),并同時伴有血清肌酶譜顯著升高,肌酸激酶高于正常峰值的5 倍,并排除其他可能引起肌酸激酶升高的疾病(心肌梗 死等)可診斷[10]。尿隱血陽性,可見紅細胞,也有助于橫紋肌溶解的診斷[11]。
患者在第一次住院期間未見明顯的尿液顏色改變,兩次住院期間尿量未見減少,原因可能是在正常生理學中,血漿肌紅蛋白是一種深紅色蛋白質,與結合珠蛋白結合;循環中肌紅蛋白的血清濃度非常低。在橫紋肌溶解過程中,肌肉細胞的分解導致大量肌紅蛋白釋放到循環中,導致血清肌紅蛋白濃度升高。雖然肌紅蛋白的半衰期很短,但我們仍然發現,在這個案例中,血清肌紅蛋白水平遠高于正常上限,表明嚴重的肌肉損傷。當肌紅蛋白的血漿水平高于0.5~1.5 mg / dL時,它超過了結合珠蛋白結合能力,肌紅蛋白通過尿液排泄,這被稱為肌紅蛋白尿[12]。然而,只有當肌紅蛋白的血漿濃度達到100 mg / dL時,這對應于200 g肌肉組織的破壞,尿液中的肌紅蛋白水平才會呈茶色或可樂色[13]。因此有色尿液不一定總是存在于橫紋肌溶解中,這可以解釋該患者尿液顏色無明顯改變。另外一種可能性是當肌紅蛋白被腎小球濾過時,它可能會形成管型并阻塞小管,最終導致急性腎功能衰竭。腎小管阻塞可能會阻止肌紅蛋白排泄到尿液中,導致尿液清澈伴血漿肌紅蛋白升高[14]。其次該患者2次入院時均處于昏迷狀態,急性腎衰期間意識朦朧,不能提供肌肉酸痛等信息,但是患者在2019年住院第1周左右時查肌酸激酶顯著增高,且高于正常峰值的5 倍 ,其次該患者血清肌紅蛋白顯著增高,也符合橫紋肌溶解的標準[15],并且患者心電圖正常,排除心肌梗死,因此考慮患者在第1次住院中發生了橫紋肌溶解.
Warren等[16]于1975年首次報道了大發作或癲癇持續狀態復發后急性重度高尿酸血癥。隨后在1978年,Luhdorf等[17]發現24例患者在10次或11次以上大發作后12 h內血清尿酸水平(Uric acid,UA)顯著升高,在其中6例嚴重高尿酸血癥患者中,有兩名出現腎功能受損。而血液中 UA 水平升高可能是由血液中 UA 的產生增加或清除率降低引起的。Saugstad等[18]提出,癲癇發作后缺氧組織過度釋放次黃嘌呤可能被黃嘌呤氧化酶轉化為尿酸,從而導致高尿酸血癥。由于尿酸也被認為是一種有效的抗氧化劑,因此尿酸升高可能是為了抵消癲癇發作期間的氧化應激[19]。且伴隨癲癇發作的代謝性酸中毒會產生酸性尿液,其中尿酸的溶解度較低,導致尿酸在腎小管腔內沉淀[17]。其次,癲癇發作期間腎上腺素能狀態的體溫過高和大量出汗可能有利于脫水并增加腎小管水的重吸收,增加腎小管尿酸鹽濃度[20],并且在發作期間血流從內臟器官分流到肌肉所致腎缺血也可能導致腎損傷[17],有病例報道,SE僅2 h后,在初始血液檢查中檢測到高尿酸血癥;然而在以前的報道沒有明確癲癇持續性發作會導致血液UA水平的迅速、大幅度增加[21]。另一種解釋是血液UA清除率降低。UA 被腎小球濾過,幾乎完全重吸收在近端小管的 S1 段。隨后出現腎小管分泌,大多數 UA 的重吸收再次發生在近端小管的 S2 段內,因此尿液中僅出現少量 UA[22]。在高尿酸血癥中,濾過的UA可能進一步濃縮并沉淀在小管中,這可能會加劇肌紅蛋白引起的梗阻。UA晶體和肌紅蛋白的腎小管內沉積增加腎小管壓并減少腎血流量,從而減慢腎小球濾過并導致腎功能不全。因此推測這可能是本例AKI的潛在機制盡管。也表明SE后高尿酸血癥可能會加劇腎衰竭的風險。通過早期檢測,這可能是可以避免的。
綜上所述,癲癇發作后,患者可能有幾個潛在的AKI危險因素,目前國內對癲癇發作后發生橫紋肌溶解導致AKI的報道較多,但是目前無統一的診療指南。 不少研究建議橫紋肌溶解在早期就要進行積極的液體復蘇治療來預防AKI的發生[15,23]。2022年1月,美國創傷外科協會重癥監護委員會發布了橫紋肌溶解癥共識文件,建議乳酸林格氏液或生理鹽水(0.9% 或 0.45%)作為橫紋肌溶解癥復蘇的液體[24]。起始速率為400 mL/h,目標導向治療尿量為 1~3 mL/(kg·h),最高可達 300 cc/h,且應根據尿量滴定,確保患者接受充分復蘇而不會出現液體蠕變。當出現藥物難以控制的嚴重的酸/堿紊亂、電解質異常和血容量過高時,應及時進行CRRT治療。其次,目前對于高尿酸血癥可能會導致AKI的報道較少,因此除了重視癲癇發作后橫紋肌溶解的診斷,也不應延遲或忽視癲癇發作后急性高尿酸血癥的診斷,以預防AKI。
利益沖突聲明 所有作者無利益沖突。